Matières
Niveaux
La conductibilité électrique est la capacité d’une substance à laisser passer un courant électrique.
La conductibilité électrique se mesure qualitativement à l’aide d’un détecteur de conductibilité électrique (DCE) à témoin lumineux. Ce type de DCE ne fournit pas de valeur numérique quant au degré de conductibilité d’une substance. L’observation du témoin lumineux du DCE permet de déterminer si le courant circule ou non dans la substance.
Lorsque le témoin lumineux du DCE s’allume, la substance conduit l’électricité.
Lorsque le témoin lumineux du DCE ne s’allume pas, la substance ne conduit pas l’électricité.


Les matériaux qui permettent le passage d’un courant électrique sont appelés des conducteurs. Les substances qui ne permettent pas le passage d’un courant électrique sont des isolants. À l’échelle atomique, c’est l’attraction des électrons par le noyau des atomes qui différencie les conducteurs des isolants.
Les électrons d’un conducteur sont faiblement attirés par le noyau de ses atomes. Cela permet le mouvement libre des électrons, donc le passage du courant électrique. La plupart des métaux sont d’excellents conducteurs électriques. Les matériaux conducteurs d’électricité sont utilisés pour assurer la fonction de conduction dans les circuits électriques.
L’argent, le cuivre et l’or sont des métaux d’une grande conductibilité électrique.

Un câble électrique en cuivre

Des connecteurs en or et des soudures en argent sur un circuit imprimé
Les électrons d’un isolant sont fortement attirés par le noyau de ses atomes. Il est donc difficile pour les électrons de se déplacer d’un atome à un autre. Comme le passage d’un courant électrique dépend du mouvement des électrons, le courant ne circule pas dans un matériau isolant.
Les matières plastiques, les bois et les céramiques sont des isolants électriques. Les matériaux isolants sont utilisés pour assurer la fonction d’isolation dans les circuits électriques.
Le caoutchouc et le verre sont des isolants électriques.

Des fils conducteurs recouverts d’une gaine isolante en caoutchou

Des disques isolants en verre sur des lignes à haute tension
La conductibilité électrique des matériaux conducteurs varie selon différents facteurs.
La conductibilité électrique dépend de l’attraction des électrons par le noyau des atomes du matériau. Lorsque cette attraction est faible, la conductibilité électrique est élevée. Le tableau suivant décrit la conductibilité de quelques métaux conducteurs.
| Métal | Conductibilité électrique (S/m) |
|---|---|
| Argent (Ag) | 6,30 × 107 |
| Cuivre (Cu) | 5,96 × 107 |
| Or (Au) | 4,10 × 107 |
| Aluminium (Al) | 3,50 × 107 |
| Fer (Fe) | 1,00 x 107 |
| Acier doux (alliage de fer et carbone) | 6,99 × 106 |
La conductibilité électrique se mesure en siemens par mètre (S/m). Dans le tableau précédent, on remarque que les meilleurs conducteurs sont l’argent, le cuivre et l’or.
Un fil dont le diamètre est plus grand contient plus d’atomes. Le débit d’électrons en mouvement dans le fil est alors plus élevé. Un fil permettant un meilleur mouvement des électrons a donc une meilleure conductibilité électrique.
Lorsque le diamètre d’un conducteur augmente, la conductibilité électrique augmente.
Pour ces deux fils conducteurs en cuivre de même longueur, c’est le fil plus épais qui a la meilleure conductibilité électrique.
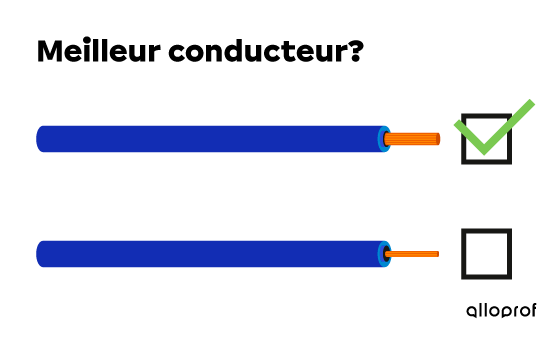
Deux fils conducteurs de diamètre différent
Le mouvement des électrons dans un fil conducteur entraine des collisions entre les autres électrons et les parois isolantes du fil, ce qui nuit au passage du courant. Plus le fil est court, moins les électrons ont l’occasion de faire des collisions, ce qui facilite le passage du courant.
Ainsi, lorsque la longueur d’un conducteur augmente, la conductibilité électrique diminue.
Pour ces deux fils conducteurs en cuivre de même diamètre, c’est le fil le plus court qui a la meilleure conductibilité électrique.

Deux fils conducteurs de longueur différente
L’augmentation de la température d’un conducteur entraine l’agitation de ses particules. Cette agitation s’ajoute au mouvement désordonné des électrons et augmente les collisions dans le fil. Davantage de collisions rendent le déplacement des électrons plus difficile, ce qui diminue la conductibilité.
Ainsi, lorsque la température d’un conducteur augmente, la conductibilité électrique diminue.
Une salle de serveurs informatiques est conçue pour que l’air y reste le plus frais possible.
Des étagères aérées, des systèmes de climatisation et même des liquides de refroidissement sont utilisés dans ce genre d’installation.
La fraicheur permet aux circuits électriques de conserver une meilleure conductibilité, donc une meilleure efficacité.

Un centre de données
La supraconductivité est un phénomène caractérisé par l’absence de résistance électrique à l’intérieur d’un matériau. Ces supraconducteurs ont une conductibilité électrique infinie, ce qui permet le passage du courant sans aucune perte d’énergie. Ce phénomène permet d’engendrer des champs magnétiques d’intensité très élevée.
Pour atteindre la supraconductivité, on doit être dans des conditions extrêmement froides, tout près du zéro absolu (-273,15 °C). Dans ces conditions, les particules sont pratiquement immobiles, laissant le champ libre au déplacement des électrons.
Le déplacement ultra rapide des trains à sustentation magnétique (Maglev) est dû à la supraconductivité. Le Transrapid de Shanghai effectue la liaison entre le centre-ville et l’aéroport (30 km) en 7 minutes et 20 secondes.

Le Transrapid de Shanghai, Chine
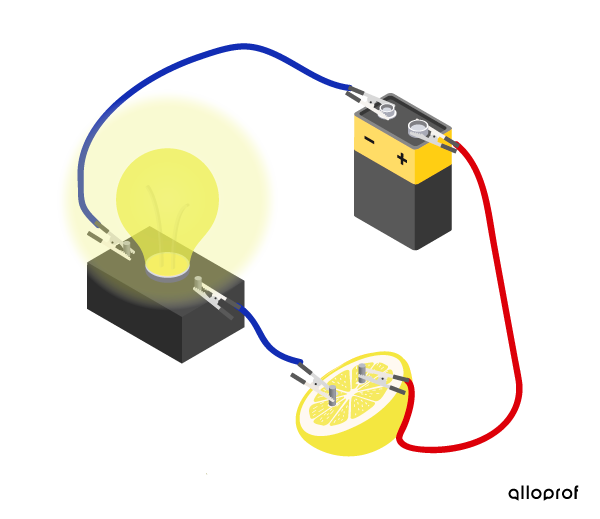
Il n’y a pas que les matériaux qui peuvent conduire un courant électrique. Les solutions d’électrolytes telles que les solutions d’acide, de base ou de sel conduisent le courant électrique, car elles contiennent des ions mobiles. Les ions, tout comme les électrons, possèdent une charge électrique. Leur déplacement permet le passage d’un courant électrique. La conductibilité électrique d’une solution dépend de sa concentration en ions.
Le jus de citron (solution acide) contient suffisamment d’ions mobiles pour permettre le passage du courant de la pile à l’ampoule. L’ampoule s’allume.