Matières
Niveaux
Le diagramme énergétique d'une transformation est un graphique qui présente les différents niveaux d'énergie des substances présentes en fonction de la progression de la transformation.
On peut illustrer le déroulement d'une réaction chimique à l'aide d'un diagramme énergétique. Ce diagramme permet de visualiser la différence d'énergie entre les réactifs et les produits impliqués dans une réaction. Il illustre également la hausse d'énergie accompagnant la formation du complexe activé. On peut donc suivre la progression du niveau d'énergie tout au long de la réaction.
Un diagramme énergétique permet de calculer la variation d'enthalpie se déroulant au cours d'une réaction chimique. Pour ce faire, le diagramme énergétique contient une courbe possédant trois niveaux distincts. On retrouve d'abord le niveau d'enthalpie des réactifs (en kJ/mol) à la gauche du graphique alors que celui des produits se trouve à la droite du graphique. Au centre, la hausse d'enthalpie accompagnant la formation du complexe activé est illustrée, ce qui correspond à l'énergie d'activation.
Les graphiques suivants illustrent l'allure que peut avoir un diagramme énergétique dans le cas d'une réaction endothermique (à gauche) et d'une réaction exothermique (à droite).
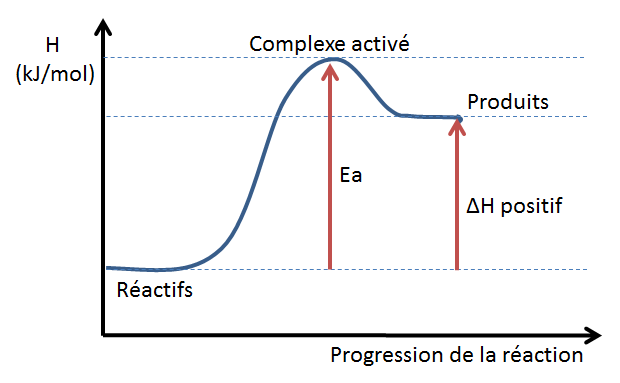
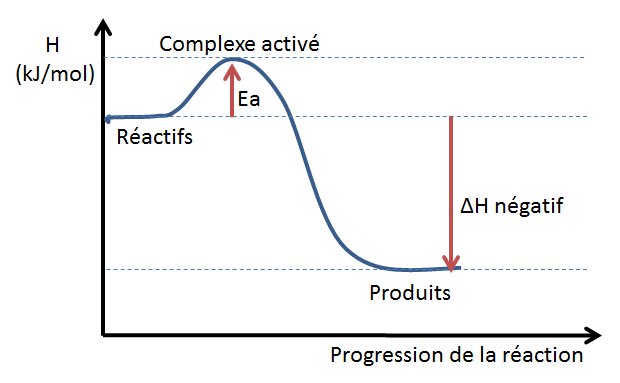
L'interprétation d'un diagramme énergétique permet de déterminer si une réaction est exothermique ou endothermique, soit par l'allure générale de la courbe ou en calculant la variation d'enthalpie de la réaction. À partir d'un diagramme énergétique, on peut aussi évaluer l'importance de l'énergie d'activation d'une réaction et comparer les réactions directe et inverse.
Il est possible de déterminer si une réaction absorbe ou dégage de l'énergie à partir de l'allure générale de la courbe. Pour se faire, il faut tracer une flèche verticale partant du niveau d'enthalpie des réactifs et terminant au niveau d'enthalpie des produits.
Exemple d'un diagramme énergétique d'une réaction endothermique: Le niveau d'enthalpie des produits est supérieur à celui des réactifs. La variation d'enthalpie est donc positive.
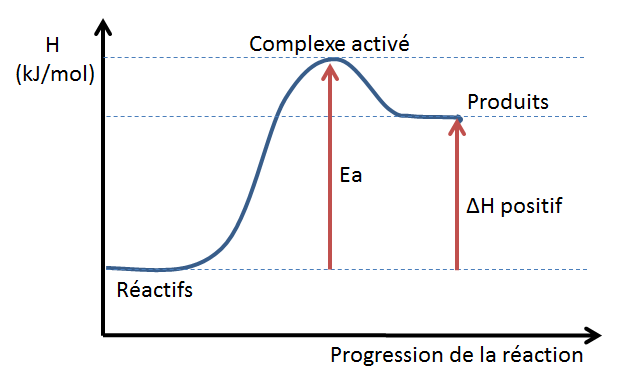
Exemple d'un diagramme énergétique d'une réaction exothermique: Le niveau d'enthalpie des produits est inférieur à celui des réactifs. La variation d'enthalpie est donc négative.
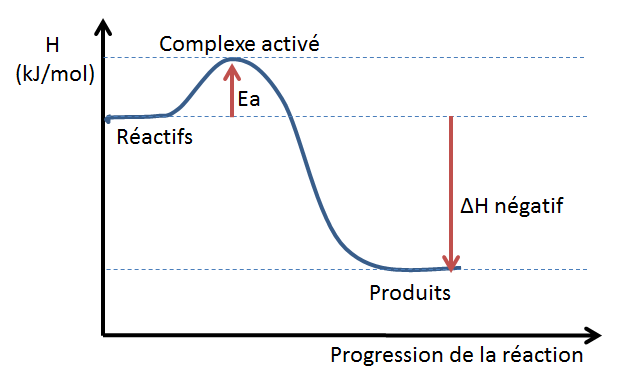
Il est possible de déterminer si une réaction absorbe ou dégage de l'énergie en calculant la variation d'enthalpie de la réaction. Le diagramme énergétique indique généralement, sur l'axe des ordonnées, la valeur énergétique des réactifs et des produits.
Pour déterminer la variation d'enthalpie, il suffit de soustraire l'enthalpie des réactifs de l'enthalpie des produits. Si la valeur est positive, la réaction est endothermique alors qu'elle est exothermique si la valeur obtenue est négative.
La formule mathématique suivante permet de déterminer la variation d'enthalpie:
ΔH=Hp−Hr
Si la valeur obtenue est positive, la réaction est endothermique.
Si la valeur obtenue est négative, la réaction est exothermique.
Il est possible d'évaluer l'importance de l'énergie d'activation d'une réaction. L'énergie d'activation est différente pour chaque réaction. Plus l'énergie d'activation est élevée et plus la réaction se déroule lentement. À l'inverse, plus elle est faible et plus la réaction est rapide.
L'énergie d'activation peut parfois être très faible, voire pratiquement nulle. Lorsque les molécules de réactifs ont suffisamment d'énergie pour franchir la barrière de l'énergie d'activation sans qu'il soit nécessaire de fournir davantage d'énergie, il s'agit d'une réaction spontanée. Le cas d'une énergie d'activation nulle est théorique, car la formation d'un complexe activé implique toujours une demande en énergie.
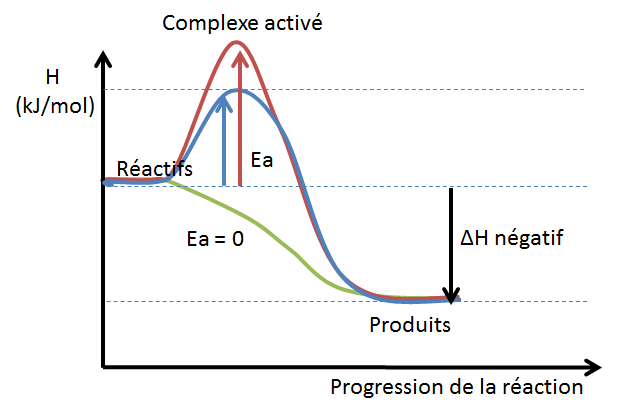
Le diagramme énergétique ci-dessous montre la variation d'enthalpie pour différentes réactions. La variation d'enthalpie est identique pour les trois réactions. Toutefois, l'énergie d'activation nécessaire à l'amorce de la réaction change. Elle est élevée dans la réaction en rouge, moyenne dans la bleue et nulle dans pour la courbe verte. On peut donc dire que la réaction rouge est relativement lente alors que la réaction verte serait spontanée.
Une réaction directe se déroule lorsque les réactifs deviennent des produits.
Une réaction inverse se déroule lorsque les produits deviennent des réactifs.
La majorité des réactions sont irréversibles, c'est-à-dire qu'elles ne peuvent se produire que dans un seul sens. C'est entre autre le cas de toutes les réactions impliquant une combustion.
Certaines réactions chimiques peuvent se produire dans les deux directions, dans leur sens directe et inverse. Il s'agit alors de réactions réversibles.
La décomposition de l'eau est la réaction inverse de la synthèse de l'eau.
Décomposition de l'eau:
2H2O(g)+488kJ→2H2(g)+O2(g)
Synthèse de l'eau:
2H2(g)+O2(g)→2H2O(g)+488kJ
Pour obtenir la réaction inverse d'une réaction, il suffit d'intervertir les réactifs et les produits. Aussi, la réaction inverse d'une réaction endothermique sera exothermique, et vice versa. Bien qu'il soit possible de le faire, il n'est pas nécessaire de tracer un nouveau diagramme énergétique lorsqu'on veut interpréter la réaction inverse. Comme on lit le diagramme énergétique de la réaction directe de gauche à droite, il suffit simplement de l'interpréter de droite à gauche pour quantifier la réaction inverse.
On lit le diagramme de gauche à droite pour la synthèse de l'eau alors qu'on lit le diagramme de droite à gauche pour la décomposition de l'eau.
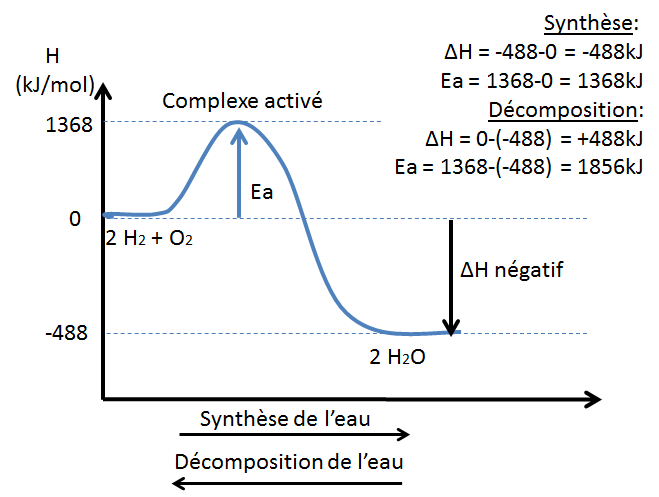
L'énergie d'activation n'est pas la même dans les deux sens d'une réaction. Cependant, la variation d'enthalpie est la même en valeur absolue, car les enthalpies des réactifs et des produits sont simplement inversées.