Populaires
Re : Question
Salut :D
Cette fiche sur les types d'agriculture et les différentes pratiques t'aidera certainement à chercher quels sont les changements avec l'invention de nouvelles techniques agricoles.
Bonne recherche :D À ta prochaine question :)
Re : Question
Diversité du monde paysan de l'Ancien Régime
Les dépendants, d'abord : au bas de l'échelle, le mendiant ; puis le journalier, manouvrier, brassier ; puis les petits exploitants, propriétaires ou non de petites exploitations à peine suffisantes pour survivre.
Re : Question
Bonsoir MinotaureDelta,
Merci d'utiliser la Zone d'entraide! :)
C'est plutôt le vassal qui jure fidélité au seigneur en échange d'une terre agricole, appelée à cette époque un fief ou une tenure.
Pour en savoir plus sur la société féodale, c'est juste ici :
N'hésite pas à nous réécrire si tu as d'autres questions! :)
Marilee
Re : Question
Bonsoir FraiseEfficace,
Merci d'utiliser la Zone d'entraide! :)
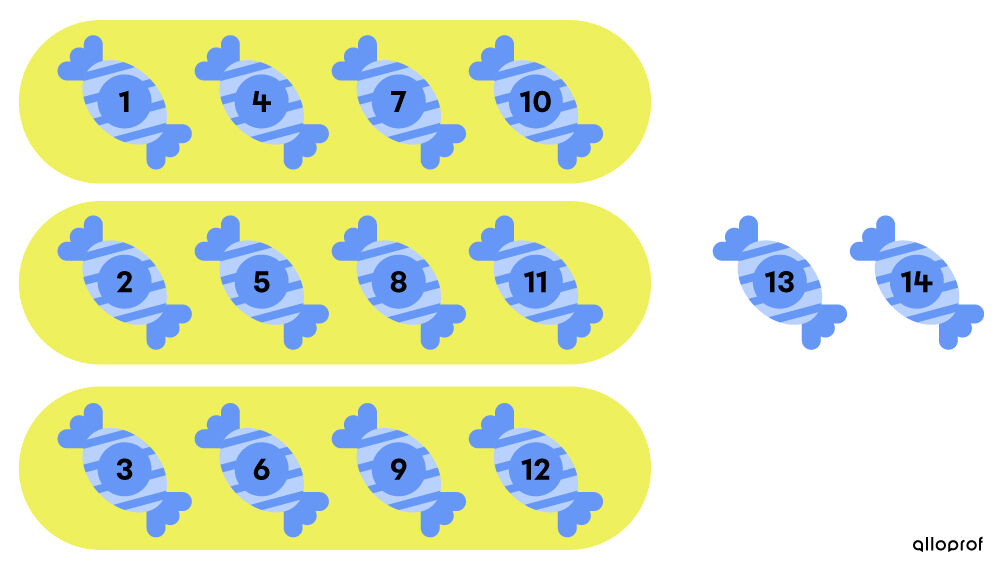
Le reste est la quantité restante après un partage en groupes égaux.
Exemple :
14 ÷ 3 = ?
14 ÷ 3 = 4 reste 2
Pour savoir comment faire une division avec reste à l'aide de la méthode de la division à crochet, je te suggère de consulter la fiche suivante :
N'hésite pas à nous réécrire si tu as d'autres questions! :)
Marilee
Re : Question
Bonjour CrocodileEmpathique6362 !
J'espère sincèrement que le délai ne t'aura causé aucun désagrément.
Une bonne question, mais dans quel contexte utilises-tu telle notion ?
Dans ce cas, considérant aussi mes connaissances limitées, je pense qu'il serait plus opportun de te diriger vers une source de référence sur le sujet, que tu pourras retrouver ici :
À la prochaine, en espérant t'apporter une aide plus substantielle !
Re : Question
Bonjour ElfeLibre1852 !
J'espère sincèrement que le délai ne t'aura causé aucun désagrément.
En complément à l'explication qui t'a été fournie, je tiens à déposer notre fiche sur le sujet :
et de partager mon mot : l'enrichissement des bourgeois devient remarquable et ils contribuent à la société (implication, réaménagement des quais, introduction et diffusion de produits, propriétaires de grandes entreprises, contrôle sur les pouvoirs économiques et politiques, etc.).
https://www.cairn.info/france-au-xviie-siecle--9782130558279-page-397.htm
J'espère que le tout te permet de te donner une vision d'ensemble.
Re : Question
Bonjour RubisSociable7740 !
De quel film en est-il question ?
En tout état de cause, je clarifie que l'intrigue du film est équivalente au déroulement de l'histoire ou l'enchaînement des événements du film.
Quant au jeu des acteurs, ceci fait référence à la performance des acteurs qui jouent dans le film.
J'espère que mon explication te permettra de répondre aux questions maintenant : )
Re : Question
Merci pour ta question!
Essentiellement, le problème se divise en quelques parties. Pour trouver le pH il faut trouver [H+]. On peut trouver [H+] grâce à la formule de la constante d'acidité (Ka) :
$$ K_a = \frac{[H^+][CN^-]}{[HCN]} $$
Légende :
• Ka : constante d'acidité
• [H+] : concentration en ions H+
• [CN-] : concentration en ions CN-
• [HCN] : concentration en HCN
Cependant, utiliser cette formule nécessite de connaitre la concentration en HCN. On peut trouver celle-ci en faisant un simple tableau stoechiométrique, et en établissant que la concentration finale de H+ et CN- est égale à x :
Par conséquent, [HCN] = 0,30 - x, car HCN a une concentration initiale de 0,30, et car x moles de HCN sont utilisées durant la réaction.
Puis, il ne reste qu'à insérer les valeurs dans la formule de Ka et isoler la variable x pour trouver sa valeur, qui correspond à [H+] :
Une fois la valeur de x isolée, il ne reste qu'à trouver la valeur du pH grâce à la formule du pH :
$$ pH = -log[H^+] $$
Légende :
• pH : pH
• [H+] : concentration en ions H+
Cette fiche du site d'Alloprof explique la constante d'acidité :
N'hésite pas si tu as d'autres questions!
Re : Question
Merci pour ta question!
Selon le principe de Le Châtelier, tout système à l'équilibre chimique tend à vouloir changer la position de son équilibre pour pallier tout changement qui vient d'être fait.
Par exemple, baisser la température ambiante aura tendance à favoriser la réaction exothermique dans l'équilibre chimique, car le système veut maintenir une température stable.
Si la réaction exothermique est la réaction directe, la constante d'équilibre aura tendance à augmenter, car il y aura plus de produits. Si la réaction endothermique est la réaction inverse, la constante d'équilibre aura tendance à diminuer, car il y aura plus de réactifs.
Ainsi, le lien entre la température et la constante d'équilibre est expliqué par le principe le Châtelier.
Cette fiche du site d'Alloprof explique le principe de le Châtelier :
N'hésite pas si tu as d'autres questions!