Secondaire 4 • 6m
Rebonjour,
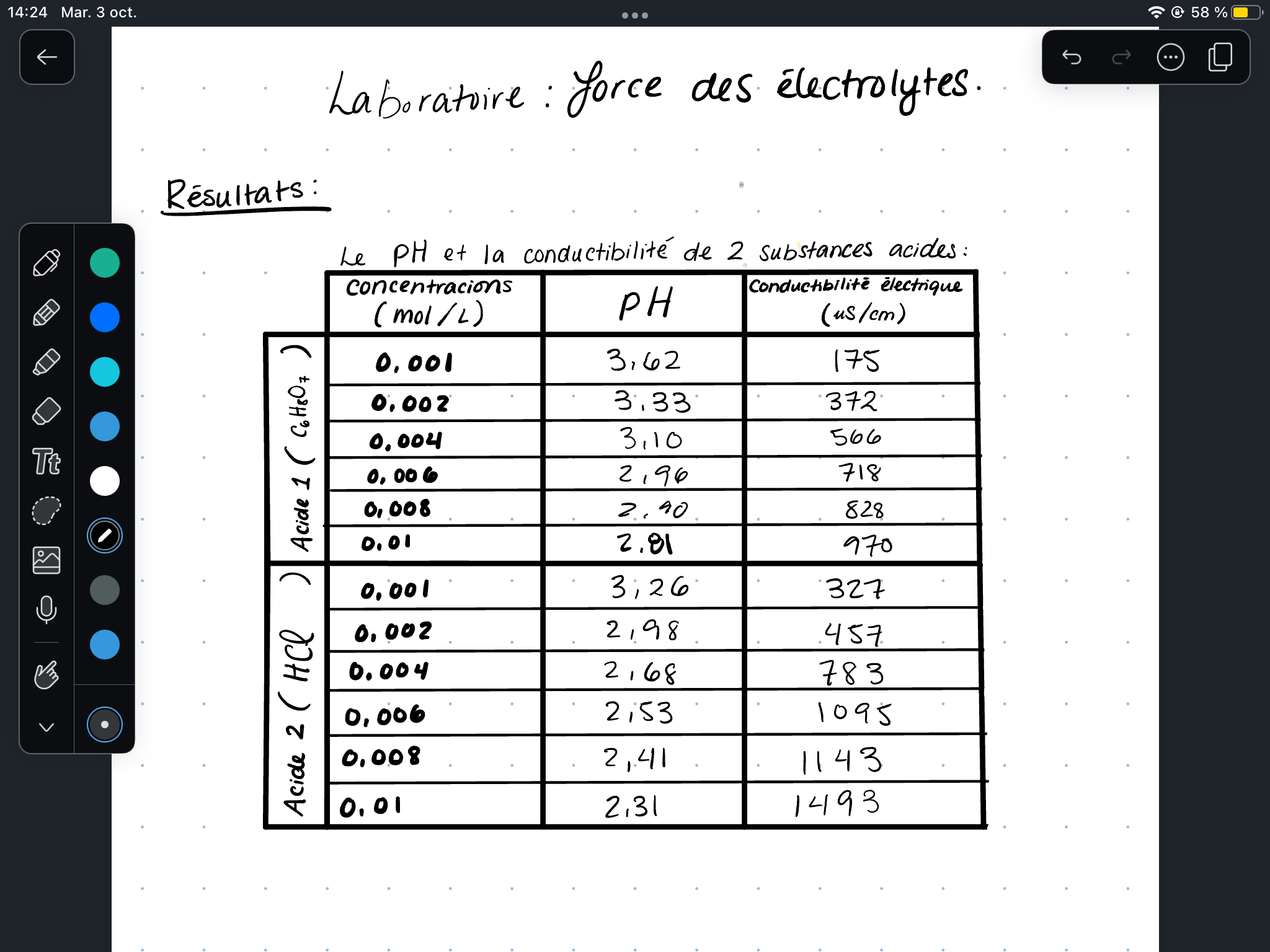
j’avais un labo à faire et ma question d’analyse était de lier le fait que la concentration augmente, le pH diminue et la conductibilité électrique augmente pour ces deux substances acides. Je n’arrive pas à comprendre les rapports entre eux.






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Merci pour ta question!
Tu peux prendre note que cet échange sera archivé à des fins d'amélioration de nos services et de recherche.
Rappelle toi que tous les composés ioniques sont des électrolytes! Plus un électrolyte se dissout et plus il est présent en grandes concentrations, plus la conductibilité est forte.
Dans cette situation, on ajoute un électrolyte fort (l'acide chlorhydrique, HCl) à une solution. Étant un acide, plus sa concentration augmente, plus la solution devient acide (le pH diminue). Aussi, plus sa concentration est grande, le mieux le courant passe, augmentant la conductibilité.
Cette fiche du site d'Alloprof explique la conductibilité électrique des solutions :
N'hésite pas si tu as d'autres questions!
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!