Secondaire 5 • 4m
salut ici je n arrive pas a comprendre c est diagrammes , moi j aurai mis pour le D correspond a un gaz parfait parce que ca repecte la loi de boyle et marriotte PV=k , mais c est faux ... donc svp m aidez ici merci






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Bonjour TitanAlpha,
Merci pour ta question!
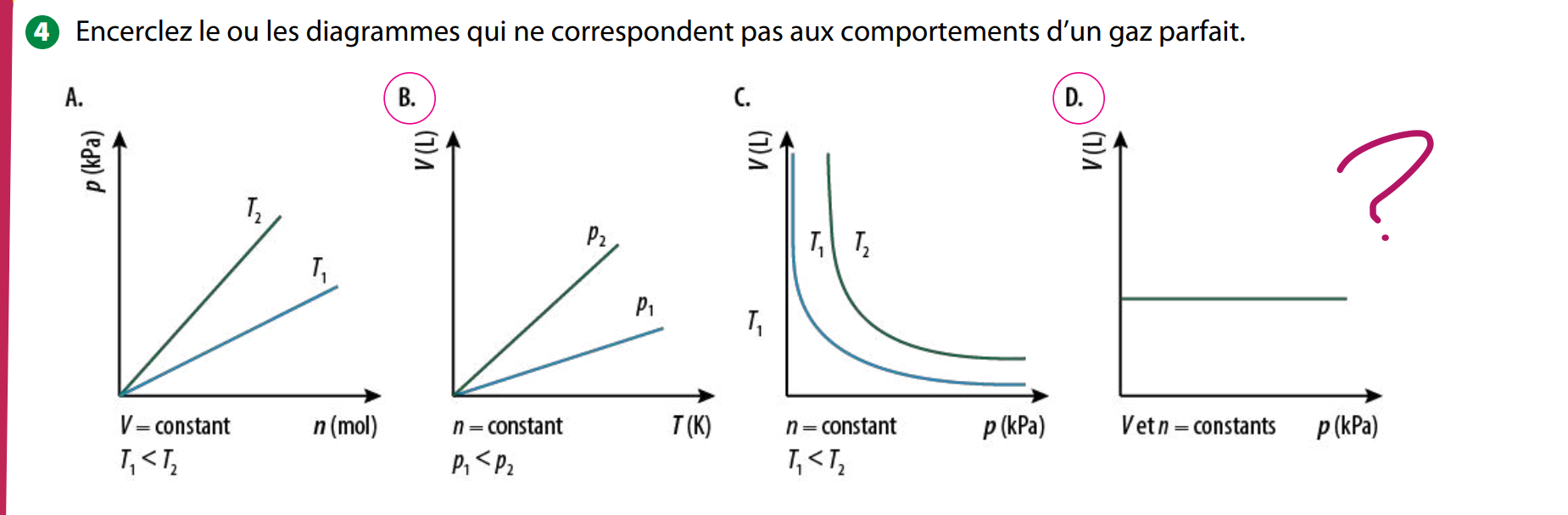
La loi des gaz parfait énonce en effet que PV = nRT, donc à PV = constante si n et T sont constants.
Dans le graphique D, le volume demeure constant. Par conséquent, la pression devrait aussi demeurer constante, puisqu'elle varie proportionnellement au volume. Ce n'est cependant pas le cas dans le graphique D, qui montre que la pression augmente malgré un volume constant. Ainsi, le graphique D représente soit une température qui augmente, soit un gaz qui n'est pas un gaz parfait.
N'hésite pas si tu as encore besoin d'aide:)
Kylan
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!