Bonsoir! Pourriez-vous m'aider avec ceci?
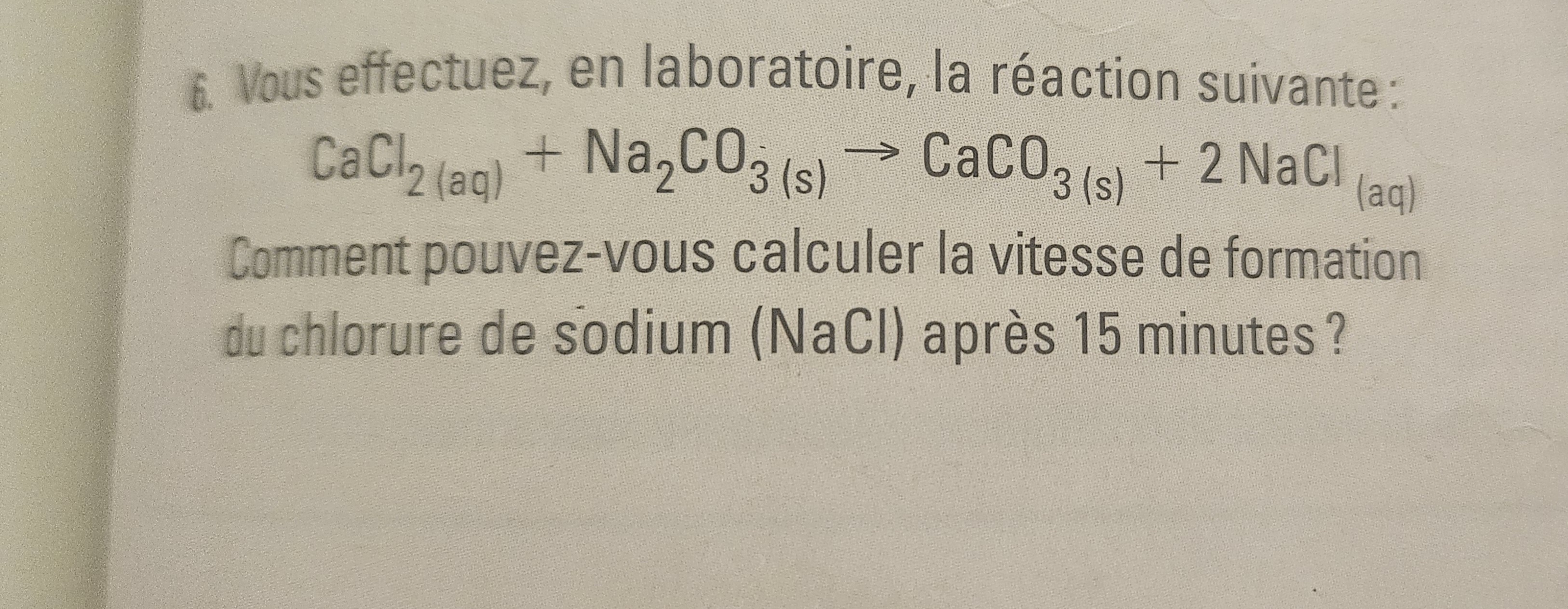
Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.

Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
Merci
Explanation from Alloprof
This Explanation was submitted by a member of the Alloprof team.
Bonjour,
Merci pour ta question!
Comme il est mentionné dans la réponse, il est important de regarder l'état des réactifs et des produits. Dans la situation, la présence de substances à l'état solide dans les réactifs et les produits nous empêche d'utiliser la masse pour calculer la vitesse de formation, ce qui rend la tâche difficile. On pourrait tenter de le faire, mais ce ne serait pas efficace. L'explication de SoleilPhilosophe9110 explique bien pourquoi.
Voici une fiche pour plus d'information :
J'espère t'avoir aidé. N'hésite pas si tu as d'autres questions
Bonjour FraiseAdorable5247,
Imagine que tu fais véritablement cette expérience. Tu as, au départ, une solution aqueuse de CaCl2, qui a l'apparence de l'eau puisque c'est de l'eau salée (le CaCl2 est un sel blanc qui devient transparent lorsque dissout). Tu as aussi une poudre blanche (le Na2CO3). Tu mets la poudre dans l'eau salée.
La réaction se produit.
Un solide blanc (CaCO3) se forme et remplace le solide blanc (Na2CO3) qui était là au départe et un sel différent (NaCl) se retrouve dissout.
Comment mesurer la quantité de NaCl dissous formé? Pas évident!
À la limite, si on peut arrêter la réaction après 15 minutes, on pourrait filtrer le liquide pour se débarrasser du CaCO3 puis faire évaporer l'eau pour recueillir le NaCl, ce qui nous permettrait de le mesurer. Mais si on doit poursuivre l'expérience, il sera difficile de connaître la quantité de NaCl produite.