Populaires
Re : Question
Salut :D
La même question a été posée ici aujourd'hui. Tu peux consulter la réponse donnée :)
N'hésite pas si tu as d'autres questions :D À bientôt :)
Re : Question
Bonjour CitrineIota,
Merci de faire appel à nos services! :)
D'abord, je te fais un petit rappel qu'une conséquence peut être négative ou positive. En ce sens, on cherche à connaître l'impact d'un évènement.
Ensuite, la principale conséquence à cette fusion de dettes est que le Bas-Canada doit maintenant lui aussi participer au remboursement d'une dette qui n'était pas la sienne au départ.
De plus, la population canadienne-française est mécontente puisqu'elle voit une injustice dans la fusion des dettes et le reste des mesures mises en place par l'Acte d'union.
Si tu souhaites en savoir plus sur le sujet, tu peux consulter la fiche suivante :
N'hésite pas à nous réécrire si tu as d'autres questions! :)
Marilee
Re : Question
Bonjour MercureOrange,
Merci de faire appel à nos services! :)
Je te suggère avant tout de bien te préparer en étudiant les notions principales vues au troisième cycle du primaire (5è et 6è année). Être bien préparé permet de diminuer le stress que l'on peut ressentir en vue d'un examen.
Voici deux fiches qui peuvent t'aider dans ta préparation:
N'hésite pas à nous réécrire si tu as d'autres questions et bonne étude! :)
Marilee
Re : Question
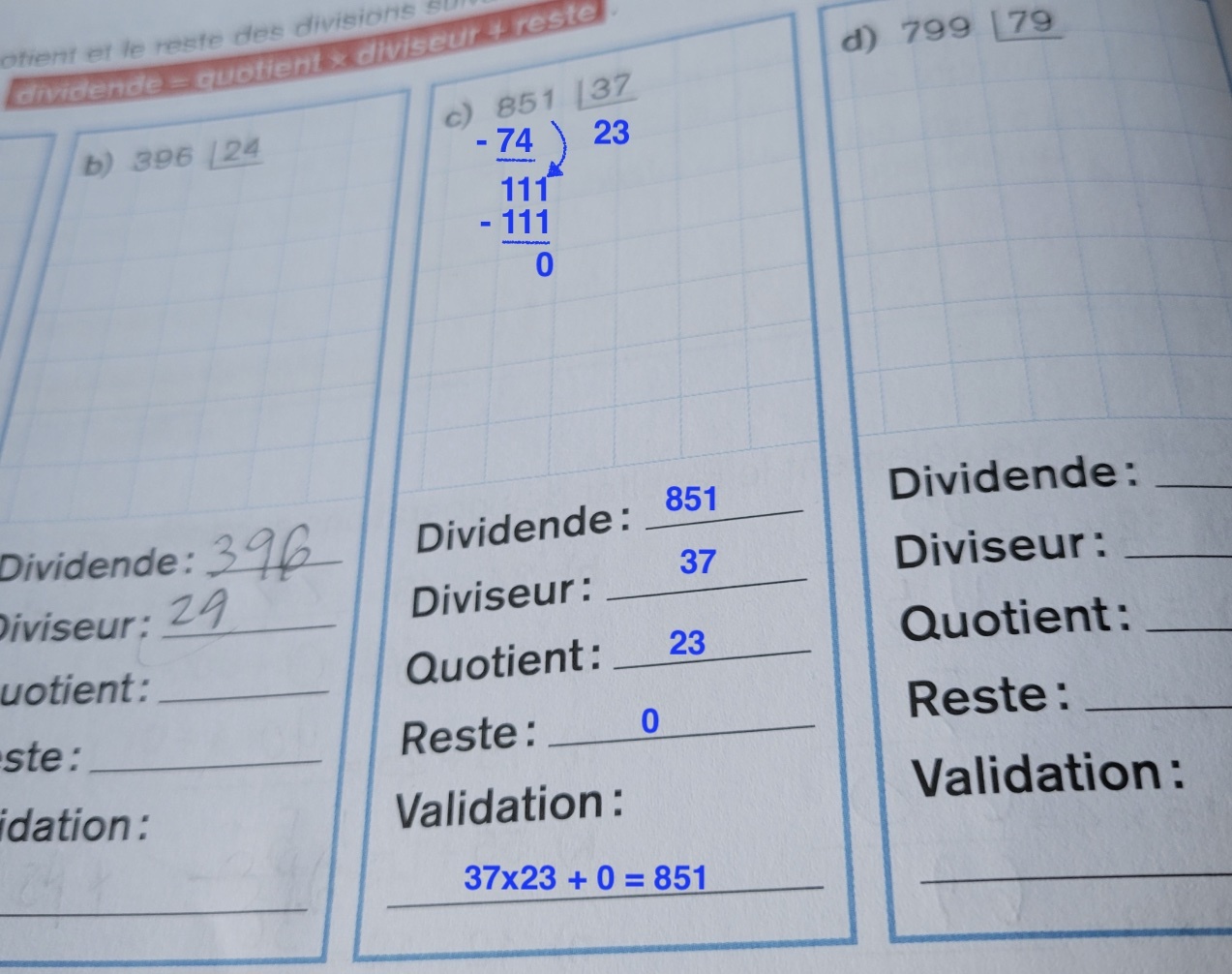
C'est le problème avec l'avènement des calculatrices, on n'a plus besoin de savoir calculer!
Fais moi confiance ce sont des connaissances à entretenir on ne sait jamais quand elles se révèleront utiles.
Je t'aide avec la division du milieu.
Re : Question
☻
Si A'(r) = P- 4r - Pi(r)
alors A''(r) = -4 - pi
Test de la dérivée seconde:
-4-pi < 0 (pour tout r) donc l extrémum est un maximum.
Re : Question
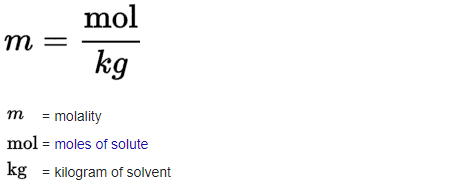
La molalité correspond à la quantité (nombre de moles) de soluté contenue dans 1 000 grammes de solvant. La molalité s'exprime en moles par kilogramme (symbole : mol/kg).
On doit calculer le nombre de moles de saccharose (C12H22011) contenues dans 1kg de solution finale
Le premier 500g de solution initiale contient
m=(60/100)x 1,3g/1mL x 500,0 mL = 390g de saccharose
MC12H22O11=12*12+22+11*16=342g/mol
nC12H22O11 = 390g/MC12H22O11 = 1.14 mol
la solution initiale pèse 1,3g/1mL x 500,0 mL=650g
on lui soustrait la masse de saccharose on obtient la masse d'eau 650g-390g =260g
On mélange 500ml de la solution initiale a 500ml d'eau, le résultat contient 1.14 mol de saccharose
et (260+500=760g) d'eau ou 0.76kg d'eau
M=1.14/0.76=1.5 mol/kg
molalité=1.5M
Re : Question
Salut, je crois que le corrigé a une erreur. J'ai vérifé ma démarche et j'ai même demandé à un prof de chimie. Elle m'a dit qu'elle aussi a trouvé 3,8 mol/kg. Voici comment moi j'ai procédé à ce problème:
1)Calculer la masse de saccharose dans la solution
m=V solution de saccharose x Masse volumique saccharose
m=500mLx1.3g/mL=650g
2) Trouver la quantité de saccharose en moles
n=m/M
n=650g/342,30g/mol= environ 1,90moles
3) Calculer la masse d'eau dans la solution
masse=volume x masse volumique
masse=500mL x 1,0g/mL=500g
4) convertir la masse d'eau en Kg
1kg=1000g
0,5kg=500g
5) Trouver la molalité
Molalité= Nombre de moles de saccharose/masse d'eau (kg)
Molalité=3,8mol/kg
Re : Question
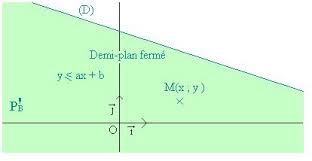
Un demi plan est déterminé par une inéquation du genre
y < ax + b
si c'est une inégalité stricte le demi-plan est ouvert sinon il est fermé (et inclut la droite)
Note les différents types d'inégalité: <,≤, >,≥
Re : Question
Salut!
Un demi-plan fermé inclut la droite frontière (les signes d'inégalité sont donc ≤ ou ≥)
tandis qu'un demi-plan ouvert exclut la droite frontière (> et <) :
J'espère que c'est plus clair pour toi! :)
Re : Question
Bonjour!
Oui! Il y a quelques cas où on peut retrouver un pronom dans un groupe nominal. Voici un exemple :
La robe qu'elle a portée était bleue.
Le groupe du nom qui occupe la fonction de sujet dans cette phrase est «La robe qu'elle a portée». Dans ce groupe du nom, on retrouve deux pronoms : «qu'» et «elle». Il est donc possible d'avoir des pronoms dans un groupe nominal! :D
Si tu as d'autres questions, n'hésite pas à nous réécrire. Nous te répondrons avec plaisir!
Laurie :)