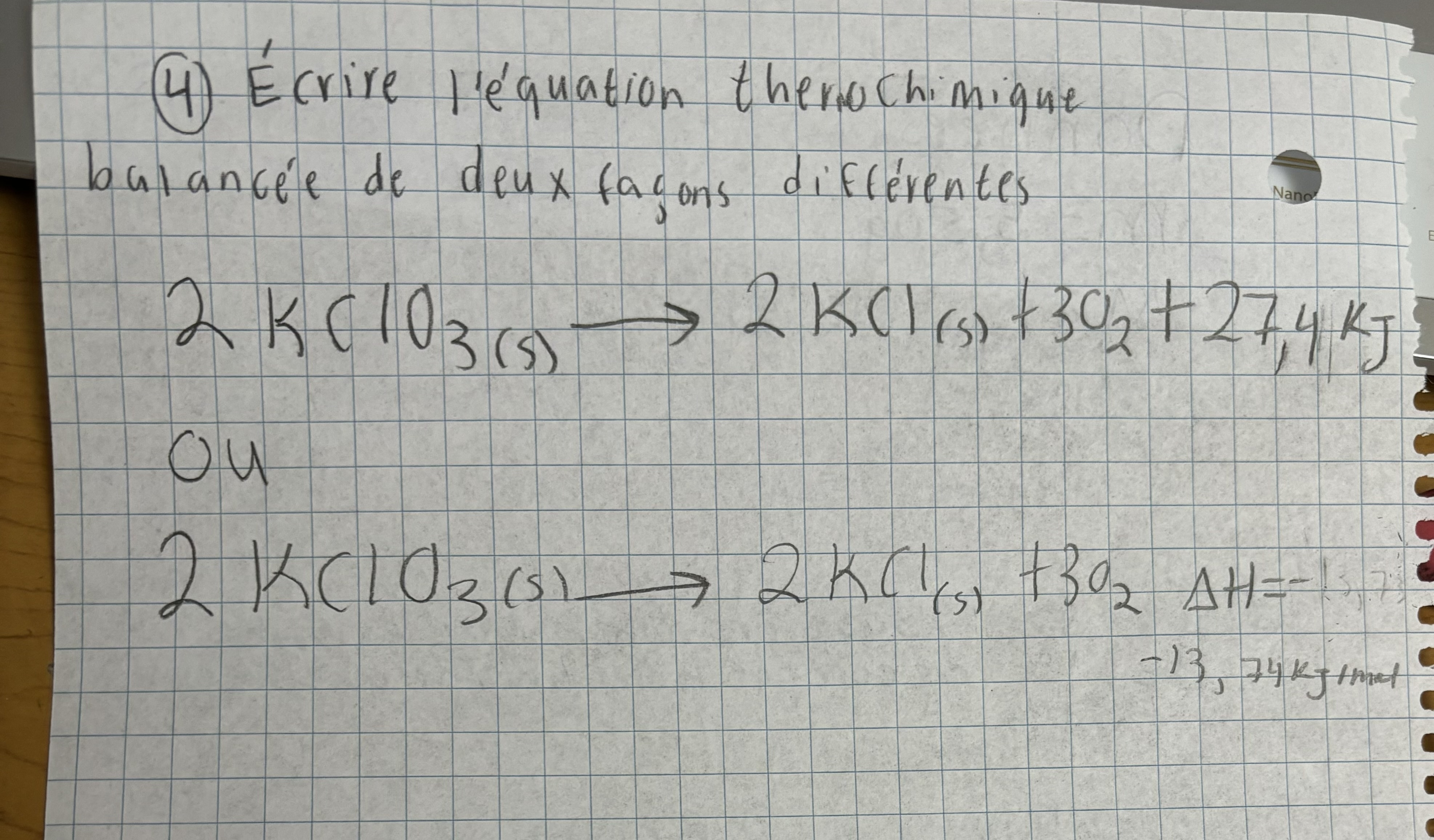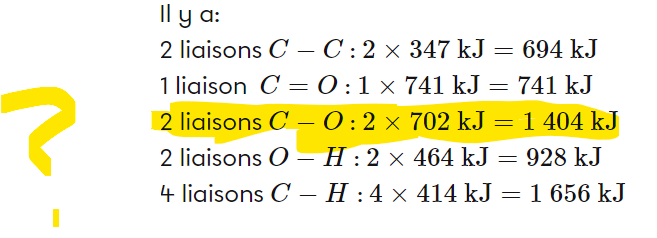Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 2aJ'avais ça a faire en exercice suppementaires (facultatif), mais je nai pa été capable de le faire :!
Vous devez préparer 100,0 g de solution H2SO4 de fraction molaire 0,00500 à partir d’une solution De H2SO4 concentrée à 62,0 %m/m dont la masse volumique est de 1,52 g/mL. Calculer le volume de la solution de H2SO4 concentrée à mesurer ainsi que le volume d’eau à ajouter, en supposant que la masse volumique de l’eau est de 1,00 g/mL. Calculs complets.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, comment résoudre cette question?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour. C'est quoi tout à fait une orbitale, et pourquoi lors de la configuration électronique, 4s viens avant 3d?
-
Vérifiée par Alloprof
Secondaire 5 • 2asi on a 140 ml plus ou moin 3 ml et on veut transformer la donner en L comment on change l’incertitude. aussi si on a 23,0*C plus ou moin 0,1*C d’incertitude et que je change ma température en kelvin comment je change l’incertitude??
-
Vérifiée par Alloprof
Secondaire 5 • 2acomment on calcul l’incertitude relative et absolue dun calcul de mole (PV=nRT)
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, alloprof. Je voulais valider mon raisonnement. On est d accord que Si la dissolution de 2,25 g de sel dans un calorimètre révèle que l’eau a dégagé 2300 J ca veut dire que la dissolution est exothermique, n est-ce pas ? merci alloprof
-
Vérifiée par Alloprof
Secondaire 5 • 2aI am currently having some trouble figuring out what should be over what in a pressure ratio. I’m working on a question at the moment and know how to follow through the question until the last step. In my calculation I got
(2)(P1)/(n1)(293)=(0.5)(P2)/(0.5n1)(253)
which I simplified down to:
253 P1 = 146.5 P2
but now I’m stuck ( don’t know if I should put 146.5P2/253P1 or 253P1/146.5P2) would someone be able to explain why it’s one over the other?
-
Vérifiée par Alloprof
Secondaire 5 • 2aJ'ai posé cette question et on ma répondu de calcluler le H+ du pH 7,2.
j'ai compris cette étape mais je ne suis pas capable de réécrire à la personne qui ma donner cette instruction pour savoir quoi faire par la suite . comment je fais pour répondre à la personne une fois qu'elle m'a donné des instruction ?
J'ai un pot contenant 1200L d'eau.
sont pH est de 7,2.
Nous voulons acidifier le pH pour qu'il soit entre 5 et 6.
j'ai donc 0,20L de solution CH3COOH.
sur la bouteille il est inscrit que la concentration du CH3COOH est de 0,4mol/L et que sa constente d'aciditer (Ka) est de 1,8x exposant 10 à la -5.
Est-ce que je vais réussir à descendre le pH suffisament pour qu'il soit entre 5 et 6 ?
Je ne sait pas quoi faire .
-
Vérifiée par Alloprof
Secondaire 5 • 2aJ'ai un pot contenant 1200L d'eau.
sont pH est de 7,2.
Nous voulons acidifier le pH pour qu'il soit entre 5 et 6.
j'ai donc 0,20L de solution CH3COOH.
sur la bouteille il est inscrit que la concentration du CH3COOH est de 0,4mol/L et que sa constente d'aciditer (Ka) est de 1,8x exposant 10 à la -5.
Est-ce que je vais réussir à descendre le pH suffisament pour qu'il soit entre 5 et 6 ?
Je ne sait pas quoi faire .
-
Vérifiée par Alloprof
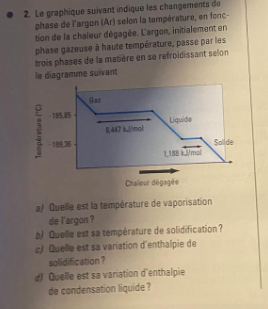
Secondaire 5 • 2aBonjour! Dans cette exercice, la réponse aux c) et d) sont -1188 kJ/mol et -6447 kJ/mol, mais pourquoi est ce qu'ils ont enlevé les virgules? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 2aLe séchage des vêtements sur une corde à linge est-il endo ou exo?
-
Vérifiée par Alloprof
Secondaire 5 • 2aLequel des énonces suivants est faux
A. 100 g d'eau à 22,4 °C possèdent une plus grande énergie thermique que 100g d'eau à 16,2 °C.
B. 100 g d'eau à 18,5 °C et 1,00 g d'eau à la même température possèdent la même agitation thermique.
C. L'énergie thermique emmagasinée dans 100g d'eau à 18,5 °C est égale à celle emmagasinée dans 1,00 g d'eau à la même température.
D. Si on mélange 100g d'eau à 21,0 °C avec 100g d'eau à 36,4 °C, l'eau à 36,4 °C va transférer une partie de son énergie thermique à l'eau à 21,0 °C
Moi je pense que c’est le b car plus la quantité d'eau est grande, plus il y a d'agitation thermique . Donc, 100 g d'eau à 18,5 °C a plus d'agitation thermique que 1,00 g d'eau à la même température. N’est-ce pas ? Merci alloprof
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je voulais valider mon raisonnement la question dit
Le chlorate de potassium (KCIO,), une substance utilisée en industrie comme agent désinfectant, se décompose thermiquement selon l'équation non balancée suivante.
KCl03(s) → KCl + 02
La décomposition thermique de 5,50 g de chlorate de potassium (KCIO,) dégage 673,2 ] d'énergie.
Écrivez de deux façons différentes l'équation thermochimique de cette décomposition.
VOICI MES DÉMARCHESEst-ce que mon raisonnement est bien fait merci alloprof
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je n’arrive pas à convertir la concentration de la solution concentrée en concentration molaire. Comment dois-je procédé?
-
Vérifiée par Alloprof
Secondaire 5 • 2aJe n’arrive pas à trouver la concentration initiale. Je ne sais pas comment utiliser le % m/m et la m/V donnée?
-
Vérifiée par Alloprof
Secondaire 5 • 2aJe comprends pas pourquoi c’est ca la réponse?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
Pourrais-je avoir de l'aide pour cette exercice de chimie :
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour dois-je utiliser la capacité thermique massique de l'eau si je ne trouve pas celle de l'hydroxyde de sodium mais qu'il est en solution?
-
Vérifiée par Alloprof
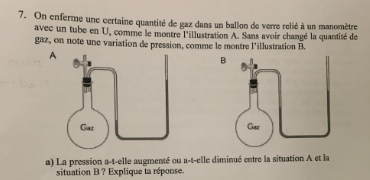
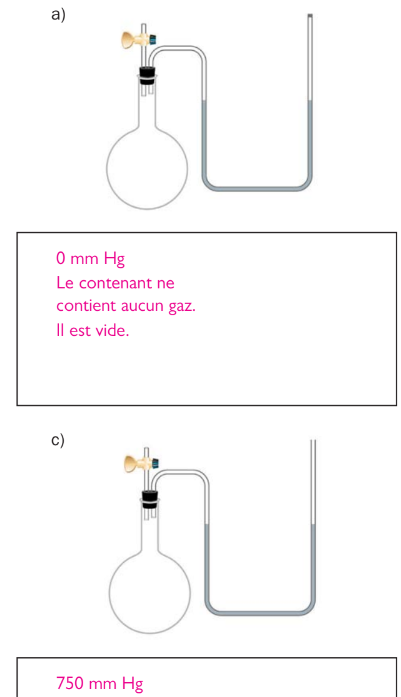
Secondaire 5 • 2aBonjour,
J'ai des problèmes à répondre à cette question en rapport avec la pression :J'espère une reponse au plus vite!
-
Vérifiée par Alloprof
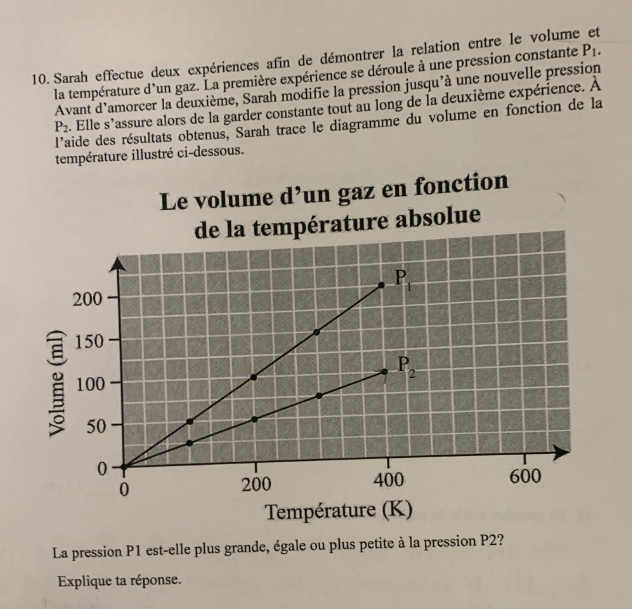
Secondaire 5 • 2aBonjour, je ne comprend pas ce problème. (#10)
-
Vérifiée par Alloprof
Secondaire 3 • 2aBonjour! J'espère que je ne vous dérange pas, mais j'ai une question pour vous:Comment est-ce que je le fais? Je ne comprends pas...
MERCIII!!!
-
Vérifiée par Alloprof
Secondaire 5 • 2abonjour, ça voulait dire quoi titrage en chimie. Une technique consiste à melanger deux solutiosn?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je ne comprends Pas quand arrondir. La réponse que j'ai eu était de 1,87 et je l ai arrondi mais la réponse dans le corrige est de 1.9 . Je ne comprends pas pourquoi merci.
-
Vérifiée par Alloprof
Secondaire 5 • 2aSalut!
J'ai une petite question concernant le diagramme énergétique. Il est indiqué dans la majorité des exercices de mon cahier que l'enthalpie des réactifs commence par 0. Mais dans quel cas l'enthalpie des réactifs ne commence pas par 0?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, j’avais un labo à faire en chimie. Il fallait qu’on trouve la chaleur molaire de deux neutralisation. Une ou la base et l’acide sont aqueux et une ou l’acide est aqueux, mais la base est solide.
Je voulais savoir, autre que le fait que le système a peu être permis les échanges de chaleur, car il était mal isolé. Quel autre source d’erreur peut expliquer que la température expérimentale est plus petite que la température théorique.
Je voulais savoir, quel effet ont des gouttes d’acides qui serait restées dans le calorimètre avant que je fasse mon expérience. Est-ce que puisque lorsque de l’eau est placée dans de l’acide ça fait une réaction exothermique, ça aurait pu augmenter la température finale. Si non je ne comprends pas l’effet que ça a.
Je voulais savoir, quelles sont deux sources d’erreurs qui pourrait expliquer que la température expérimentale est plus grande que la température théorique. Est-ce que ça pourrait avoir un lien avec la quantité de base en gramme que j’ai utilisé?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, pourriez-vous m'aider sur cette question s'il vous plaît ? :
Dans 5g d'eau, combien y a-t-il d'atomes d'hydrogène ?
Je vous remercie d'avance !
Très belle soirée... 😊
-
Vérifiée par Alloprof
Secondaire 5 • 2aPour ma question sur les énergies de liaisons pour le diazote,je parle de cela.On peut voir 2 N avec une liaison double et je ne comprend pas pourquoi.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je comprends pas pourquoi ici c'est marqué que 2 liasions de C-O est 2x702 pusique l'énergie de liaison de C-O c'est 358?Merci de m'aider!
-
Vérifiée par Alloprof
Secondaire 5 • 2aJe ne comprend la différence entre ces deux énoncés.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,je voudrais savoir,pour les énergies de liaisons,le N² peut être formé d'une liaison simple,d'une liaison double et d'une liaison triple.Dans quel cas la liaison simple et double arrive et quand savoir lorsqu'il faut les utiliser pour trouver la bonne énergie?