Secondaire 5 • 1a
Bonsoir, est-ce que dans ce problème j'ai besoin de trouver la masse molaire de H2SO3 ou je peux faire une produit-croise de g/mol? Si oui, comment est-ce que je sais quand il faut faire quoi? Merci!
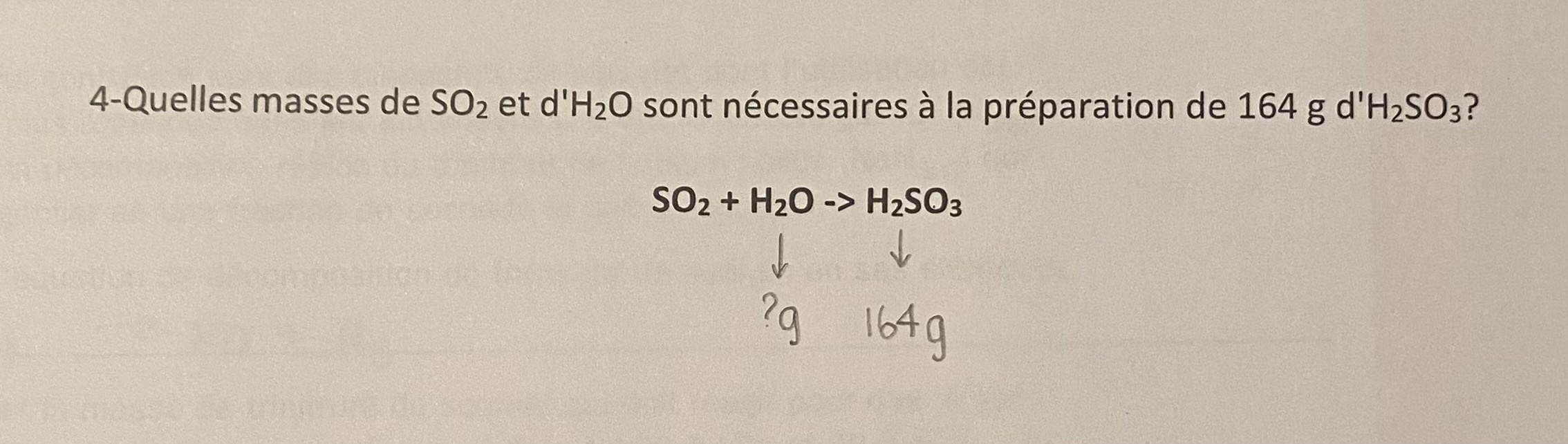






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Salut AluminiumTranquille5113,
Merci pour ta question!
Pour pouvoir faire des proportions, donc de la stœchiométrie, on doit absolument avoir des moles! Ainsi, ici tu devras transformer 164 g de H₂SO₃ en moles à l'aide de la masse molaire. Ensuite, tu pourras trouver le nombre de grammes de SO₂ pour le nombre de moles que tu as trouvé et le nombre de grammes de H₂O pour le nombre de moles que tu as trouvé avec la masse molaire des molécules respectives.
En espérant t'avoir aidé,
Laurie
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!