Bonjour!
J'ai un exercice sur la loi de Hess qui m'a vraiment mélangé; la-voici:
Dans l'exercice suivant, jai été capable de déterminer l'équation globale (l'équation de la vaporisation du benzène en vert).
Déjà, comme vous pouvez le voir dans ma démarche en haut, même après avoir additioné et soustrait les substances de chaque côté, je n'arrive pas à éliminer comme par ex le CO2 et le H2O. Je ne comprends pas comment je peux jouer avec les coefficients stoéchiométriques, alors que mon équation globale est vraiment simple avec juste 1 mol comme coefficient et pas d'autres éléments.
Une autre chose, c'est que notre enseignant en classe nous a mentionné qu'il est inutile d'utiliser la deuxième équation lors des calculs. Mais, pourquoi on n'en a pas besoin? Puis, si il y a des cas similaires qui se présentent dans des futurs exercices, comment est-ce que je peux le savoir?
Merci, j'ai vraiment besoin de le comprendre :D

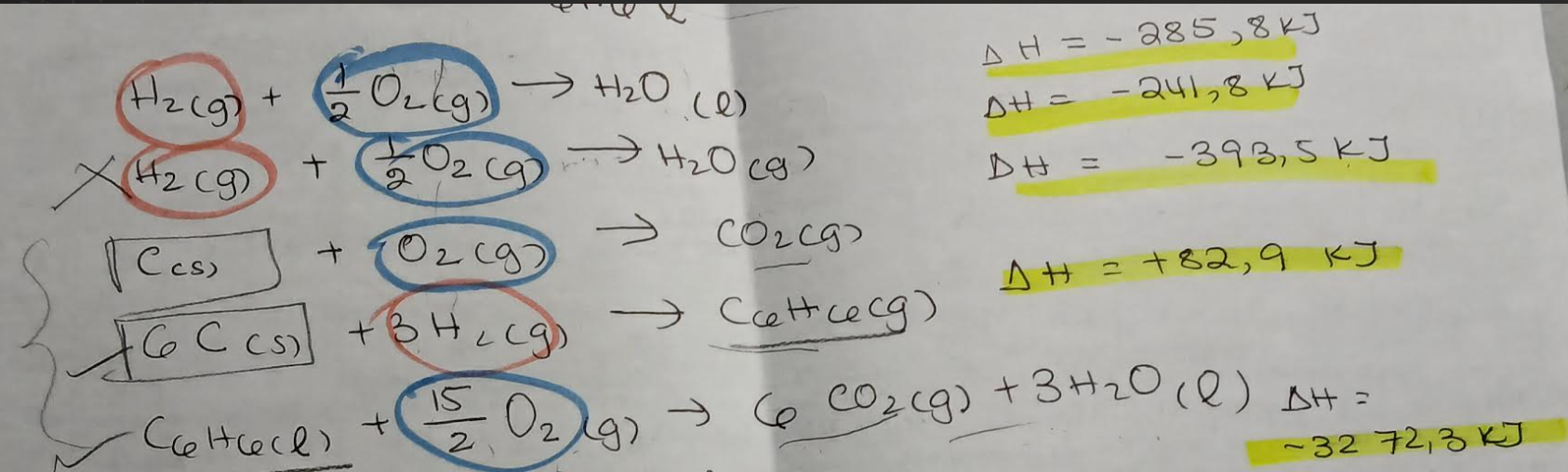






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Bonjour OpaleDynamique,
Merci pour ta question!
Ton enseignant t'as dit de ne pas tenir compte de la deuxième équation probablement par souci de simplicité, puisqu'il s'agit simplement de l'évaporation de l'eau (en fait, dans ce cas, ce serait probablement plus H2O (l) -> H2O (g)). Pour les exercices à venir, tu devrais toujours être prévenu si tu dois ignorer une des équations. Sinon, tu peux prendre pour acquis qu'elles sont toutes importantes.
Pour faire disparaitre le CO2 et le H2O, tu dois utiliser des équations en réactions intermédiaires qui ont ces molécules du côté opposé. Par exemple, dans l'équation de départ (celle qui contient le C6H6 liquide comme réactif), le CO2 est un produit. Tu dois donc utiliser une réaction intermédiaire qui comporte le CO2 comme réactif et la balancer pour que celui-ci disparaisse.
Pour plus d'exemples sur la loi de Hess:
N'hésite pas si tu as besoin d'aide:)
Kylan
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!