Re-bonjour!
J'avais quelques questions sur le chapitre de chaleur de réaction et la loi de hess; les-voici:
1) Je ne comprends absolument pas c'est quoi la capacité calorifique d'un calorimètre. Il y a certains facteurs qui me bloquent et donc, voici l'extrait du cahier que je ne comprends pas:
De un, pourquoi est-ce qu'on parle de calculer la chaleur dégagée ou absorbée par le calorimètre, alors qu'on utilise toujours l'eau comme outil pour mesure la chaleur impliquée dans une réaction, à l'aide de la formule Q=mcΔT?
Aussi, je ne comprends pas pourquoi (surligné en jaune), il est nécessaire de tenir en compte la masse et la capacité thermique massique d'autres matériaux constituant la bombe calorimétrique, alors que la réaction se passe dans un milieu contenant de l'eau?
En quoi est-ce que la capacité calorifique est différent de la capacité thermique massique?
2) Est-ce qu'il faut absolument toujours avoir l'équation globale avant de manipuler les équations partielles?
Je veux donne deux exemples rapides dans lesquels je ne suis pas sûre...
Si la question me dit uniquement de déterminer l'équation thermique globale de chaque réaction, alors est-ce qu'en additionnant les substances entre eux, ce que j'aurais, ça serait l'équation globale? Car ici, je n'ai pas de référances sur le nombre de moles à multipiler en suivant une équation de départ par ex.
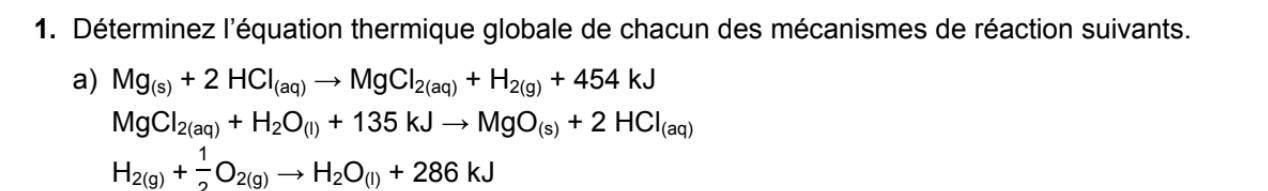
Alors que, si j'ai un exercice comme ceci, est-ce que je dois m'imposer une équation globale pour me guider dans les calculs avec les équations partielles?
Merci énormément pour apporter ces clarifications :D








Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Bonjour OpaleDynamique,
Merci pour ta question!
La capacité calorifique est un ancien terme pour désigner la capacité thermique. Il s'agit en fait de la chaleur (c).
Le calorimètre est justement un appareil servant à mesurer les échanges de chaleur, qui contient de l'eau. Il s'agit donc du même principe de calcul que les calculs de la chaleur impliquée dans une réaction impliquant l'eau, comme ceux auxquels tu es habitué.
Il faut tenir compte de la masse de toutes les composantes du calorimètre puisque chacune de ces composantes va absorber une partie de la chaleur. Elles jouent donc toutes un rôle dans la réaction.
L'équation globale est l'équation finale balancée qui correspond aux réactifs initiaux et aux produits finaux après tout le mécanisme réactionnel. C'est l'équation "finale" de la loi de Hess.
Pour plus d'informations sur la loi de Hess:
N'hésite pas si tu as encore besoin d'aide:)
Kylan
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!