Secondaire 4 • 7m
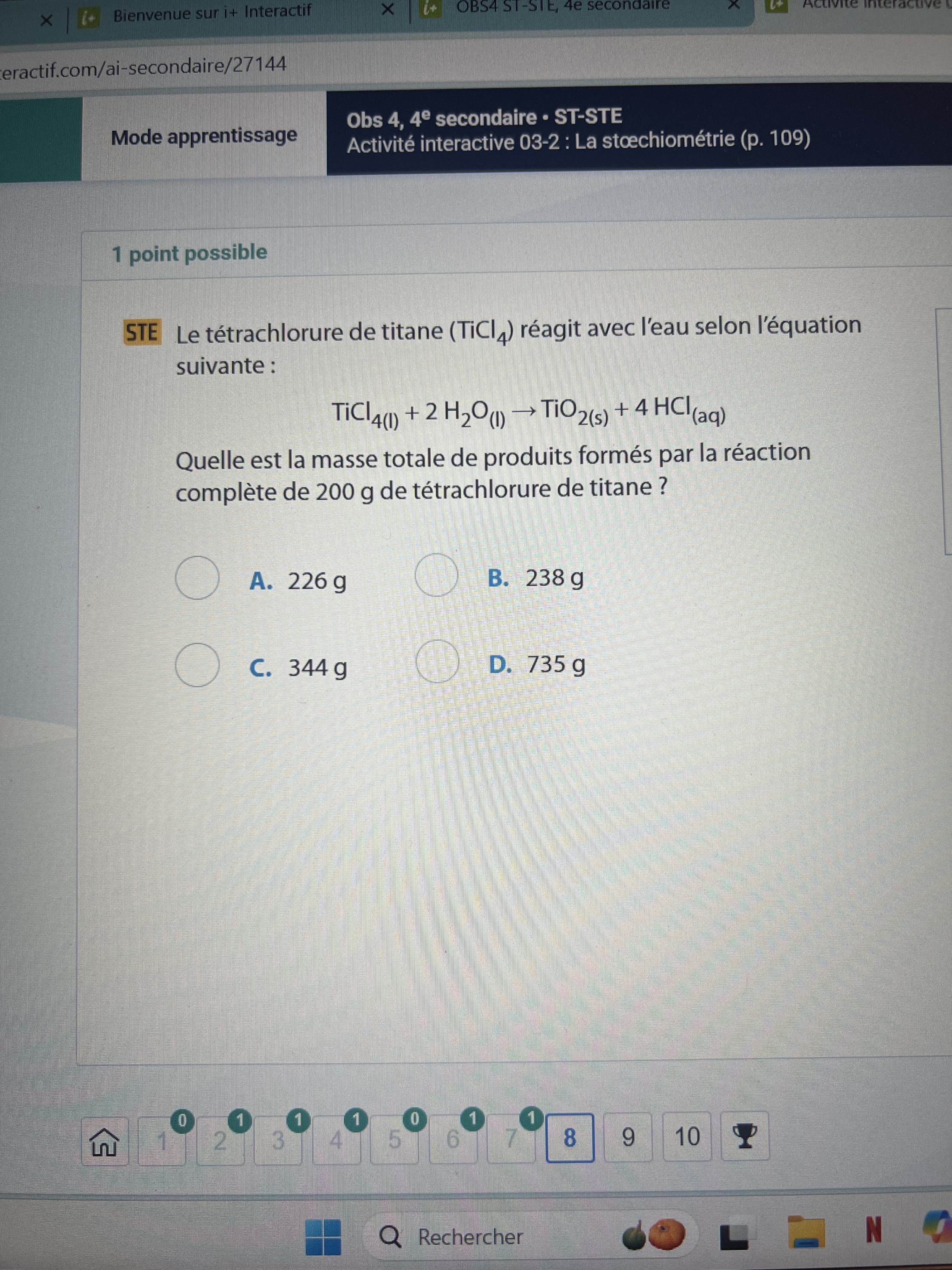
Bonjour, j’ai essayé de faire cet exercice ,mais je ne comprends pas pourquoi je ne doit pas juste additionner la masse des réactifs pour avoir la réponse est ce que quelqu’un peut m’explique svp?






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Bonjour,
Merci pour ta question!
En fait, c'est parce que le rapport des coefficients stœchiométriques n'est pas proportionnel au rapport entre les masses. Il est proportionnel au rapport entre les nombres de moles.
Ainsi, pour trouver la réponse, tu dois transformer la masse de 200 g de tétrachlorure de titane en moles. Ensuite, tu utilises les rapports stœchiométriques pour déterminer le nombre de moles de produits formés. Enfin, il te reste à retransformer le nombre de moles en grammes.
Voici une fiche qui pourrait t'aider :
N'hésite pas si tu as d'autres questions!
Zachary T. :)
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!