Secondaire 5 • 4a
Salut!
Je suis tombé sur une question difficile :
Balancer la stœchiométrie de l'équation de la réaction suivante. Ensuite, trouver la vitesse (en mol/s) de la réaction si 20 mL de HCl ont réagit pour former les produits en 30s. La réaction se déroule à température et pression constante (25°C et 101,3 kPa).
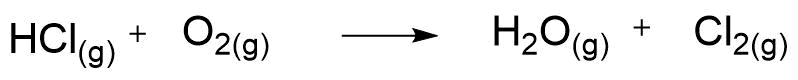






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Salut!
La première étape pour résoudre ton problème est de trouver les coefficients stœchiométriques. Si tu n'es pas habitué avec ce concept, je t'invite à visiter cette page :
Plusieurs méthodes sont possibles. Pour ma part, je préfère commencer avec les molécules ayant le plus d'atomes, car elles risquent d'être celles avec les plus petits coefficients. Pour ta part, il s'agit du dichlorure (Cl2) et de l'eau (H2O). Si ton produit final contient deux atomes de chlore, alors tes réactifs doivent aussi avoir deux atomes de chlore. Il faut faire la même démarche pour chaque molécule et chaque atome et on obtient la réponse suivante :
Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
Pour la suite de ta question, il faut mélanger les concepts des gaz parfaits et celui de la vitesse de réaction. Tout d'abord, il faut trouver la quantité de réactif en mole. Si tu n'es pas familier avec la loi des gaz parfaits, je t'invite à consulter cette page web :
Il faut convertir la température en température absolue (Kelvin) et le volume de mL en L :
Avec ces informations tu pourras calculer le nombre de moles et en faisant attention aux unités, tu devrais obtenir la réponse suivante :
Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
À partir de cette réponse, il te suffit de diviser la quantité en mole par le temps pour donner la valeur de vitesse comme ceci :
Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
J'espère que tu trouvera cette réponse utile!
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!