Populaires
Re : Question
Bonjour Requintimide, mis à part les images de tes problèmes qui sont un peu floues, ce qui m'étonne c'est qu'on ne voit aucun développement (ton travail sur chaque problème) de ta part.
Cela me donne l'impression que tu comptes un peu trop sur une aide extérieure pour faire tes problèmes.
Réfléchir et commencer le problème font partie de l'apprentissage de la matière.
Commence et on t'aidera à continuer/compléter.
Re : Question
Salut :D
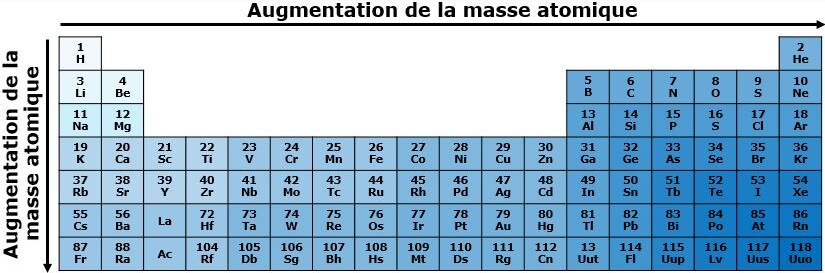
Les atomes sont plus lourds en fonction de leur nombre de protons et d'électrons. Plus il y en a, plus l'atome sera lourd.
Dans une même période, la masse atomique augmente de gauche à droite dans le tableau périodique. Puisque le nombre de particules de l'atome augmente de gauche à droite avec le numéro atomique, la masse atomique augmente également dans la même direction, car un plus grand nombre de particules implique nécessairement une plus grande masse.
Dans une même famille, la masse atomique augmente de haut en bas dans le tableau périodique. Comme le numéro atomique augmente de haut en bas, un plus grand nombre de protons se retrouvent dans les atomes situés dans le bas du tableau périodique, ce qui implique nécessairement une plus grande masse atomique.
N'hésite pas si tu as d'autres questions :)
Re : Question
Salut :D
101,3 kPa correspond à 1 atm, c'est un taux, alors on peut l'inscrire comme une fraction (101,3kPa/1 atm).
Aussi, pour pouvoir éliminer les unités atm présentes dans ton 3,65 atm, il faut mettre l'unité atm au dénominateur.
J'espère que ça répond à ta question :) N'hésite pas s'il y a quoi que ce soit :D À bientôt :)
Re : Question
En fait, je crois qu'il faudrait écrire :
Le tableau et/ou la statue de cire vont se vendre à prix d'or — très bientôt.
J'espère que j'aide!
Re : Question
Bonjour DiamantAlpha2583!
Pour compléter les explications de mon collègue Anthony, je crois que tu confonds peut-être les 2 façons d'exprimer
L’énergie libérée (dans une réaction exothermique) et l’énergie absorbée (dans une réaction endothermique).
Regarde bien l’exemple ci-dessous tiré de la fiche sur les réactions exothermiques et endothermiques:
Comme tu le remarques ici, l'énergie libérée se retrouve bien dans les produits (+ 95,4 kJ).
Il existe une autre façon aussi d'exprimer cette libération d'énergie en utilisant l'expression ΔH:
Dans cette autre façon d'exprimer l'énergie libérée, l'énergie ne se retrouve pas dans les produits au niveau de l'équation chimique. Le ΔH s'écrit un peu plus en retrait à droite de l'équation chimique et représente la variation d'énergie subit par le système lors de la réaction chimique. Dans l'exemple le ΔH égale -95,4 kJ, ce qui veut dire que le système a perdu 95,4 kJ d'énergie. Énergie qui a été libérée d'où l'expression "exothermique".
Dans le cas d'une réaction endothermique:
Ainsi en exprimant l'énergie gagnée avec le ΔH:
J'espère que ces précisions t'aideront à mieux comprendre ces concepts!
Merci d'avoir utilisé notre service d'entraide!
Bien à toi,
ThonLucide8631
Re : Question
Bonsoir à toi !
J'espère sincèrement que le délai ne t'aura causé aucun désagrément.
Je crois que le lien suivant sera en mesure de t'aider :
Le cas contraire, réécris-nous avec entrain !
Re : Question
Salut :D
Comme ma collègue Marilee a répondu, tu passeras les autres matières en secondaire 4, puis, si tu coules le cours d'été, tu resteras en maths de secondaire 3. Si tu le passes, tu iras également en maths secondaire 4.
N'hésite pas si tu as d'autres questions :)
Re : Question
Salut :)
Si tu as une proposition concernant un jeu, écris-la à l'équipe de service technique ici.
Merci :D À ta prochaine question :)
Re : Question
Salut DiamantAlpha2583,
Merci pour ta question!
Généralement, lorsqu'il y a une réaction exothermique, de l'énergie est dégagée et la milieu de réaction se réchauffe. L'énergie est du côté des produits, elle est donc produite et elle réchauffe le milieu. L'enthalpie de réaction est négative pour les réactions exothermiques.
Pour une réaction exothermique, c'est l'inverse, l'énergie est absorbée par la réaction. Le milieu de réaction se refroidit et l'énergie est du côté des réactifs. L'enthalpie de réaction est positive pour les réactions endothermiques.
J'espère que ça t'aide et n'hésite pas à nous réécrire !
Anthony B.
Re : Question
Bonjour ElfArtistique,
Merci pour ta question :)
Le mécanisme d'engrenage est plus avantageux puisqu'il est plus précis que des roues de frictions.
Par exemple dans ton horloge tu as de l'engrenage. Celui-ci sera beaucoup plus précis pour tes heures qu'une roue de friction.
Avantage :
- Ne permet aucun glissement entre les roues grâce aux dents.
- Peut être de très petite taille, ce qui permet de transmettre des mouvements dans de petits espaces avec une grande précision.
Voici une fiche :
J'espère avoir aidée !
N'hésite pas si tu as d'autres questions :D
BrachiosaureTimide314