Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 2aJe ne sais pas comment trouver les équations partielles, je crois qu’il y a un tableau et on y aura accès pour l’examen, mais je ne l’ai pas donc je ne comprends pas comment résoudre le problème.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, pour appliquer la loi de Hess dans un problème, je ne trouve pas le tableau pour faire les équations partielles, j’aurais besoin d’aide svp!
-
Vérifiée par Alloprof
Secondaire 2 • 2ac’est quoi la différence entre les alcalines et les alcalins
-
Vérifiée par Alloprof
Postsecondaire • 2aQu'est-ce qu'un Coulomb? Une force, une énergie..?
-
Vérifiée par Alloprof
Secondaire 5 • 2aSalut à nouveau, je voulais simplement dire qu'il demandait combien de particules étaient dans la question précédente que j'avais envoyée. La réponse serait environ 1,2044E24 particules qui est égale à 2 mol, mais je vous remercie quand même d'avoir confirmé ma réponse, c'est très apprécié.
La question était ; Combien de particules d'un gaz sont présentes dans un volume correspondant à deux fois le volume molaire à une température de 220 Ket une pression de 206,6 kPa?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, dans le corrigé pour cette question, ils ont noté la pression partielle du l'eau comme étant 2,64 kPa mais je ne sais pas comment y arriver.
Un mélange de NO2 et de NO est recueilli par déplacement d'eau, à une température de 22°C et une pression de 99,3 kPa, quelle est la pression partielle du NO2?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, voici une autre question que je ne comprend pas comment résoudre: Une bonbonne de 1000ml est entreposé dans une pièce dont la température est de 22,0ºC. Le gaz qu’elle contient exerce une pression de 880 mmHg. Quelle quantité de gaz contient cette bonbonne?
Je ne comprend pas comment trouver la pression (KPA) pour faire mon calcul avec le 880 mmHg
-
Vérifiée par Alloprof
Secondaire 5 • 2aVoici un autre problème de chimie : Une enseigne lumineuse contient du néon gazeux qui lui confère des teintes de rouge. quelle est la quantité de gaz présente à l’intérieur des tubes de cette enseigne, alors que la température est de -8ºC en hiver?( Le volume total des tubes est de 34,5 L et leur pression interne est de 0,2kPa) .
Je ne sais pas c’est quoi que je dois chercher… la masse, la masse volumique, ….?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour voici un problème en chimie que je dois résoudre, mais je ne comprend pas comment savoir si c’est un gaz parfait ou non… comment je suis sensée le savoir? Voici la question : Frédéric reçois un échantillon comportant exactement 0,30 mol de gaz dans un ballon de 2.0L . Afin de déterminer si ce gaz se comporte comme un gaz parfaits elle effectue différente mesure. Elle note ainsi une pression de 245 kPA et une température de 23,5ºC. Quelle est sa conclusion?
-
Vérifiée par Alloprof
Secondaire 5 • 2aSalut à nouveau, je voulais juste confirmer si quelqu'un pourrait vérifier si ma réponse est correcte, sinon, j'aimerais savoir comment obtenir la réponse correcte.
Réponse: 2 mol
Question ; Combien de particules d'un gaz sont présentes dans un volume correspondant à deux fois le volume molaire à une température de 220 Ket une pression de 206,6 kPa?
-
Vérifiée par Alloprof
Secondaire 4 • 2aBonjour,
Je me demandais comment on peut former un acide suivant la formule H+ avec un non-métal ou un ion poly atomique. Ce que je comprends pas c’est le fait que H+ fait un lien covalent, alors comment le diviser en ion H+ et ion qqch- s’il fait pas un lien ionique?
Merci en avance pour votre explication :)!
-
Vérifiée par Alloprof
Primaire 3 • 2aSES quand en va apprendre la chimi
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour j’ai poser la question hier cependant je n’ai pas réussi à le faire du coup si quelqu’un pourrait m’envoyer une explication de cette dernière sa serait très apprécié merci d’avance et voici la question;
Un réservoir métallique contient 8,00 moles à TPN. En augmentant la température de 20,0°C, quelle quantité de gaz doit-on ajouter afin de tripler al pression initiale?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
Je me demandais comment pouvait-on reconnaître une augmentation/diminution de la pression dans une équation chimique si la température reste constante et dont les coefficients stoechiométriques sont respectés?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, voici une question dans mon lab de chimie: Combien de litre(s) théoriquement faut-il pour soulever votre enseignant de 158 lb aux conditions de la classe?
je ne la comprend pas, pouvez-vous m'aider?
Les conditions de la classe sont de 101,9Kpa et 22,7oC
-
Vérifiée par Alloprof
Postsecondaire • 2aBonsoir,
J'aurais besoin d'aide avec cette question : la demi-vie de l'uranium 238 est de 4,5 milliards d'années et est indépendante de la concentration initiale. Combien de temps prendra la désintégration de 10% des atomes d'un échantillon d'uranium 238? S'il y avait 1,5 x 10^18 atomes d'uranium 238 dans un échantillon lorsque l'univers s'est formé il y a 13,8 milliards d'années, combien en reste-il aujourd'hui?
t1/2 = 4,5 x 10^9
n = 1
10% de désintégration signifie qu'il reste 90% d'uranium.
t1/2 = In2/k --> 4,5 x 10^9 / In 2 = k = à peu près 1,44 x 10^-10 s^-1
[A]o = 1,5 x 10^18 --> t = 13,8 x 10^9s
[A]t = ?
In ([A]t/[A]0) = -kt
[A]t = [A]0 e^-kt = 1,5 x 10^18 e^-1,44x10^-10s^-1 x 13,8 x 10^9s = à peu près 2,06 x 10^17 atomes d'uranium, mais la bonne réponse est d'à peu près 1,8 x 10^17 atomes d'uranium.
Pour la première question, j'aimerais savoir si c'est 4,5 + (4,5/2) = 6,8 x 10^8 ans, si oui, pourquoi?
Merci et bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Postsecondaire • 2aBonsoir,
J'aurais besoin d'aide avec le #1.Voici mes démarches :Les réponses sont respectivement 57kPa et 100kPa.
Merci et bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Primaire 5 • 2aPuise savoir quelle phénomène explique la tombée de la neige. svp des explications chimiques mais assez simples à comprendre .
Merci et à bientôt
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, pour mon lab de chimie, j'ai besoin de savoir comment une mongolfière s'élève dans les airs. Il faut l'expliquer avec un principe physique.
-
Vérifiée par Alloprof
Secondaire 4 • 2aBonjour!
J'ai deux questions:
1) En fait, je ne comprends pas pourquoi des liaisons covalentes vont former des ions polyatomiques?
Par exemple, dans le cas de l'ammoniac (NH₄), je ne comprends paspourquoi ce composé est ionique. Si j'ai bien compris le principe de la liaison covalente, un atome d'azote a 3 atomes célibatires dans sa couche périphérique. Donc, il lui suffit de partager 3 électrons avec 3 atomes d'Hydrogène (H). Donc un composé qui respecte la règle de l'octet aura la formule chimique NH3.D'où vient donc le quatrième atome d'Hydrogène et pourquoi et comment est-ce que l'ammoniac devient un composé ionique?2) Dans le cas d'une liaison ionique, pourquoi est-ce que c'est incorrect d'écrireNa+Cl-comme formule chimique? Ce sontdeux ions, non?
Merci ;)
-
Vérifiée par Alloprof
Secondaire 5 • 2aje sais pas si il manque une information mais la question est celle ci. ; Un réservoir métallique contient 8,00 moles à TPN. En augmentant la température de 20,0°C, quelle quantité de gaz doit-on ajouter afin de tripler la pression initiale?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
J'ai une question pour mon labo :
Est-ce que tous les gaz se comporteraient de la même façon dans les mêmes conditions expérimentales?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
j'ai une question en chimie concernant la théorie cinétique des gaz ,est-ce-que l'espace entre 2 molecules differente mais ayant la meme pression et donc la meme quantité d'atome,est la meme dans chaque bouteille?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
Dans la loi des gaz parfaits, ça veut dire quoi “Les particules de gaz n’ont aucune interaction entre elles”? N’est-ce pas contradictoire avec le deuxième point qui mentionne que les gaz rebondissent sans perdre de l’énergie, ce qui signifie qu’ils interagissent entre eux?
Merci, bonne soirée!
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
J'ai une question à propos du la rédaction du rapport de laboratoire, précisément à la partie de l'hypothèse. Si on fait un laboratoire et qu'on prédit ce qui va être la réponse et qu'on dit pourquoi on pense cela, on a besoin de donner un exemple? Par exemple, je fais un laboratoire sur le but de déterminer la formule empirique et le pourcentage massique de l'Oxyde de magnésium, et moi je dis que 👇👇👇Est-ce que j'ai besoin de prouver avec des calculs?
-
Vérifiée par Alloprof
Secondaire 4 • 2aBonsoir, je ne comprends pas comment savoir la force d'une électrolyte (forte ou faible) à partir de sa formule chimique, serait-il possible de m'expliquer? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je ne comprends rien de ce numéro réaction et tout je ne sais pas comment les différencier et comment trouver la réponse à ces questions. Pourriez-vous m’aider svp?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour!
Je n'arrive pas à comprendre cette question! J'aimerais avoir des explications. Merci!
Un volume de gaz d’une masse molaire de 62,0g/mol s’effuse à travers une paroi poreuse pendant 2h56min. Combien prendra de temps un volume identique de NO2 (g)?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
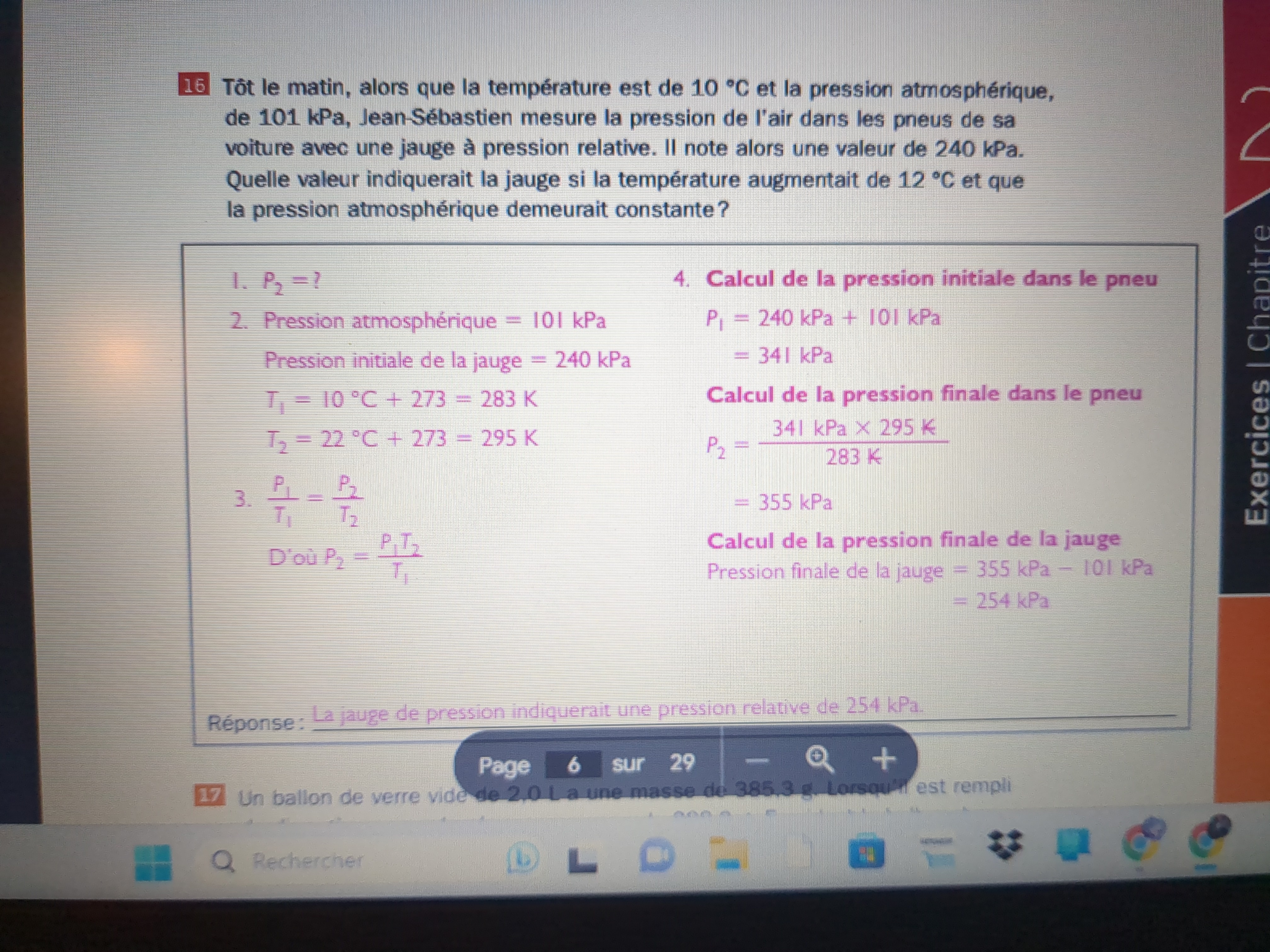
Je ne comprends pas pourquoi on a additionner la pression atmosphérique avec la valeur de 240 kPa et pourquoi à la fin on l'a soustrait. Merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
Je ne comprends pas pourquoi on a additionner 101,3 KPa. Même si j'ai noté l'explication, je ne comprends toujours pas.
Merci