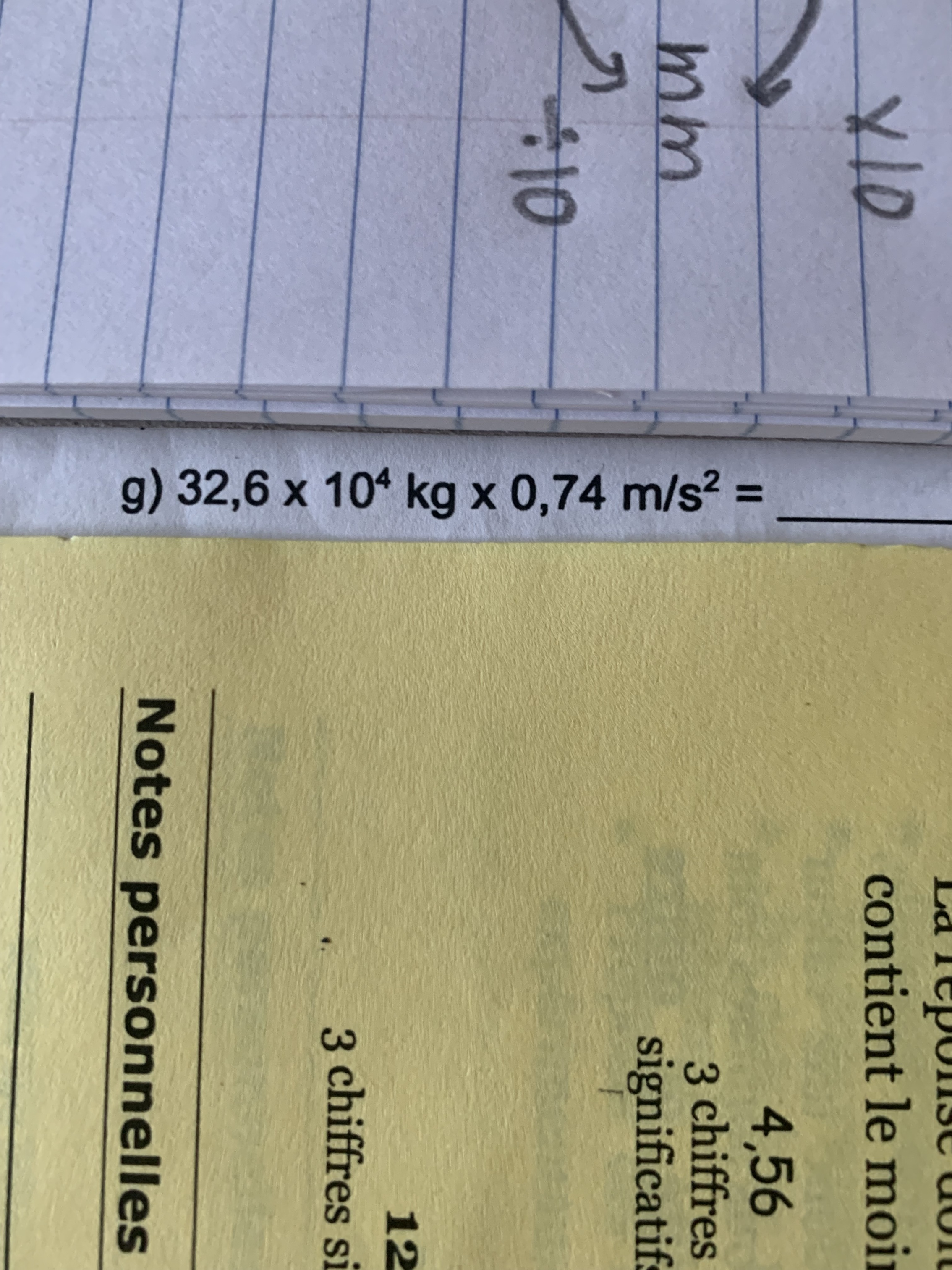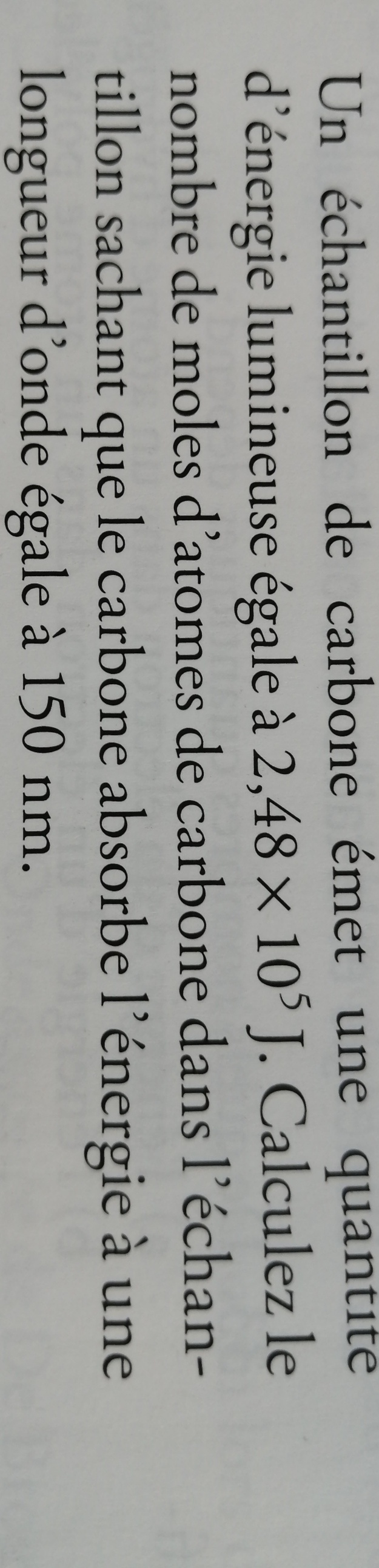Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 2aPouvez-vous m'aider à écrire ces équations balancées, merci
-La dissociation électrolytique du CH3COOH
-La décomposition du d'hydroxyde de baryum en ses éléments
-La décomposition du CH3COOH en ses elementsm equation balancee
-la décomposition du SULFATE de sodium en ses element
-
Vérifiée par Alloprof
Secondaire 5 • 2aComment trouver le volume du vinaigre et masse du bicarbonate de soude dans un labo de sac ziploc? si on a la masse volumique du vinaigre qui est de 0,84 mol/L et on a trouver le volume du sac. ou doit-on utiliser la stœchiométrie dans ce labo?
-
Vérifiée par Alloprof
Postsecondaire • 2aJ'ai tenté ce numéro plusieur fois mais je ne l'ai jaimais bon je ne sais pas ce qu'il faut faire. J'aurais besoin d'aide svp.
-
Vérifiée par Alloprof
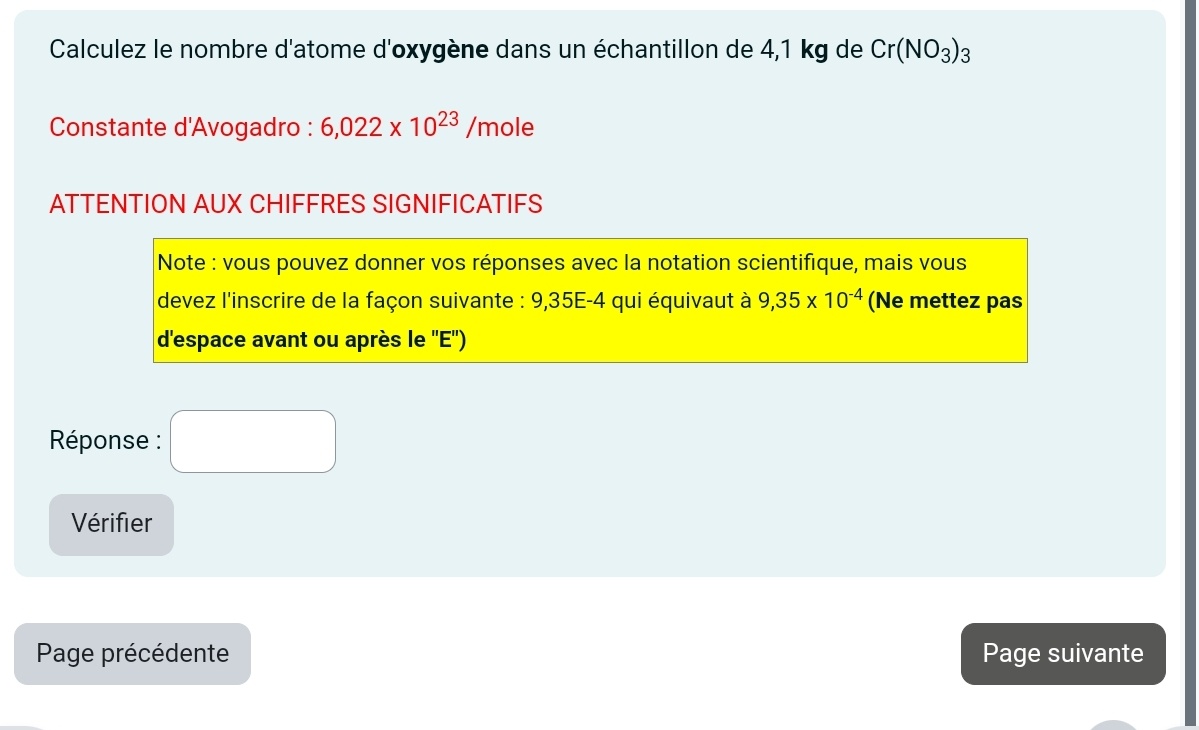
Secondaire 5 • 2aBonjour je ne comprends pas ce numero il faut tenir compte des chiffres significatifs et des unités merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour je ne comprends pas ce numero il faut tenir compte des chiffres significatifs et des unités merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je me demandais si je peux avoir de l’aide avec une question. "Quelle serait la molarité d’une solution faite par le mélange de 100 mL d’eau à 70 mL d’une solution de NaOH, 5 mol/L?"
Merci et bonne journée!
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je me demandais si je pourrais avoir de l’aide avec le numéro 2. Merci, bonne journée!
-
Vérifiée par Alloprof
Postsecondaire • 2aBonsoir,
J'aurais besoin d'aide avec cette question : calculer la molalité d'une solution obtenue en mélangeant 500,0 mL d'une solution aqueuse de saccharose (C12H22011) de pourcentage massique égale à 60% et de masse volumique 1,3g/mL avec 500,0 mL d'eau de masse volumique égale à 1,0g/mL.
Voici mes démarches :
m = ?mol/?kg = 1,139351446 mol / 0,5 kg = à peu près 2,27 mol/kg
60g/100g x 1,3g/1mL x 500,0 mL = 390g
nC12H22O11 = 390g/MC12H22O11 = 1,139351446 mol
msolvant(kg) = (500,0 ml H2O x 1,00 g/mL) / 1000mL = 0,5 kg
Pouvez vous m'expliquer pourquoi je n'arrive pas à la bonne réponse qui est de 1,5 M.
Bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Postsecondaire • 2aBonsoir,
J'aurais besoin d'aide avec cette question : une solution aqueuse d'acétone (CH3COCH3) de molalité égale à 1,29 mol/kg a une masse volumique égale à 0,990 g/mL. Calculer sa concentration molaire volumique.
Voici mes démarches :
C = n/V = 1,29 mol (déjà donné dans le problème) / (1,29 mol / 1000g, qui vient du 1 kg) / (990g/L, qui vient du 0,990g/mL)
0,990 g : 1 mL
1L : 1000 mL
(1000 mL x 0,990g) / 1 mL = 990g/L
Le tout me donne à peu près 1,27 M. Par contre, la bonne réponse est de 1,19 M. Pouvez-vous m'expliquer pourquoi je n'arrive pas à la bonne réponse?
Merci et bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, pouvez vous m'aider à résoudre cet exercice svp, merci bcp!!!
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, pouvez vous m'aider à résoudre cet exercice svp, merci.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour! Pourruez vous m'aider avec cette question svp?? Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour voilà deux numéros:
32,6 x 10 à la 4 kg x 0,74 m/s2 et 6,3 m x 2,4 s-2
Il faut tenir compte des chiffres significatifs et dès unités! Je ne comprends vraiment pas comment je peux mettre kg en m/s2 et m en s-2
-
Vérifiée par Alloprof
Secondaire 5 • 2aJe mesure un le diamètre d'un objet et j'obtiens 1,80cm, donc 3 chiffres significatifs. Si je veux le rayon, je dois diviser par 2 donc j'obtiens 0,90cm, ce qui correspond à 2 chiffres significatifs. Pour en avoir 3, il faudrait ajouter une décimale. Or, ma règle (qui monte à coup de 0,1cm) n'est pas assez précise pour ajouter cette décimale. Dois-je garder ma réponse ou la changer?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir alloprof! Pouvez vous m'aider à résoudre ce type de questions svp? C'est des exercices de rappels de l'année dernière et je ne me souviens plus des formules. Merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aPourquoi est-ce la quantité de solide ne modifie pas l'état d'équilibre? Je ne comprends pas le lien avec sa concentration étant 100% lui-même. Pourtant il doit y avoir une quantité de solide autant qu'une quantité de gaz pour pouvoir faire la réaction.
-
Vérifiée par Alloprof
Secondaire 5 • 2aComment on ecris 1,254 +/- 0,00031 g/mL en respectant les règles d’écriture pour l’incertitude?
-
Vérifiée par Alloprof
Postsecondaire • 2abonjour,
Quelqu'un pourrait m'expliquer car je ne comprends pas ce que je suis censée faire.
Bonne journée!
-
Vérifiée par Alloprof
Postsecondaire • 2aBonjour Alloprof! Je n'arrive vraiment pas à trouver la réponse à cette question? Pouvez vous m'aider ? Je ne sais pas quel est le lien entre l'énergie et le nombre de mol
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
J'ai besoin d'aide en chimie
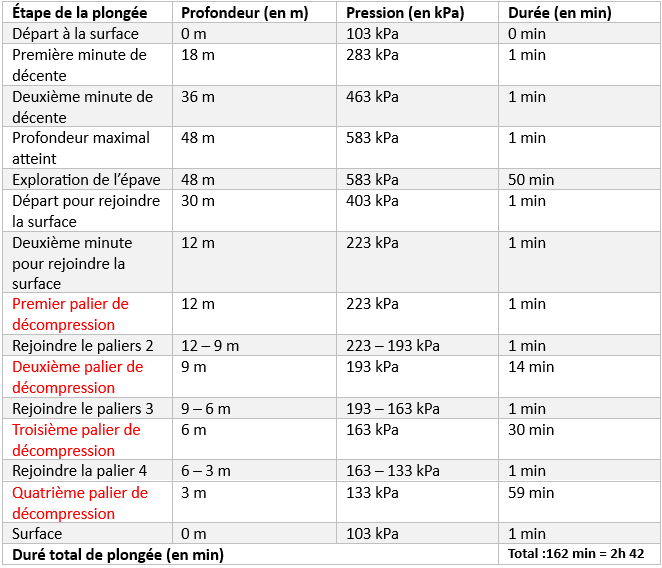
Le problème à résoudre : Calculez la quantité d’air nécessaire pour la durée totale de plongée du plongeur choisi. Comparez votre réponse avec la quantité d’air que votre plongeur consommerait à la surface pour cette même période de temps.
Les donnés :Mon tableau :Ma question :
Je dois faire quoi pour trouver la quantité de mol durant la plongée et la quantité de mol durant un moment fictif si il était en surface pour ensuite faire une comparaison entre les deux résultat.
Ma théorie :
Je pense que le plongeur demandera plus d'air sous l'eau que en surface.
Svp aidé moi, à l'aide...
PS : Dire la raison du refus de ma question serai apprécier.
Merci
-
Vérifiée par Alloprof
Secondaire 4 • 2aBonsoir, pouvez-vous svp m'aider a répondre a cette question
On mélange 50,0 mL d’une solution de sulfate de sodium, Na2SO4(aq), à 0,20 mol/L avec 80,0 mL d’une solution d’acétate de plomb (II), Pb(CH3COO)2(aq), à 0,10 mol/L. Un précipité blanc se forme. Identifie-le et calcule la masse maximale qu’on pourra recueillir.
Merci et bonne soirée!
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
j’ai essayé de faire un problème de chimie par moi-même j’ai été me corrigé et j’ai compris la moitié de celui-ci. Je ne comprend pas comment qu’on trouve le 350 mm?
merci à vous!
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
j’ai faite un problème de chimie et avec le corriger, j’ai pus avoir la bonne réponse. Cependant, je ne comprend pas la réponse.
la question est : un manomètre indique une pression de 3,65 atm. Quelle est la pression de ce gaz en KPa?
j’ai dû faire 3,65 atm x 101,3 KPa / 1 atm
mais je ne comprend pas pourquoi je divise par 1 atm?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
j’aimerais savoir comment qu’on peux savoir si les particules sont plus lourde que d’autres ?
Merci à vous
-
Vérifiée par Alloprof
Postsecondaire • 2aEquilibrez la r´eaction chimique suivante, en milieu basique, ´ CrO− 4 (aq) + C5H10O4(aq) → Cr3+(aq) + HCO− 3 (aq)
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour Alloprof! Pouvez vous m'expliquer comment résoudre ce numéro, car je n'y arrive vraiment pas?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour Alloprof! Pouvez vous m'expliquer comment résoudre ce numéro, car je n'y arrive vraiment pas?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour Alloprof! Pouvez vous m'aider à résoudre ce problème s'il vous plaît? Je n'y arrive pas.
-
Vérifiée par Alloprof
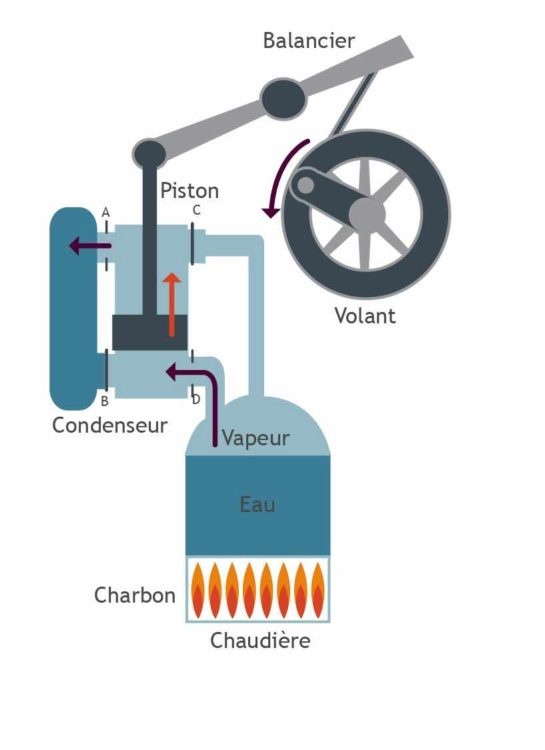
Postsecondaire • 2aBonjour j'ai sue dans les livres que le dix-neuvième siècle à été un siècle de révolution industrielle et surtout grâce à la fameuse machine à vapeur de James Watt.
Mais ma question est pourquoi c'est de la vapeur d'eau qui pousse le piston dans le cylindre à la place du monoxyde de carbone produit par la combustion du charbon de bois , charbon minier ou du bois ? Quelle avantages avait t'ils à utiliser la vapeur d'eau à la place des gas de combustion carbone pour pousser un piston dans un cylindre ?
-
Vérifiée par Alloprof
Secondaire 3 • 2aBonjour, pouvez-vous m'aider a répondre a cette question.Merci et bonne journée!