Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 2aSalut!
Je voulais savoir si jai bein resolue mon prob
-
Vérifiée par Alloprof
Secondaire 5 • 2aRe-bonsoir,
MrRamzi Z ?Tout d'abord, merci de m'avoir répondu aussi vite. Merci.
Ensuite, si je vous envoie un exemple d'exercice qui me pose problème en photo, est ce que cela serait mieux ? Comme cela, par exemple.Encore une fois, merci beaucoup de votre aide. Bonne soirée.
TortueDynamique1064
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
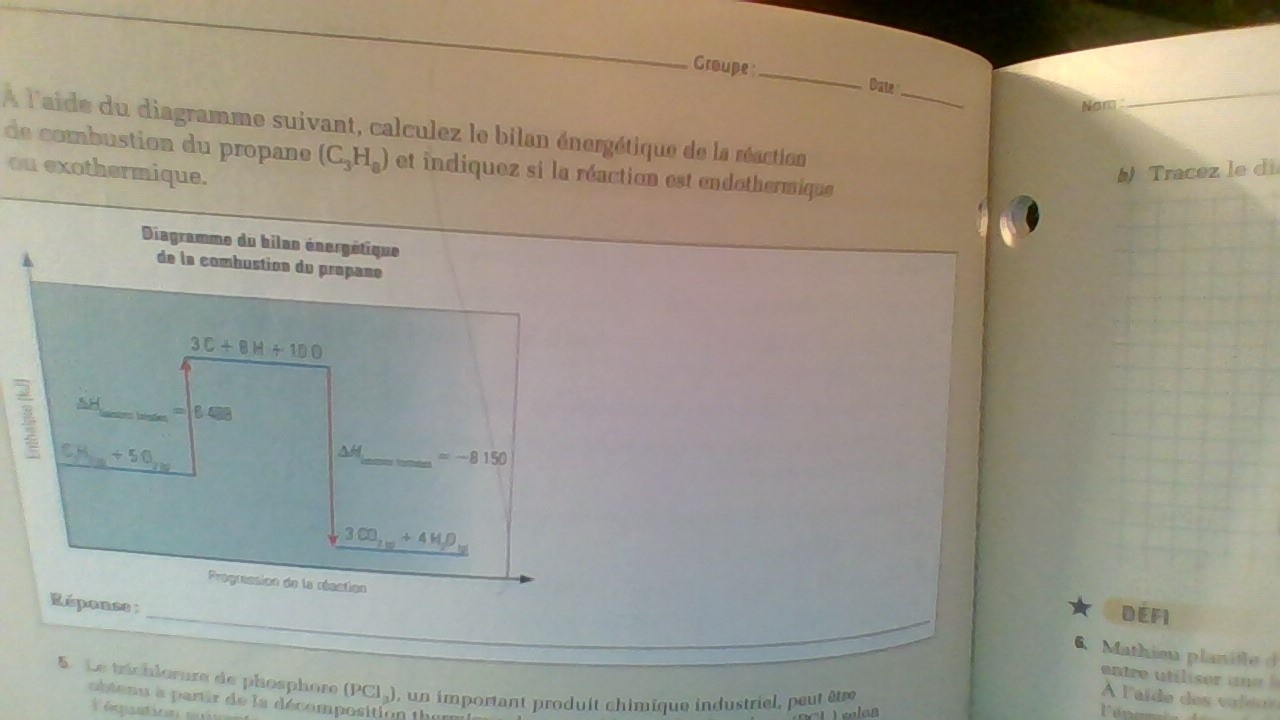
je vous écris parce que j'ai de la difficulté à faire mes exercices portant sur l'enthalpie (toute sorte d'enthalpie) ainsi que la vitesse de réaction. Mon examen de fin d'année est mercredi prochain, et je ne me sens pas très prête, à vrai dire. J'ai déjà consultée vos fiches, et essayée vos exercices en ligne, mais en vain. Mon problème est vraiment au niveau de quand vient le temps de faire mes exercices. Là, cela bloque complètement. J'ai l'intention d'appeler ce dimanche, afin de demander l'aide d'un professeur, mais si vous pouvez déjà commencer à m'aider, cela serait encore mieux.
Merci d'avance,
Une élève de secondaire 5 en détresse de chimie.
P.S.: Nous travaillons avec le manuel, et les cahiers de révision Quantum, autant en chimie qu'en physique.
-
Vérifiée par Alloprof
Secondaire 3 • 2aJe ne comprends pas comment faire ceci! un contenant helium continent 15 l d’helium sous press ion a environ 2 250kpa a 24,5 degree. Combien de moles helium a til dans le contensnt
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, j’aimerais savoir si cette équation est correct:
Na2CO3(aq) + H2O(l) —> 2 Na+(aq) + 2 OH-(aq) + CO2(aq)
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir, j'aimerai savoir pourquoi lors de la résolution, on utilise l'acide propionique et non l'acide nitrique pour trouver la vitesse
-
Vérifiée par Alloprof
Secondaire 5 • 2aJ’aimerai savoir si cette équation est correct. Je m’intéresse particulièrement au chargé des produit
Na2CO3(aq) + H2O(l) —> 2 Na+(aq) + OH-(aq) + HCO3(aq)
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, j’aimerais savoir si cette équation est correct.
Na2CO3(aq) + 2 H2O(l) —> 2 Na+(aq) + 2 OH-(aq) + 2 HCO3(aq)
-
Vérifiée par Alloprof
Secondaire 5 • 2aComment puis-je calculer l’écart entre la plus petite et la plus grande valeur en pourcentage d’un laboratoire?
-
Vérifiée par Alloprof
Postsecondaire • 2aA//O BONJOURR
BYE BYE
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour!
Je voulais savoir si la modification des facteurs d’équilibre comme la température fait varier les concentrations des substances solides et liquides? Genre par exemple, dans la photo ci-dessous, est-ce que l’augmentation de la température fait diminuer NaHCO3 ( un solide) ou augmenter H2O ( liquide)? Ou est-ce qu’on doit simplement laisser ces cases vides….
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aComment indiquer la chaleur molaire de formation de chacune des substances formées lorsqu’ils y a deux produits?
ex:
2 C2H6 + 7 O2->4 CO2+6 H2O enthalpie=+2858kJ
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir, dans le cadre d’un laboratoire en chimie, nous avons dû procéder à la dilution du vinaigre deux fois. Lorsqu’est venu le temps de calculer la constante d’acidité pour les solutions diluées, mes réponses étaient proches de la constante théorique mais pas exactement pareil. Une question nous a donc été posée : « La constante d’acidité dépend-elle de la concentration en acide ? ». Je ne sais pas quoi répondre à cette question car je pensais que seule la température pouvait changer la constante d’acidité et que la variation de la concentration en acide n’influait pas la valeur de la constante. Le problème, c’est que plus je calculais la concentration d’une solution diluée, plus ma constante diminuait légèrement …Pourriez-vous m’aider ? Merci :)
-
Vérifiée par Alloprof
Secondaire 5 • 3acomment calculer la variation d’enthalpie molaire de formation du dioxyde de soufre:
2 H2S+3 O2 -> 2 SO2(g) + 2 H2O + 1036 kJ
-
Vérifiée par Alloprof
Primaire 4 • 3aPourquoi réaction solitaire ne fonctionne pas?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je dois calculer le constante de basicité du Na2CO3, mais je n’arrive pas à trouver l’équation de dissolution. C’est pour un rapport de laboratoire, donc j’avais juste la donné expérimental du pH. J’ai réussie à calculer la concentration de OH, qui est de 0,0000631 mol/L et la concentration initial de Na2CO3 est de 0,1 mol/L.
-
Vérifiée par Alloprof
Secondaire 5 • 3aSalut!
je voulais savoir, est ce que pour se numero ,il faudra appliqué IVE, pour savoir la concentration de la solution à l'équilibre(soustraire avec le concentration du h+ trouver à laide du ph) et après calculer KA.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour je ne sais pas comment trouver la pression partielle dans ce numéro alors que j'ai juste la pression totale et il y a seulement un gaz dans l'équation chimique. Je me demande donc si la pression totale est aussi la pression partielle du gaz concerné
-
Vérifiée par Alloprof
Secondaire 5 • 3aQuel est le lien entre la poudre de protéines et:
-aspect énergétique des transformations
-la cinétique chimique
-l'équilibre chimique
-
Vérifiée par Alloprof
Secondaire 5 • 3aSalut, j'ai un examen de laboratoire en chimie très bientôt et nous devons savoir comment déterminer l'ordre d'une réaction chimique expérimentalement sauf que je n'ai aucune idée comment la trouver. Est-ce qu'on pourrait m'aider?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
J’ai une question à propos de la théorie cinétique des gaz. Si la température augmente, cela veut dire que l’énergie cinétique augmente aussi. Or, est-ce que la vitesse cinétique augmentera aussi?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour!
Si le volume de titrant est plus grand pour neutraliser un acide qu'un autre, est-ce que l'acide ayant besoin de plus de titrant est faible ou fort?
Merci beaucoup!
-
Vérifiée par Alloprof
Secondaire 5 • 3aJe ne comprends pas comment régler ce problème?
Si on mélange dans un contenant isolé 100 g d'huile à 90,0°C et 100 mL d'eau à 25,0°C, quelle sera la température finale du mélange?
je sais que je dois utilisé la formule Q=mc delta t, mais je n’y arrive pas
-
Vérifiée par Alloprof
Secondaire 5 • 3aSalut!
je ne comprend pas ce que cest une reaction réversible exothermique. (n6)
-
Vérifiée par Alloprof
Secondaire 5 • 3aSalut!
cest pour le numero 13 b
j'ai la mauvaise réponse, pourquoi?
-
Vérifiée par Alloprof
Secondaire 5 • 3aSalut !Je ne suis pas sûr de comment faire le dernier numéro
-
Vérifiée par Alloprof
Secondaire 5 • 3aComment faire ce problème?
-
Vérifiée par Alloprof
Secondaire 5 • 3aSalut!
j'ai la mauvaise reponse ( la bonne est 1,77x10 à la -4) , mais je ne vois pas mon erreur.
-
Vérifiée par Alloprof
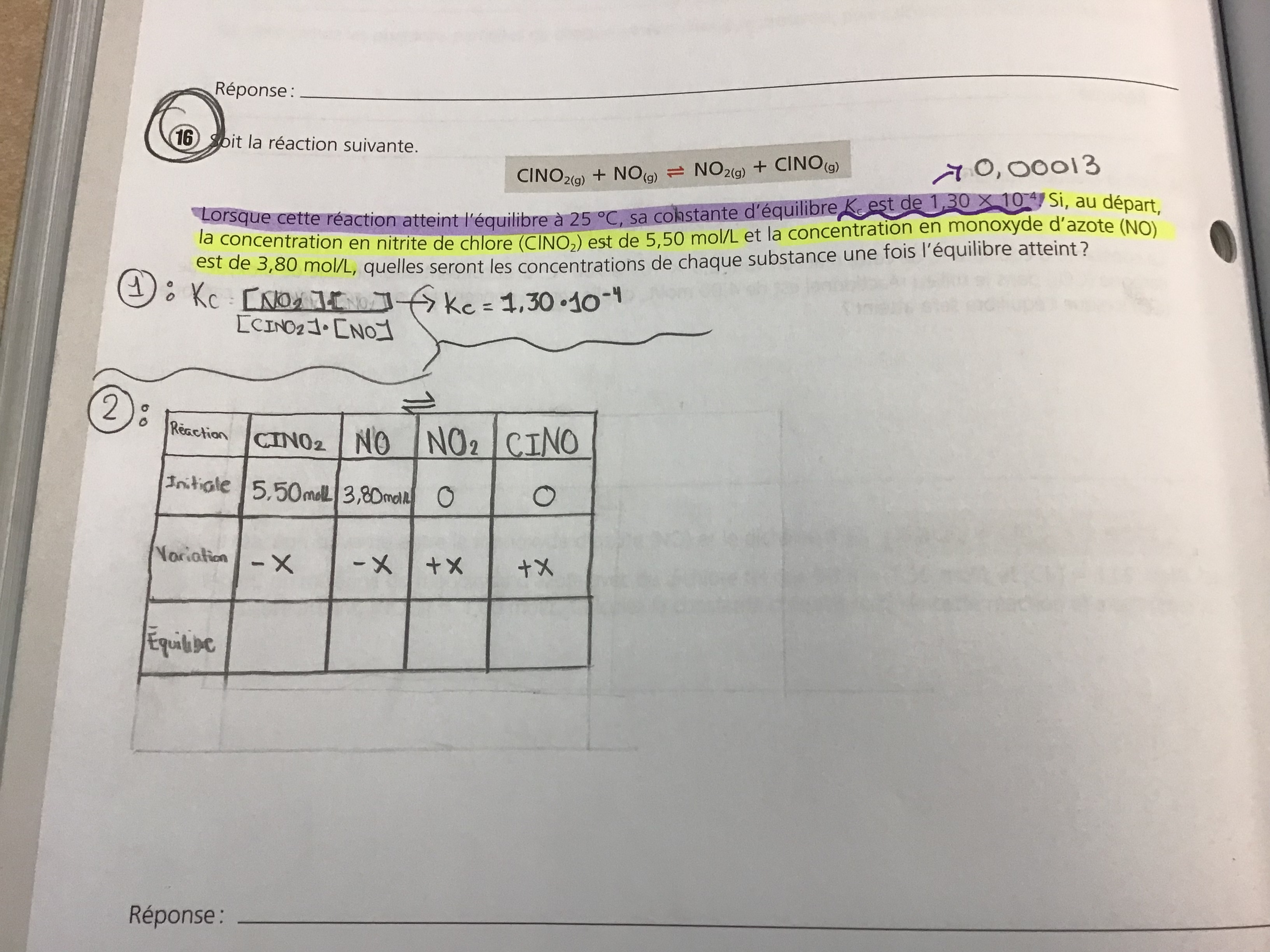
Secondaire 5 • 3aJe ne suis pas sure comment je dois utiliser la formule pour trouver toute les concentrations. Alors j’aurai besoin d’aide pour continuer.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour Equipe alloprof,
Je suis confronter a un excercice dans lequel je dois trouver le pourcentage de dioxygene par rapport a un melange de trois ballons dont le dioxygene. Par rapport a la question, dois-je trouver le pourcentage de dioxygene par rapport au nombre de mol ou par rapport a la pression.
Les donnes que nous avons sont les suivantes: le pressions partielles de chaque ballons, le volume de chaque ballon.
Merci d'avance.