Matières
Niveaux
Une réaction chimique, parfois appelée changement chimique ou transformation chimique, se produit lorsqu’une ou plusieurs substances, les réactifs, interagissent pour former une ou plusieurs nouvelles substances, les produits.
Un réactif est une substance consommée au cours d’une réaction chimique. Sa quantité tend à diminuer.
Un produit est une substance formée au cours d’une réaction chimique. Sa quantité tend à augmenter.
Contrairement aux changements physiques, une réaction chimique modifie la nature des substances impliquées. En effet, les réactifs d’une réaction chimique n’ont pas les mêmes propriétés caractéristiques que les produits formés.
De plus, on peut reconnaitre la présence d’une réaction chimique grâce à certains indices, tels qu’un changement de couleur, un dégagement gazeux, la formation d’un précipité, etc.
Les réactions chimiques peuvent être représentées de différentes façons et regroupées en catégories qu’on appelle les types de réactions chimiques.
Différentes représentations sont utilisées pour décrire les substances impliquées dans une réaction chimique. On représente généralement une réaction chimique à l’aide du modèle particulaire ou à l’aide d’une équation chimique.
Lorsqu’on représente une réaction chimique selon le modèle particulaire, les atomes sont généralement schématisés par des boules. La couleur et la grosseur des boules varient, de sorte que des atomes d’éléments différents sont représentés par des boules de couleur et/ou de taille différentes. De plus, les boules peuvent être assemblées pour représenter des molécules et des composés.
La réaction chimique de combustion du carbone peut être représentée à l'aide du modèle particulaire de la manière suivante. Dans cette réaction, 1 atome de carbone réagit avec 1 molécule de dioxygène pour produire 1 molécule de dioxyde de carbone.
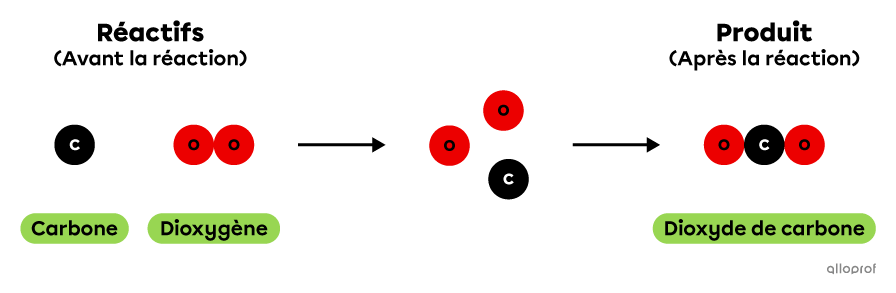
La combustion du carbone selon le modèle particulaire
Une réaction chimique peut correspondre à plusieurs types de réactions à la fois. Par exemple, la réaction de respiration cellulaire correspond à la fois à une réaction d’oxydation et à une réaction de décomposition.
Une réaction de synthèse est un type de réaction chimique où deux réactifs ou plus interagissent pour former un nouveau produit.
On peut reconnaitre une réaction de synthèse en analysant le nombre de réactifs et de produits différents, ainsi que la complexité des substances impliquées.
Il est possible de reconnaitre une réaction de synthèse grâce aux indices suivants :
les réactifs sont plus nombreux que les produits;
les réactifs sont des substances plus simples que le ou les produits formés.
Dans la réaction suivante, de l’éthylène réagit avec du dihydrogène pour former de l’éthane.
Il s’agit d’une réaction de synthèse parce que deux réactifs, soit de l’éthylène et du dihydrogène, réagissent pour former un produit, de l’éthane. Les réactifs sont donc plus nombreux que les produits. De plus, les deux réactifs impliqués sont des molécules plus simples que le produit formé. En effet, l’éthylène et le dihydrogène contiennent chacun moins d’atomes que l’éthane.
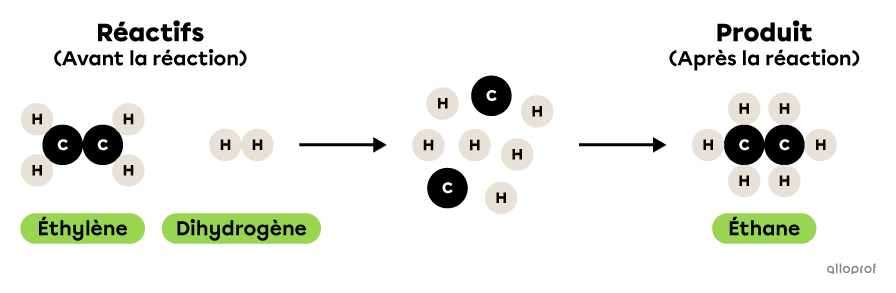
La synthèse de l’éthane
La photosynthèse est une réaction de synthèse dans laquelle du dioxyde de carbone réagit avec de l’eau en présence d’énergie lumineuse pour produire du glucose et du dioxygène.
On reconnait qu’il s’agit d’une réaction de synthèse parce que la molécule de glucose produite est plus complexe que les deux réactifs impliqués.
Chez les végétaux, cette réaction chimique se déroule dans les chloroplastes.
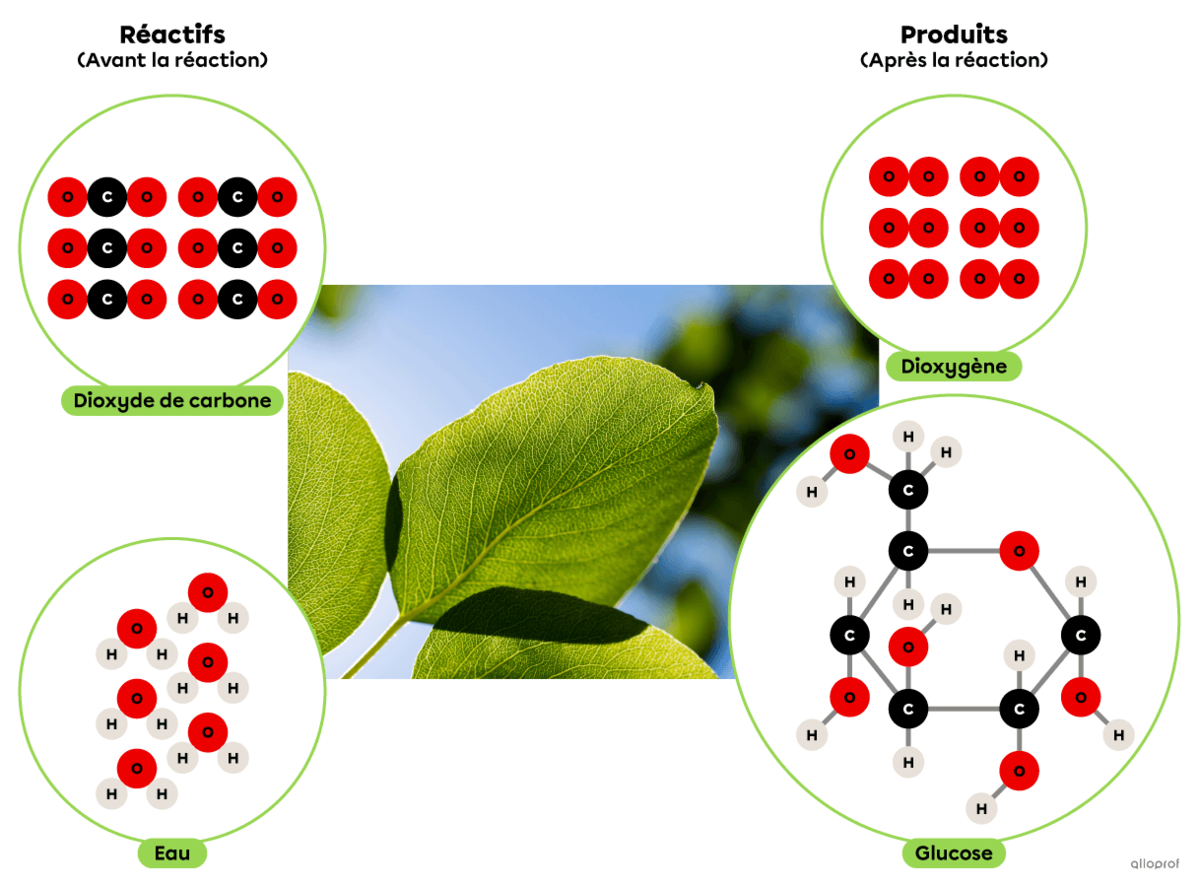
La photosynthèse selon le modèle particulaire
Une réaction de décomposition est un type de réaction chimique où les atomes d’un réactif se dissocient et se réorganisent pour former plusieurs produits.
On peut reconnaitre une réaction de décomposition en analysant le nombre de réactifs et de produits différents, ainsi que la complexité des substances impliquées.
Il est possible de reconnaitre une réaction de décomposition grâce aux indices suivants :
les produits sont plus nombreux que les réactifs;
le ou les réactifs sont des substances plus complexes que les produits formés.
Lors de la réaction suivante, le peroxyde d’hydrogène se décompose pour former du dihydrogène et du dioxygène.
On reconnait qu’il s’agit d’une réaction de décomposition parce qu’un seul réactif, soit le peroxyde d’hydrogène, est décomposé pour former deux produits, soit du dihydrogène et du dioxygène. De plus, le peroxyde d’hydrogène est une molécule plus complexe que chacun des deux produits formés. En effet, elle contient plus d’atomes que le dihydrogène ou le dioxygène.
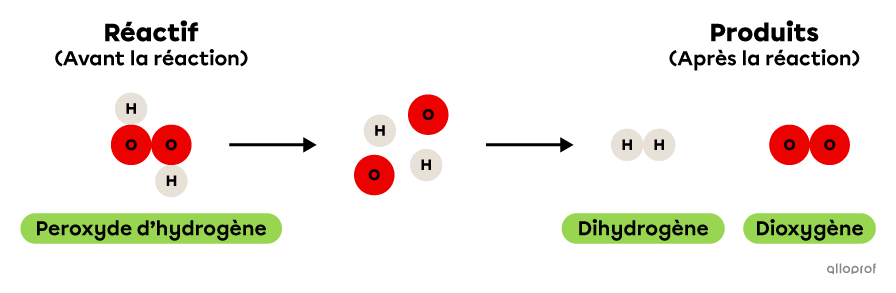
La décomposition du peroxyde d’hydrogène
Lors de la digestion chimique, des réactions de décomposition permettent à des molécules complexes, comme les constituants alimentaires, d’être décomposées en molécules plus simples et assimilables par l’organisme, les nutriments.
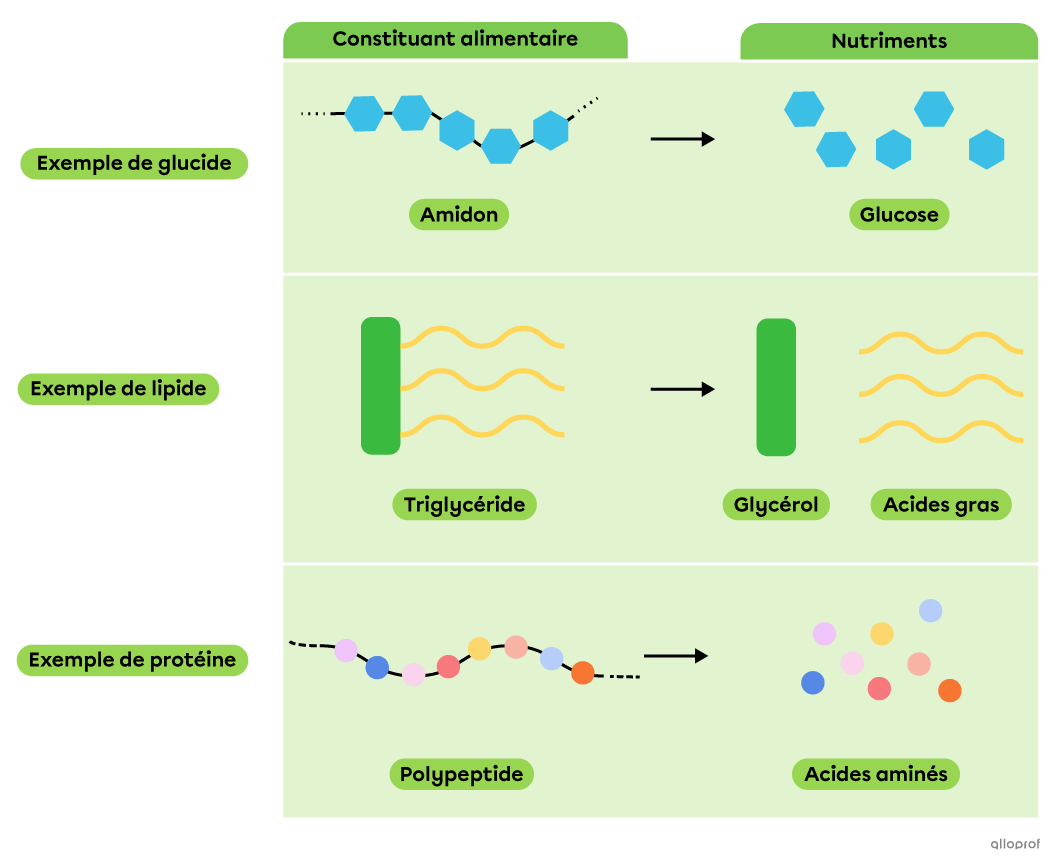
La décomposition des constituants alimentaires en nutriments
Une réaction de précipitation est une réaction chimique qui se produit lorsque deux substances en solution interagissent de manière à produire un solide peu ou non soluble appelé précipité.
Lorsqu’on mélange une solution de chlorure de sodium avec une solution de nitrate d’argent, on observe la formation d’un précipité blanchâtre.
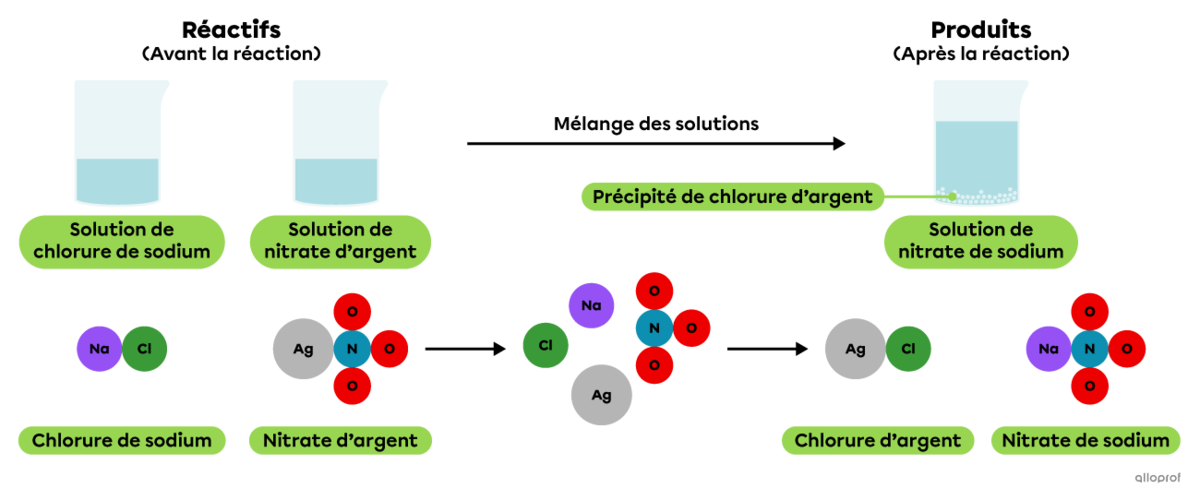
La précipitation du chlorure d’argent
Une réaction d’oxydation est une réaction chimique impliquant de l’oxygène ou une substance ayant des propriétés chimiques semblables à celles de l’oxygène dans les réactifs.
Lors de la réaction suivante, le fer réagit avec du dioxygène pour former de l’oxyde de fer, communément appelé de la rouille. Il s’agit en effet d’une réaction d’oxydation parce que le dioxygène est l’un des réactifs impliqués dans la réaction.

L’oxydation du fer
Les réactions de combustion sont des réactions chimiques au cours desquelles il se produit une réaction d’oxydation et un dégagement d’énergie.
Lors de la réaction de combustion suivante, le propane réagit avec du dioxygène pour former du dioxyde de carbone et de l’eau. De plus, la combustion du propane produit un dégagement d’énergie thermique qui est couramment utilisé pour la cuisson des aliments ou pour le chauffage des immeubles.
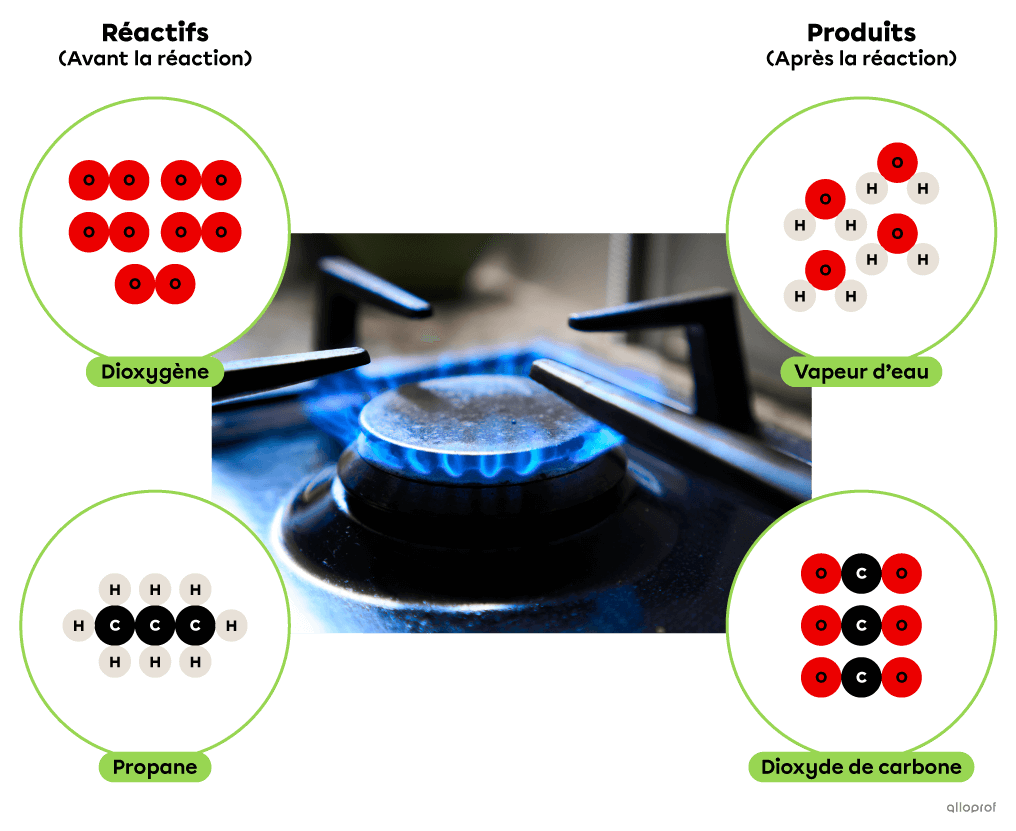
La combustion du propane
La respiration cellulaire est une réaction chimique se déroulant dans les cellules animales et végétales.
Elle comprend une réaction d’oxydation puisque le glucose réagit avec du dioxygène pour former du dioxyde de carbone et de la vapeur d’eau. De plus, la respiration cellulaire produit l’énergie essentielle au bon fonctionnement des cellules.
Puisqu’elle comprend une réaction d’oxydation et un dégagement d’énergie, on peut également affirmer que la respiration cellulaire est une réaction de combustion.
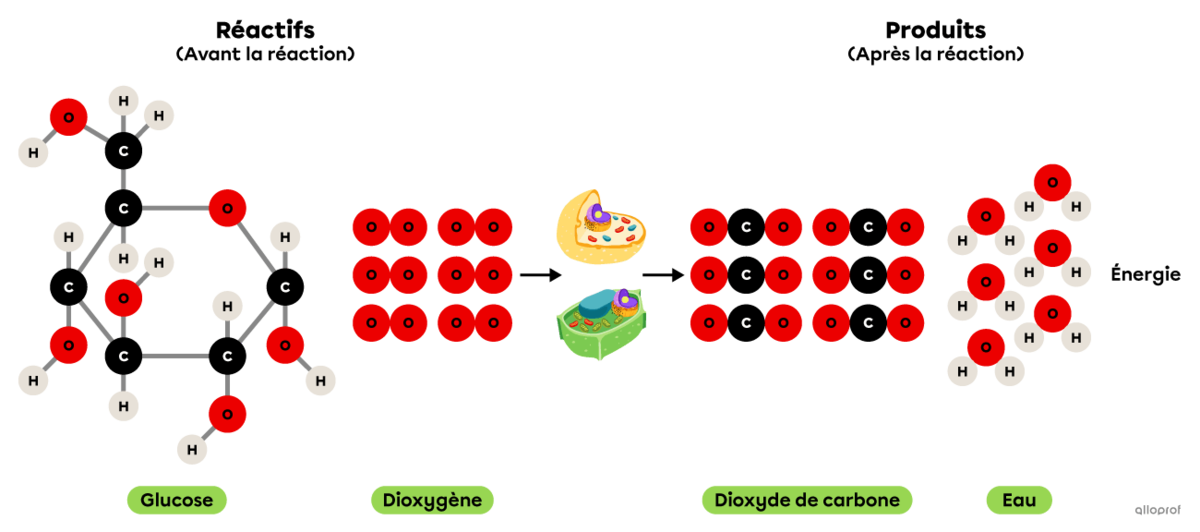
La respiration cellulaire