Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 3aJe me demandais comment formuler une ouverture dans une conclusion d'un laboratoire de chimie afin d'obtenir tous mes points .
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour à vous, le corrigé me donne cette réponse
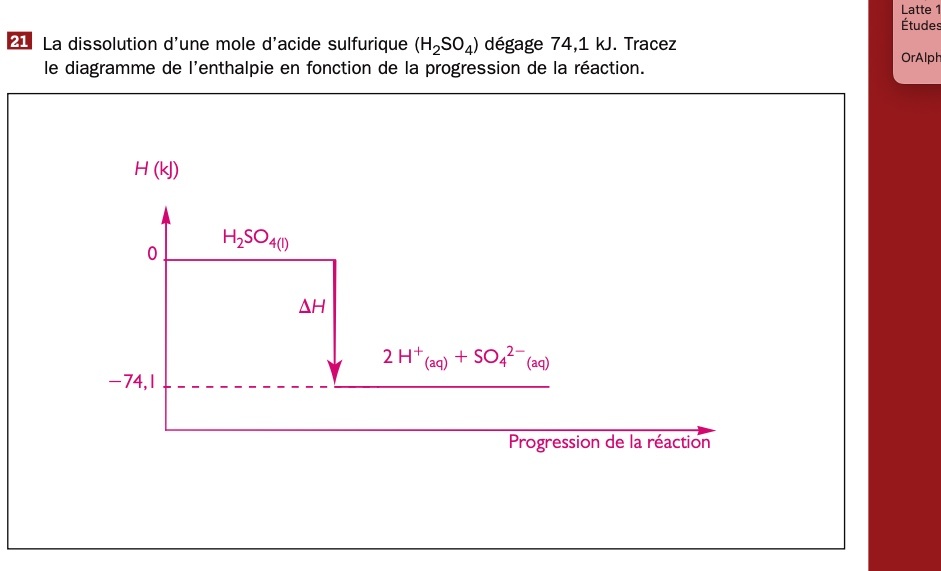
Ma question est au niveau d'une équation de dissolution.
Quand je fais l'équation de dissolution pour une mole de H2SO4,
ça me donne ceci:
H2S04(l) devient H2SO4(aq)
Dans un autre exemple d'une équation de dissolution le livre CHI-5061-2 p17 donne
C02(g) devient CO2(aq)
Pourquoi dans le corrigé les molécules des produits sont séparés?
-
Vérifiée par Alloprof
Primaire 5 • 3a2milmetre plus de sentilitre sa fait combien
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
J'essaie de résoudre ce problème:
Récrivez les équations suivantes en indiquant la chaleur de réaction en kJ/mol de produit. N’oubliez pas de respecter la convention des signes.
- d)La synthèse de 3 moles de dioxyde de soufre gazeux (SO2) dégage 890,4 kJ
Quand je fais l'exercice ma réponse est la suivante au niveau de l'équation ( Pour la chaleur massique j'ai déjà la réponse: -296,8kj/mol
3s(s) + 3O2(g) donne 3SO2(g)
Celle du corrigé donne celle-ci:
- S(s) + 2 O2(g) ➞ SO2(g) Pourquoi la réponse donne 2 O2 du côté des réactif et des produit elle donne SO2 sans avoir le 2 en avant de la molécule de SO2.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
J’ai déjà posé cette question et on m’a répondu, mais ça n’a rien changé. Je ne comprends toujours pas ce numéro.
« Dans cette expérience, on titre à deux reprises la quantité d'iode présente dans un échantillon 25,0 mL de solution aqueuse. Si la concentration du titrant est de 2,00 x10-4 mol/L et que le volume au point d'équivalence est de 45,0 mL, quel est le nombre de mole d'iode dans l'échantillon? »
Pouvez-vous m’expliquer la démarche à suivre ou me donner la réponse SVP 🙏?
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Je suis entrain de faire un rapport de laboratoire sur la chaleur molaire de dissolution et je m’occupe de faire les tableaux des données et des résultats. Je me demandais c’est quoi la différence entre le tableau des données et celui des résultats. Je me demandais aussi qu’est que je dois indiquer dans chaque un des tableaux.
Merci,
-
Vérifiée par Alloprof
Secondaire 5 • 3aje n'arrive pas répondre à cette question
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir,
Je n’arrive pas à répondre à une question en chimie et je me demandais si vous pouviez m’orienter ou, dans le meilleur des mondes, me donner la réponse.
La question va comme suit:
« Dans cette expérience, on titre à deux reprises la quantité d'iode présente dans un échantillon 25,0 mL de solution aqueuse. Si la concentration du titrant est de 2,00 x10-4 mol/L et que le volume au point d'équivalence est de 45,0 mL, quel est le nombre de mole d'iode dans l'échantillon? »
Merci d’avance!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je me demandais si j'avais bien fait les incertitudes pour ce calcul.
-
Vérifiée par Alloprof
Primaire 6 • 3aLorsqu'on mélange des Mentos et du Coke, pourquoi est-ce que ça explose?
-
Vérifiée par Alloprof
Secondaire 1 • 3aBonjour!
J'ai une question en lien avec les atomes et le modèle de John Dalton.
Comment sait-on de quoi est formé la molécule?
Merci beaucoup pour toutes vos réponses!
CarboneOptimiste5839 <3
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour! Je suis présentement en train de faire un laboratoire, et il faut indiquer les incertitudes absolues. Je comprend comment calculer celle-ci, mais je ne sais pas où les mettre dans mes calculs. C'est un labo sur la dissolution de chaleur molaire.
À présent, j'ai mis les incertitudes absolues dans les tableaux des données. Mais, par la suite, pour les calculs à l'aide de la formule Q=mcdeltaT, dois-je les mettre? Ou encore, pour calcluer la variation de température? Ou pour trouver le nombre de moles?
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aEst ce que jai bien fait le premier nuemro? Pour le deuxieme je ne comprend pas trop quoi faire apres.
-
Vérifiée par Alloprof
Secondaire 3 • 3atout atome ou groupe d'atomes qui transporte une charge électronique est appelé
-
Vérifiée par Alloprof
Postsecondaire • 3aBonsoir ca fait 4 heures que je me casse la tête je comprends pas svp :
Un échantillon de 1,017 g de CaCO3 pur est neutralisé entièrement par 39,28 mL d'une solution de HCl. La réaction de neutralisation non équilibrée est la suivante :
CaCO3(s) + 2HCl (aq) = CaCl2(aq) + H2CO3
Calculer la concentration et le pourcentage masse volume de cette solution de HCl. (Réponses : C = 0,5174 M et %m/V = 1,886%)
-
Vérifiée par Alloprof
Secondaire 5 • 3aje n'arrive pas à répondre à cette question
-
Vérifiée par Alloprof
Secondaire 5 • 3aC'eat quoi la différence entre une réaction de neutralisation en une étape et une autre réaction faites en 2 étapes?
-
Vérifiée par Alloprof
Secondaire 5 • 3aSelon ce qu'on a apprit, n'importe quel gaz peut être dangereux s'il remplace l'oxygène dans l'organisme, donc ici quelle est la bonne réponse???
-
Vérifiée par Alloprof
Secondaire 5 • 3apouvez vous me dire laquelle est la bonne réponse
-
Vérifiée par Alloprof
Secondaire 5 • 3aEst ce que jai bien fait les 2 exercices? pour le #5 je netais pas certaine si la masse de l’eau était importante pour trouver la reponse
-
Vérifiée par Alloprof
Postsecondaire • 3aBonsoir,
Je tente de faire cet exercice, j'ai consulté allo prof pour les démarches d'un numéro similaire mais je ne parviens toujours pas à avoir la bonne réponse. Voilà le problème en question:
Calculez le nombre d'atome d'oxygène dans un échantillon de 2,8 kg de Cr(NO3)3 .
Merci beaucoup de m'aider le plus vite possible.
-
Vérifiée par Alloprof
Secondaire 5 • 3aJe ne comprend pas comment repondre a cette question, jai lu les notes d’Alloprof sur la capacité thermique massique mais je ne comprend pas.
-
Vérifiée par Alloprof
Secondaire 5 • 3aqj'ai eu la bonne réponse, mais je pense que j'ai tort.
merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir, c'est quoi les 4 façons qu'on peut utiliser pour calculer la chaleur d'une réaction pour savoir si elle est endothermique ou exothermique ? je sais qu'il y a la variation d'enthalpie, le bilan énergétique, la calorimétrie mais la quatrième je l'ai oublié ! Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aEst ce que jai bien repondu a la question?
-
Vérifiée par Alloprof
Primaire 6 • 3aBonjour
Je ne comprends comment l' H2o sevapore avec la chaleur. Pouvez vous m'aider a comprendre?
Merci :)
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour! Avez-vous une vidéo explicative pour un laboratoire en lien avec une seringue contenant un gaz à l’intérieur?
-
Vérifiée par Alloprof
Postsecondaire • 3aBonjour j'ai un DM dont un exo de dissolution auquel je n'ai absolument rien compris,pourtant j'suis pas mauvais en chmie.Merci de m'apporter quelques élément de réponse je veux la réponse á la question 5 svp
On considère la réaction de dissolution du sulfate d'argent Ag2So4 (s).La constante d'équilibre associé est de K=1,6.10^-5 mol de suflate d'argent (2 Ag+ (aq)+So4 2- (aq)) dans 500 mL d'eau
1.Ecrire l'équation d'la réaction associée a la dissolution du suflate d'argent.
2.Calculer le quotient d'la réaction initial.
3.Dans quel sens cette réaction va-t-elle se dérouler?
4.Dresser un tableau desciptif de la transformation et exprimer le quotion d'la réaction à l'équilibre.
5.Calculer l'avancement à l'équilibre.
6.Quelle est la masse de sulfate d'argent non dissolu?
-
Vérifiée par Alloprof
Postsecondaire • 3aAidez moi svp 🙏
On considère la réaction de dissolution de sulfate d'argent Ag2,5O Là valeur de la constante d'équilibre
associée à l'équation de la réaction vaut : K = 1, 6.10-5 . On introduit initialement 1,0.10-'mol de sulfate
d'argent dans 500nL d'eau
1 Éerire l'équation de la réaction de dissolution de sulfate d'argent
2 Calculer le quotient de réaction dans l'état initial avant toute évolution .
3 Dans quel sens évolue le système ?
4 Dresser le tableau d'avancenment descriptif de cette transformation et exprimer le quotient de réaction à
1'équi libre.
5 Calculer l'avancement de la réaction à l'équilibre
Quelle est la masse de sulfate d'argent non dissociée?
-
Vérifiée par Alloprof
Postsecondaire • 3aBonjour, je n’arrive pas à faire ce numéro le a) et le c), j’aurais besoin d’aide. Merci.