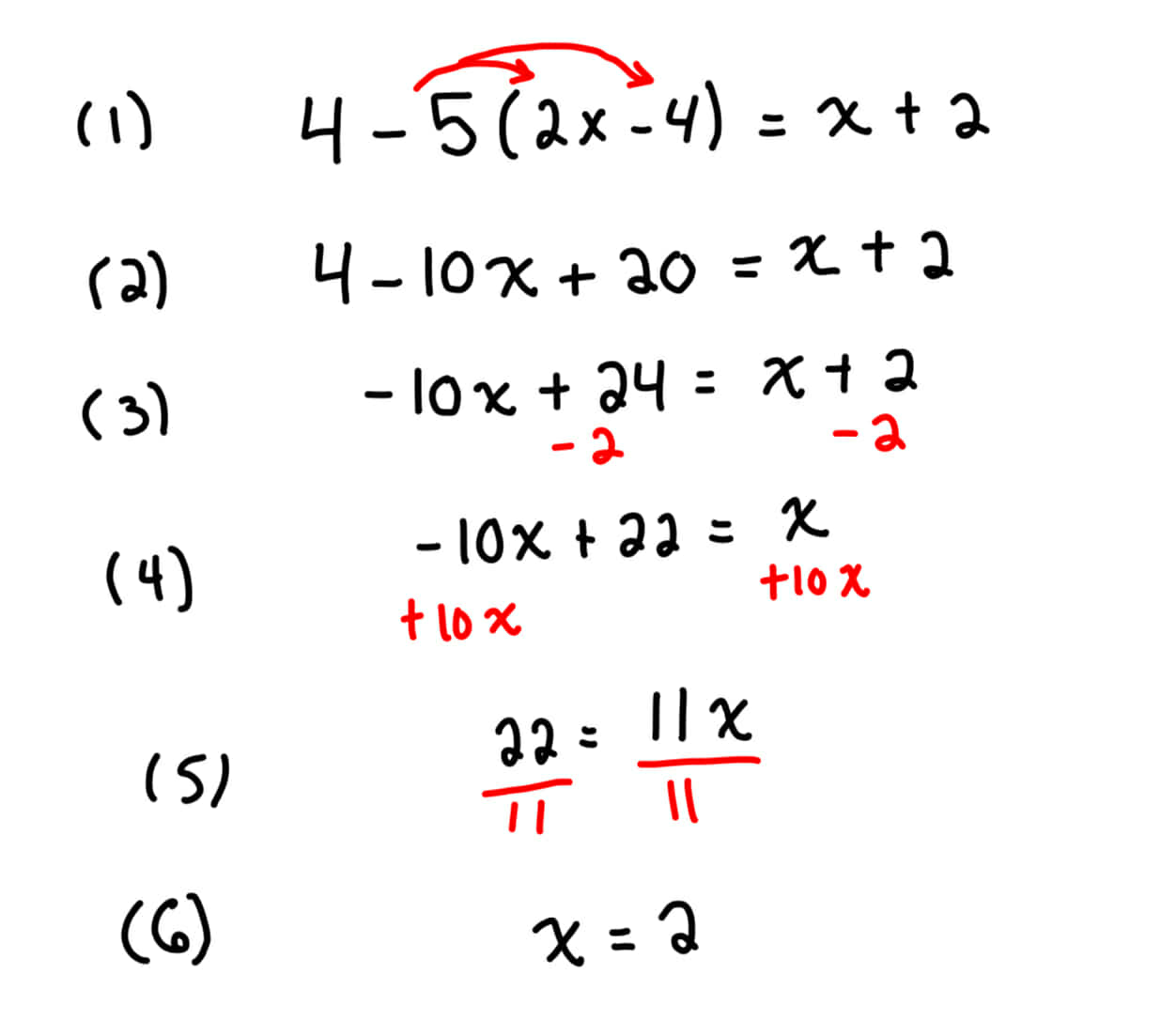Best Of
Re: Question
Bonjour ElfeTimide5414,
Merci pour ta question!
La technique de PCR est utilisée pour amplifier un morceau d'ADN. Lorsque l'on utilise cette technique, il faut avoir préalablement prélevé l'ADN des cellules. Une des étapes cruciales de l'extraction de l'ADN est l'étape de la lyse cellulaire. La lyse cellulaire permet de détruire les membranes des cellules pour libérer l'ADN qui se retrouve à l'intérieur. Ainsi, les cellules sont en quelque sorte « détruites » lors de cette étape. La centrifugeuse, quant à elle, sert bel et bien à séparer l'ADN du mélange. Les cellules ne se brisent donc pas lors de l'étape de la centrifugeuse.
Voici un lien pour plus d'informations :
J'espère avoir répondu à ta question! N'hésite pas si tu as d'autres questions!
Re: Question
Bonjour AbeilleDynamique5694,
Merci pour votre question!
En faisant le numéro, j'arrive à la réponse de votre fille. J'ai déterminé la valeur de x en détaillant chacune des étapes. Voici ma démarche :
J'espère vous avoir aidé! Si jamais vous avez d'autres questionnements, n'hésitez pas à nous réécrire!
Re: Question
Bonjour AbeilleDynamique5694, merci pour votre question !
Essayons de le résoudre ensemble.
$$4 - 5(2x - 4) = x + 2$$
Dans un premier temps, nous allons distribuer la parenthèse:
$$4 - 10x + 20 = x + 2$$
On va simplifier l'expression à gauche :
$$ 24 - 10x = x + 2$$
Maintenant, on va déplacer les termes constants à droite et les termes variables à gauche :
$$-10x - x = 2 - 24$$
On simplifie :
$$-11x = -22$$
Et enfin, on divise par -11 pour avoir seulement x à gauche :
$$x = \frac{-22}{-11}$$
Et nous avons donc :
$$ x = 2$$
N'hésitez pas à nous écrire si vous avez d'autres questions !
Re: Question
Bonjour MaringouinOptimiste2150, merci pour ta question !
En fait, c'est tout simplement un calcul de dilution ici ! Tu veux calculer le volume d'une solution d'eau de javel qui est moins concentrée que la première.
$$ C_1 V_1 = C_2 V_2$$
Ici, tu connais déjà la concentration initiale, le volume initial et la concentration finale, il ne te reste plus qu'à calculer le volume final.
Voilà une fiche pour t'aider : https://www.alloprof.qc.ca/fr/eleves/bv/sciences/la-dilution-c1v1-c2v2-s1054
N'hésite pas à nous écrire si tu as d'autres questions !
Re: Question
Bonjour!
1) L'électricité est acheminée à l'aide de lignes électriques. Pour en savoir plus sur le transport de l'électricité, je te suggère de consulter la page ci-dessous, qui provient du site d'Hydro-Québec :
2) Il est difficile pour moi de t'aider ici, puisque je ne sais pas de quelle source d'énergie tu parles. Je t'invite à nous réécrire en nous donnant quelques précisions.
3) Pour connaître les différents types de biomes terrestres, je te suggère de consulter la fiche ci-dessous :
Si tu as d'autres questions, n'hésite pas à nous réécrire. Nous te répondrons avec plaisir!
Laurie :)
Re: Question
Salut!
Merci de faire appel à nos services! 🙂
Voici quelques conseils que tu peux suivre pour t'améliorer en anglais :
- Regarde des vidéos, des films, des émissions en anglais (avec les sous-titres en français). Avec le temps, tu pourras mettre les sous-titres en anglais et ensuite complètement enlever les sous-titres.
- Joue à des jeux en anglais. Sur Alloprof, nous avons les jeux suivants : https://www.alloprof.qc.ca/fr/eleves/bv/jeux#f-topics=english
- Lis des livres en anglais, même s'ils sont petits ou pour les jeunes enfants. Recherche aussi les mots que tu ne comprends pas. Cela te permettra d'acquérir du vocabulaire. Notre jeu Book of Spells te propose plusieurs livres avec des niveaux de difficulté variable : Book of Spells | Alloprof
- Demande à tes ami(e)s ou à des membres de ta famille de parler en anglais avec toi. Ils/elles pourront te donner des conseils et cela te permettra de pratiquer la prononciation de certains mots.
Je te recommande également de consulter cette fiche, qui offre d'autres astuces efficaces pour progresser en anglais : Trucs pour s'améliorer en anglais | Alloprof
J'espère que cela t'aide! Tu es capable, ne perds pas espoir! :) N’hésite pas à nous réécrire si tu as d’autres questions! 🙂
Re: Question
Salut!
C'est faux! :) On ne peut pas distribuer la valeur absolue sur une addition :
$$ |-x+5|≠ |-x|+|5|=x+5$$
Donc, |-x+5| ≠ x+5
Voici une fiche présentant les différentes propriétés de la valeur absolue : La notation valeur absolue | Secondaire | Alloprof
Si tu as d'autres questions, n'hésite pas à nous réécrire! :)
Re: Question
Coucou CardinalVirtuose7123 !
Merci de nous avoir posé ta question.
En effet, tu dois calculer la TPS et la TVQ séparément et les additionner ensuite. La TPS (taxe sur les produits et services) et la TVQ (taxe de vente du Québec) sont calculées séparément parce qu'elles sont gérées par des administrations fiscales distinctes. La TPS est une taxe fédérale (Canadienne), administrée par l'Agence du revenu du Canada (ARC), tandis que la TVQ est une taxe provinciale, gérée par Revenu Québec.
Voici une fiche pour t'aider à faire les calculs :
Et une vidéo explicative :
J'espère que cela répond à ta question ! :)
N'hésite pas à repasser au besoin.
À bientôt :)
Re: Question
Salut FauconArtistique8879 !
Merci de nous avoir posé tes questions. :)
Tout d'abord, pour tes examens de sciences, je te conseille de réviser fréquemment la matière à l'étude. Nous avons des exercices sur Alloprof pour t'aider. Pour les mathématiques, il s'agit de s'exercer également.
Voici une fiche avec des conseils pour t'aider à te préparer à tes examens :
En ce qui concerne tes résultats scolaires, essaye de comparer tes résultats avec toi-même. L'important est que tu t'améliores ! :) Essaye de seulement te comparer avec toi-même. Si tes résultats scolaires s'améliore et que tu as la note de passage, je crois que tu peux être fier de toi. :)
Finalement, la cote R c'est un calcul du rendement (ou des résultats) scolaire des élèves qui sont au CÉGEP. Ce résultat entre 0 et 50 permet de classer les étudiants peu importe l'école à laquelle ils ont étudié. Ensuite, les étudiants ont accès à certains programmes universitaires selon leurs résultats.
Voici un site internet qui t'explique en détail la cote R:
J'espère que cela répond bien à tes questions.
N'hésite pas à repasser nous voir ! :)
À bientôt !
Re: Question
Salut FauconArtistique8879 😁
Merci pour ta question!
L'examen est une bonne matière de vérifier ta compréhension de la matière. Aussi, des exercices le sont. Essayer d'expliquer la notion à un.e collègue permet aussi de valider ses connaissance et sa compréhension.
Écris-nous si tu as d'autres questions. 😊
À bientôt sur la Zone d'entraide! 😎