Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir, j'espère que vous allez bien.
J'ai besoin d'aide sur ce numero.
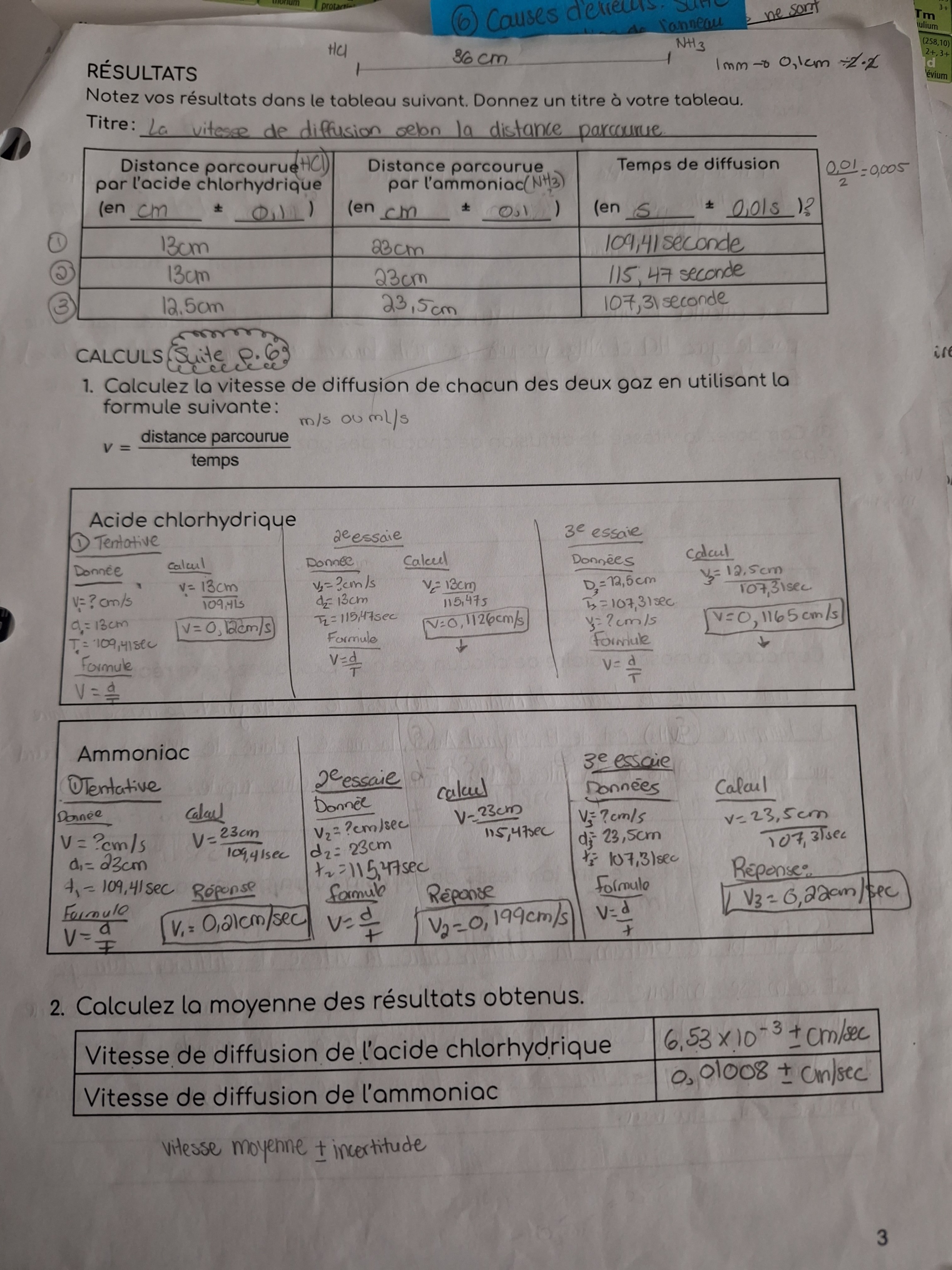
MerciVoici mes demarches. Là je ne sais pas comment faire pour trouver a partir de quel wagon le nuage de chlorure d'ammonium est apparu. J'ai lu d'autre élèves qui ont poser cette question mais j'ai pas compris
Merci
-
Vérifiée par Alloprof
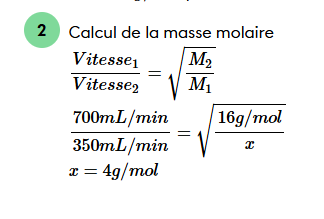
Secondaire 5 • 1abonjour je n'arrive pas a comprendre comment il on fait pour resoudre sa. comment je doit rentrer sa dans la calculatrice. je voudrais savoir comment faire si mon x etait dans les 4 place.( v1 ou v2 ou m2 ou m2)et celui la aussi j'Ai pas compris
-
Vérifiée par Alloprof
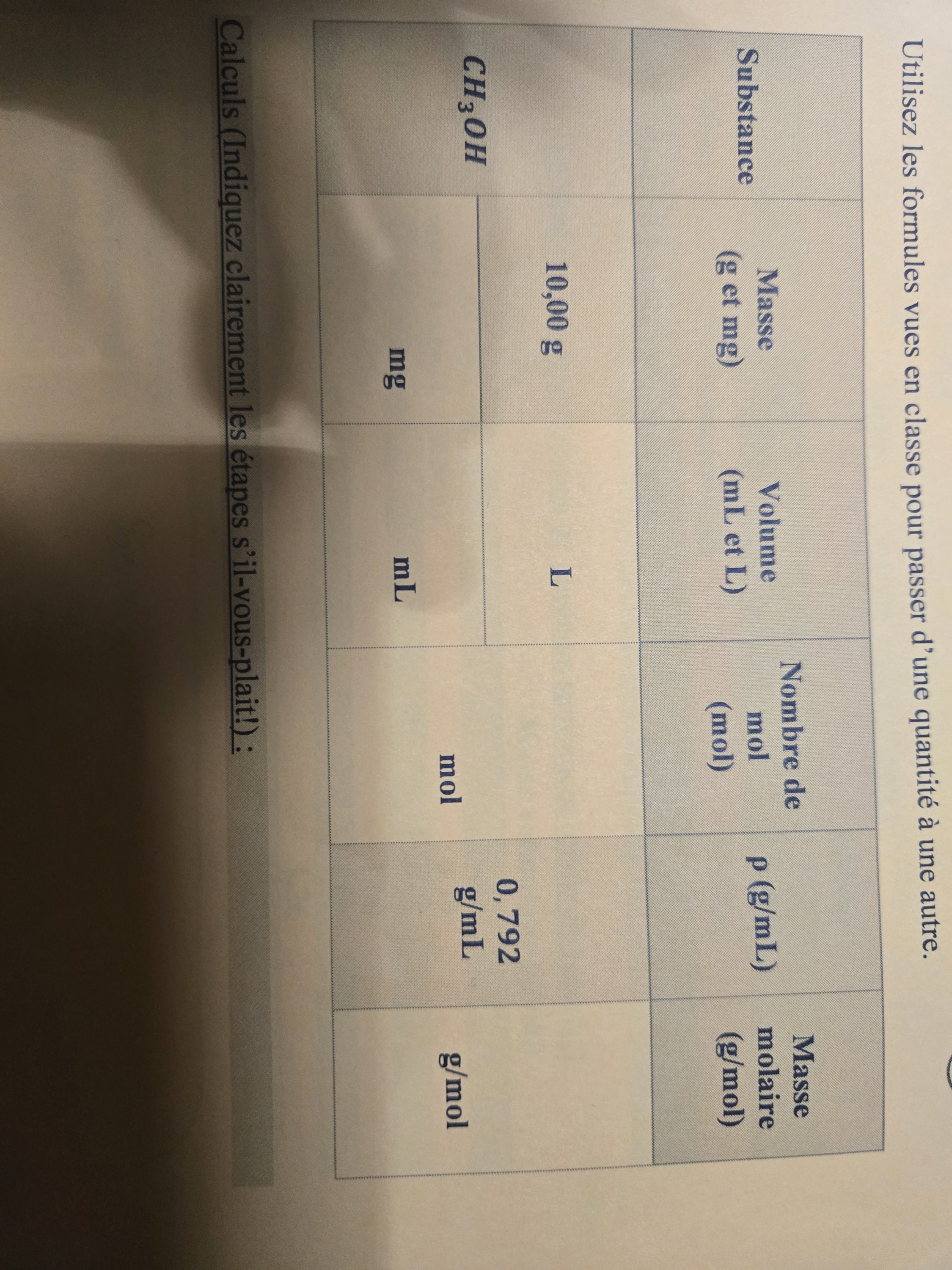
Secondaire 5 • 1aBonjour j'ai ce tableau à remplir. Je ne sais pas par où commencer. Comment savoir si j'utilise les bonnes formules?mmencer.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, je me demandais si à température et pression constante un gaz x et un gaz y peuvent avoir le même nombre de moles? Ex: Si on a 1L d'O2 et 1L de H à température et pression constate vont-il avoir le même nombre de moles?
-
Vérifiée par Alloprof
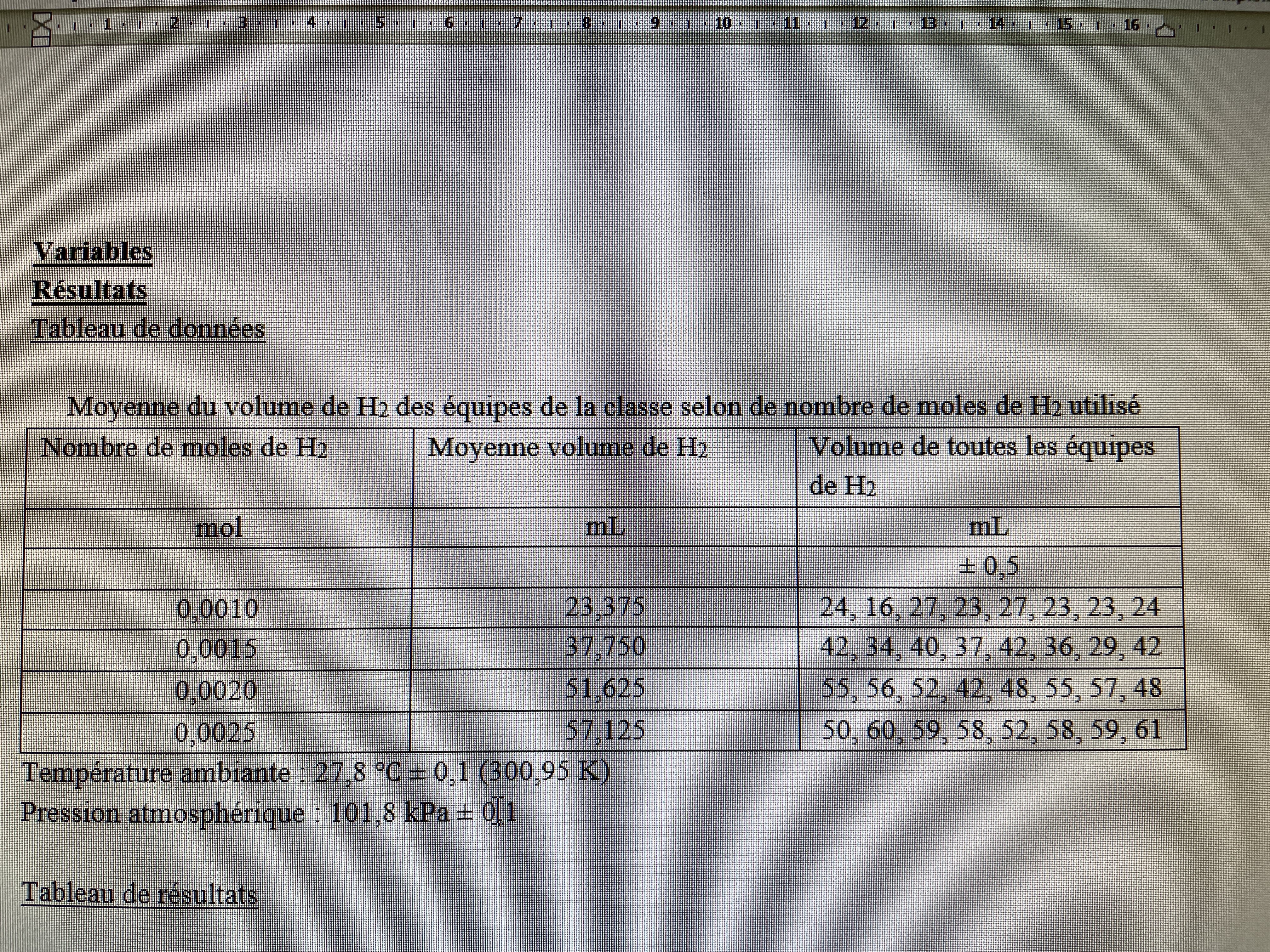
Secondaire 5 • 1aBonjour dans un tableau de données qui représente la moyenne du volume de h2 des équipes de ma classe selon de nombre de moles de h2, je dois faire une colonne avec les données de chaque équipe. La façon que je l’ai fait n’est pas bonne. Quelle serait un bonne façon de faire la colonne (la troisième)? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour pouvez vous m’expliquer comment faire le numéro c)? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour Alloprof, pourriez-vous m'expliquer ce numéro que je ne comprends pas?
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! Que faut-il faire avec l'information que c'est contenant rigide? Est-ce que cela veut dire que P1 = 101,3kPa?
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! Je ne comprend pas laoi des combinaisons gazeuses, pourriez-vous m'aider s'il-vous-plait? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir,
Quel serait un exemple de protocole d’un laboratoire pour trouver la masse molaire d’un gaz inconnu en trouvant le nombre de moles d’un autre gaz dont on connaît la nature?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aEst ce que j'ai la bonne formule? Comment faire pour trouver les autres valeurs . Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, je ne comprend pas pouquoi au P1 et P2 faut soit additionner ou soustraire avec la pression atmosphérique.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir,
Est-de que vous pouvez m’expliquer comment répondre à cette question?
Merci beaucoup et bonne soirée!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, est l’exercice cinétique moyenne ET l’énergie cinétique sont les mêmes pour tous les gaz si la tempéture est la même.
merci : )
-
Vérifiée par Alloprof
Secondaire 5 • 1aJe comprends la réponse, mais pourquoi le D n'est pas bon ?
-
Vérifiée par Alloprof
Secondaire 5 • 1aJe ne comprends pas pourquoi le B n'est pas vrai. Merci de m'aider.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! Je ne comprends pas ce problème et je ne pense pas avoir bien noté mes variables.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, j’ai déjà posé cette question mais je la repose car je ne comprends tjr pas.Donc en me basant sur cette exercice, je me dis que l’exercice cinétique moyenne et l’énergie cinétique est la même pour tous les gaz si la tempéture est la même. Toutefois, si c’était réellement le cas,c’est l’exercice B qu’on aurait coché mais ce n’est pas le cas, on a coché le C. Je suis mêlé, j’ai l’impression que les deux exercices ce contredise même si je sais que c’est impossible que ce soit le cas. Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, je ne comprends pas calculer l’erreur relative sur une température. Admettons que j’ai une température de zéro degré Celsius et une erreur absolu de plus ou moins 0,1 degrés Celsius comment puis-je faire ce calcul.
-
Vérifiée par Alloprof
Postsecondaire • 1aQuel est le calcul pour la concentration volumique en % v/v?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour. Est-ce que l’énergie cinétique des gaz n’est pas la même chose que l’énergie cinétique moyenne des gaz. Si j’ai bien compris pour l’énergie cinétique moyenne d’un gaz, s’il y a la même température et l’énergie cinétique moyenne est la même. Par contre, pour l’énergie cinétique, il faut tenir compte de la masse molaire des gaz et de leur vitesse même si la température est la même ?
merci !
-
Vérifiée par Alloprof
Secondaire 5 • 1a- Je ne comprends pas cet énoncé :
- L’énergie cinétique du mouvement de translation de ces particules est relative à la température absolue. L’énergie cinétique moyenne des particules de n’importe quel gaz est donc identique à la même température.
-
Vérifiée par Alloprof
Secondaire 4 • 1aje ne comprend pas les atomes poly atomiques. Comment puis-je savoir leur but et est ce que je doit les mémoriser
-
Vérifiée par Alloprof
Secondaire 5 • 1abonjour! est-ce que le volume molaire d’un gaz est une propriété caractéristique de chaque gaz? mercii:)
-
Vérifiée par Alloprof
Postsecondaire • 1aBonjour,
Je ne suis pas sûre comment faire la question 2 ci-dessous. J'utilise la formule C1V1=C2V2 pour trouver ma concentration en OH- et je fait la différence pour le H+, mais ça me donne un nombre négatif.
1. Quelle masse de soude faut-il dissoudre dans 0.4 L d’eau pour obtenir une solution ayant un pH égal à 12 ?
2. À 0.1 L de cette solution de soude (pH = 12), on ajoute 0.7 L d’eau. Quelle est la nouvelle concentration molaire en ions OH et H+ de cette solution ?
3. Quel est son nouveau pH ?
-
Vérifiée par Alloprof
Secondaire 5 • 1aJe ne comprends toujours pas pouvez vous m’aider svp
-
Vérifiée par Alloprof
Secondaire 5 • 1aJe ne comprends pas ce numéro pourriez-vous m’aider svp.
-
Vérifiée par Alloprof
Secondaire 5 • 1aSalut!
Dans un laboratoire de chaleur molaire de dissolution où il faut dissoudre ( dans un calorimètre) une certaine quantité d’un soluté X dans une certaine quantité d’eau, qu’est ce qui pourrait expliquer le fait que la chaleur molaire expérimentale soit inférieur à la chaleur molaire théorique?
Merci!
-
Vérifiée par Alloprof
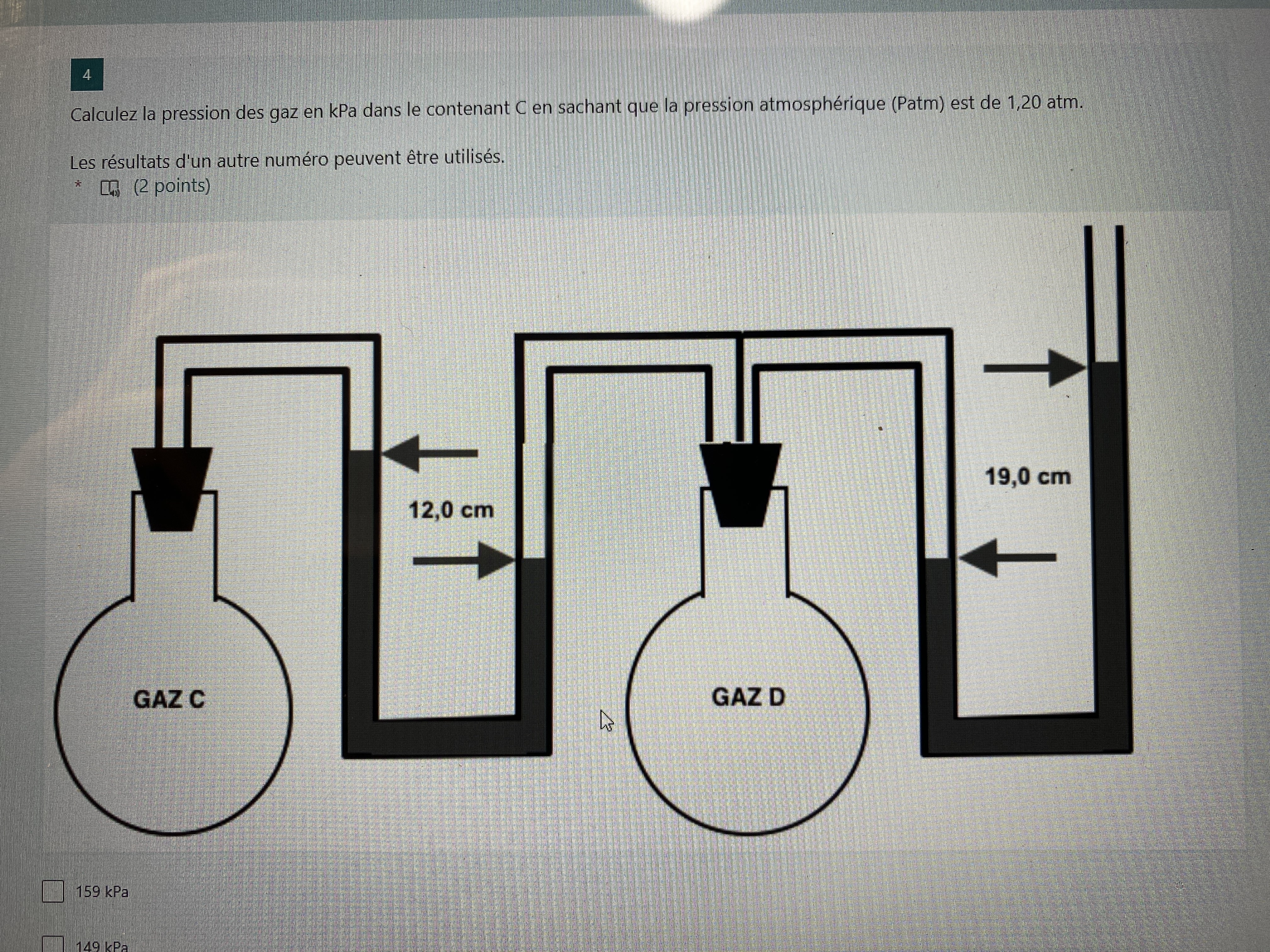
Secondaire 5 • 1aJ’aimerais savoir comment faire pour trouver la pression du gaz C et D si la pression est de 1,20 atm.
-
Vérifiée par Alloprof
Secondaire 5 • 1aAllo!
quel est un bon titre pour mon tableau? J’en ai fait deux, mais je ne suis pas trop sûre. Il ne doit pas être trop long, mais doit être clair en même temps et j’ai peur de ne pas mettre assez d’infos. C’est mélangeant!Aussi, j’ai juste créé une colonne « random » pour mon pourcentage de rendement qui n’a pas de lien avec aluminium ou alun. Est-ce que c’est correct ou vous pouvez que je vais perdre des points?