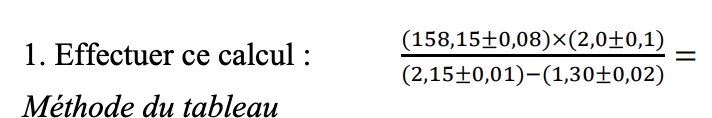Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 1aRebonjour,
Je ne comprends toujours pas comment faire une formule chimique à l'aide des ions positifs et négatifs. Par exemple:
Al 3+ et O 2- = Al2O3
Quel est le processus pour arriver à cette réponse? Et comment savoir si on doit ajouter à l'aluminium ou à l'oxygène pour rendre le tout neutre?
Merci :)
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Je ne comprends pas comment faire une formule chimique à l'aide des ions positifs et négatifs. Par exemple:
Li+ et SO3 2- = Li2SO3
Quel est le processus pour arriver à cette réponse?
Merci :)
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour, je ne comprends pas la masse molaire. Pouvez-vous m'expliquer en détails comment ça marche?
Merci beaucoup
-
Vérifiée par Alloprof
Secondaire 5 • 1aest ce qu’on pourrait m’expliquer la question? S’il vous plaît 😄
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! Je fait de la revision de l'an passer en sciences et J'ai une question qui dit"Quelle est la concentration en ions H+ d'une solution dont le ph est 4,7" et il y a un Tableau en dessous (vide) je ne suis pas sûre de savoir quoi faire....
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Pouvez-vous m'aider avec les charges des ions polyatomiques et les charges d'atome comme le fer?
Et qu'est-ce que des métaux de transferts et comment affecte t-ils une charge?
Merci :)
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
pouvez-vous m’aider avec ce problème je ne le comprend pas vraiment ce que je doit faire
merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aJe ne comprends pas pourquoi je n’arrive pas à la bonne réponse
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour! Je ne comprends pas bien la notation de Lewis, Je comprends que le nombre point représente le nombre d’électrons à la dernière couche électronique mais je ne comprends pas comment la façon de placer les point autour du symbole a une importance comme pour l’hélium.
Merci beaucoup!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
j’aimerais savoir quand utiliser et différencier la Masse molaire atomique et moléculaire de l’utilisation du nombre d’atome et de particule. Par exemple dans ce devoir, quand est-ce nécessaire de calculer le nombre de particules et quand doit-je seulement utiliser la masse molaire du tableau périodique et les additionner. Il s’agit d’un devoir de chimie secondaire 5. J’espère que vous pourrez m’aider et bon début d’année à tout les étudiants. Merci d’avance pour l’aide. 😀👊
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour.
Je ne pas compris pourquoi la réponse est ça (le O).:
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour
Dans mon cahier de chimie.
Il disait que la dissolution de propane était représenté comme celle ci:
C3H8 —h2o—-> 3 C -4 + 8 H+. Pourquoi est ce que le produit n’a pas le même nombre d’électron perdu que gagner . Je croyais que puisque que le réactif est neutre , L’addition des produits seraient aussi neutre.
Merci
NeptuneSarcelle6678
-
Vérifiée par Alloprof
Postsecondaire • 1aComment puis-je calculer ma concentration de HCL concentré en ayant seulement le pH (2.25), le volume 10ml et la masse molaire qui est de 36.46 g/mol?
merciiiii
-
Vérifiée par Alloprof
Postsecondaire • 1aAllô, aujourd’hui j’ai eu un laboratoire de chimie sur la préparation des solutions de sel (NaCl) et de sucre. Je dois maintenant remplir un compte rendu avec les informations que j’ai annoté. Je l’avoue, je ne sais pas trop quoi faire pour « le volume total de la solution (Vsln) »
De plus, je ne suis pas sûre de comprendre, dans le tableau 2, les volumes des solutions concentrées. (Voir image)
J’ai vraiment besoin d’aide, merci infiniment.
-
Vérifiée par Alloprof
Secondaire 5 • 1aÇa fait 50 minutes que jattend pour l'aide d'un prof mais personne répond
Alors je vais poser ma question ici :Est ce que je dois arrondir le b) si oui comment
-
Vérifiée par Alloprof
Secondaire 5 • 1abonjour, pouvez vous me dire pourquoi les polyatomique ont une charge. Exemple : pourquoi SO4 a une charge de -2.
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour,
Je me demandais pourquoi il y a une capacité maximum de 8 électrons de valence (sur la dernière couche électronique), sachant que la capacité maximum d'électrons par couche est de 8, 18, 32, 50... (ordre de couche électronique). De plus, qu'est-ce qui caractérise le nombre d'électrons sur une couche électronique? Par exemple, comment se fait-il que l'atome Astate (85 protons, famille des Halogènes...) a ses électrons placé ainsi : 2, 8, 18, 32, 18, 7? Qu'est-ce qui fait que ce n'est pas 2, 8, 18, 32, 17, 8?
Merci beaucoup!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour je comprend pas pourquoi je ne trouve pas la même réponse.La réponse est 12,50 mol j’ai trouvé 1,25x10^47 mol
-
Vérifiée par Alloprof
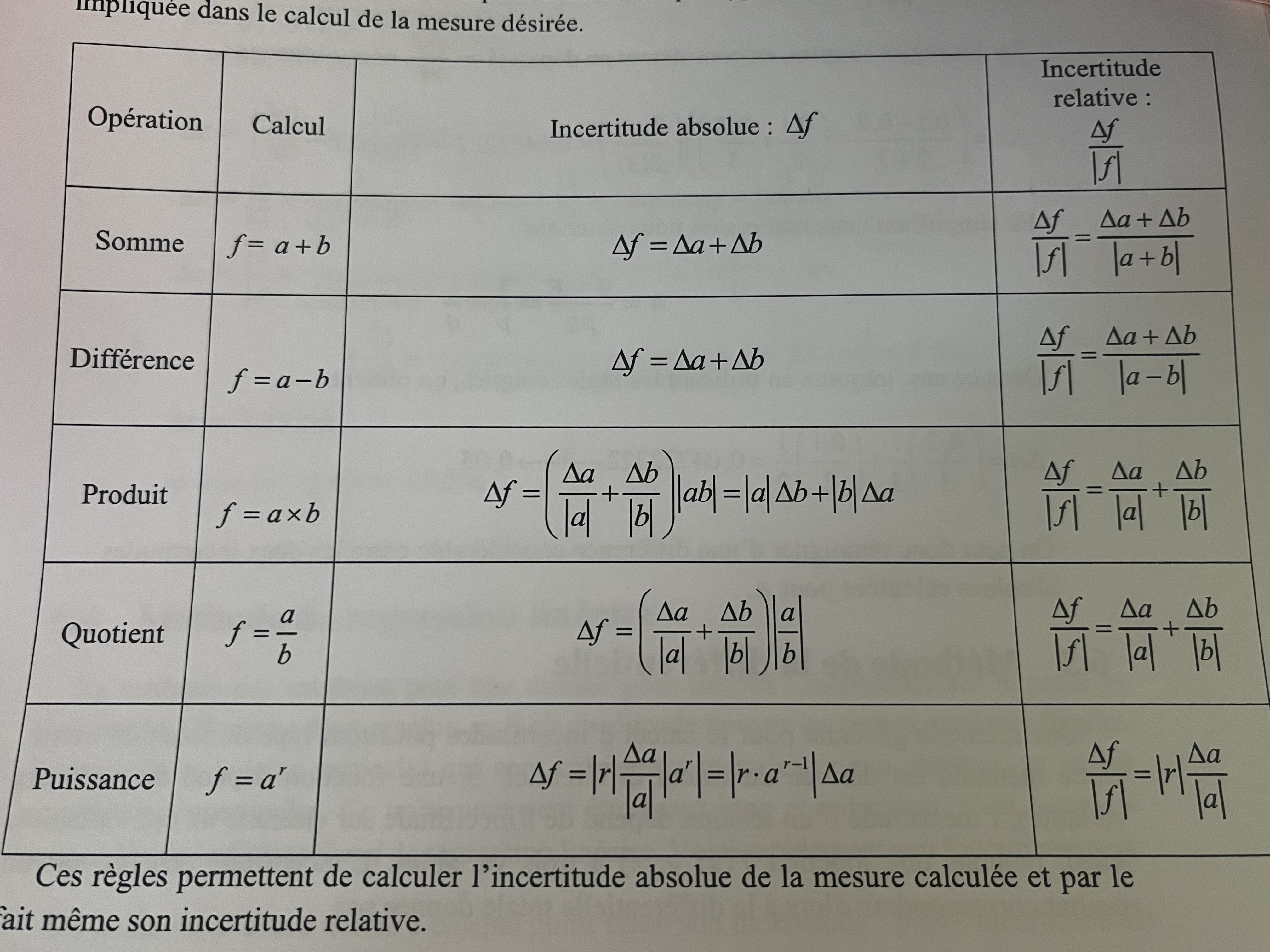
Secondaire 5 • 1aBonjour! Je faisais des calculs d’incertitude et dans le corrigé on me dit d’utiliser cette formule afin de résoudre ça:
Cependant, dans la liste de formule, je ne vois pas cette proposition où on multiplie par f à la fin, dans le cas où il n’y a pas de puissance…Merci!
-
Vérifiée par Alloprof
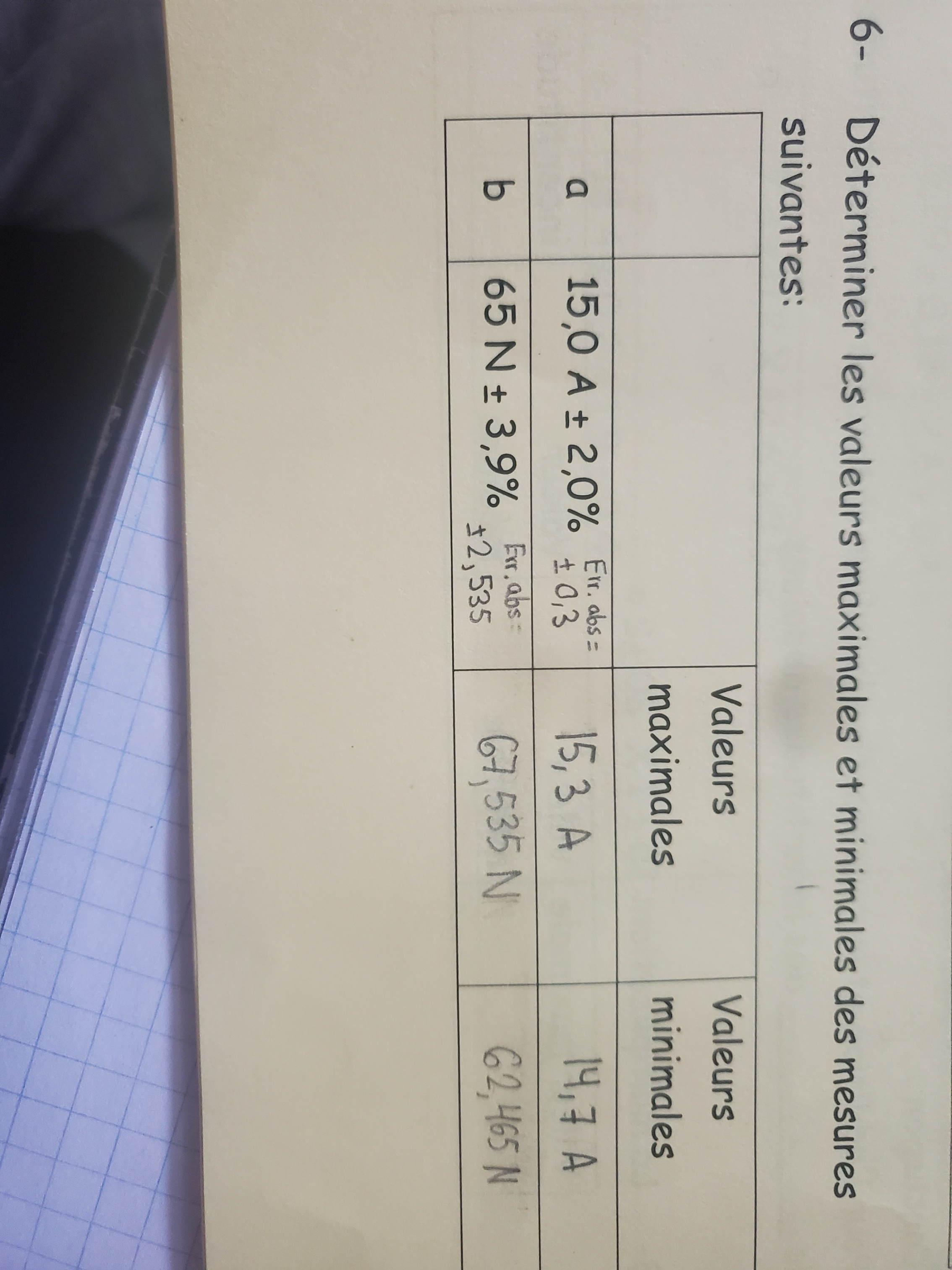
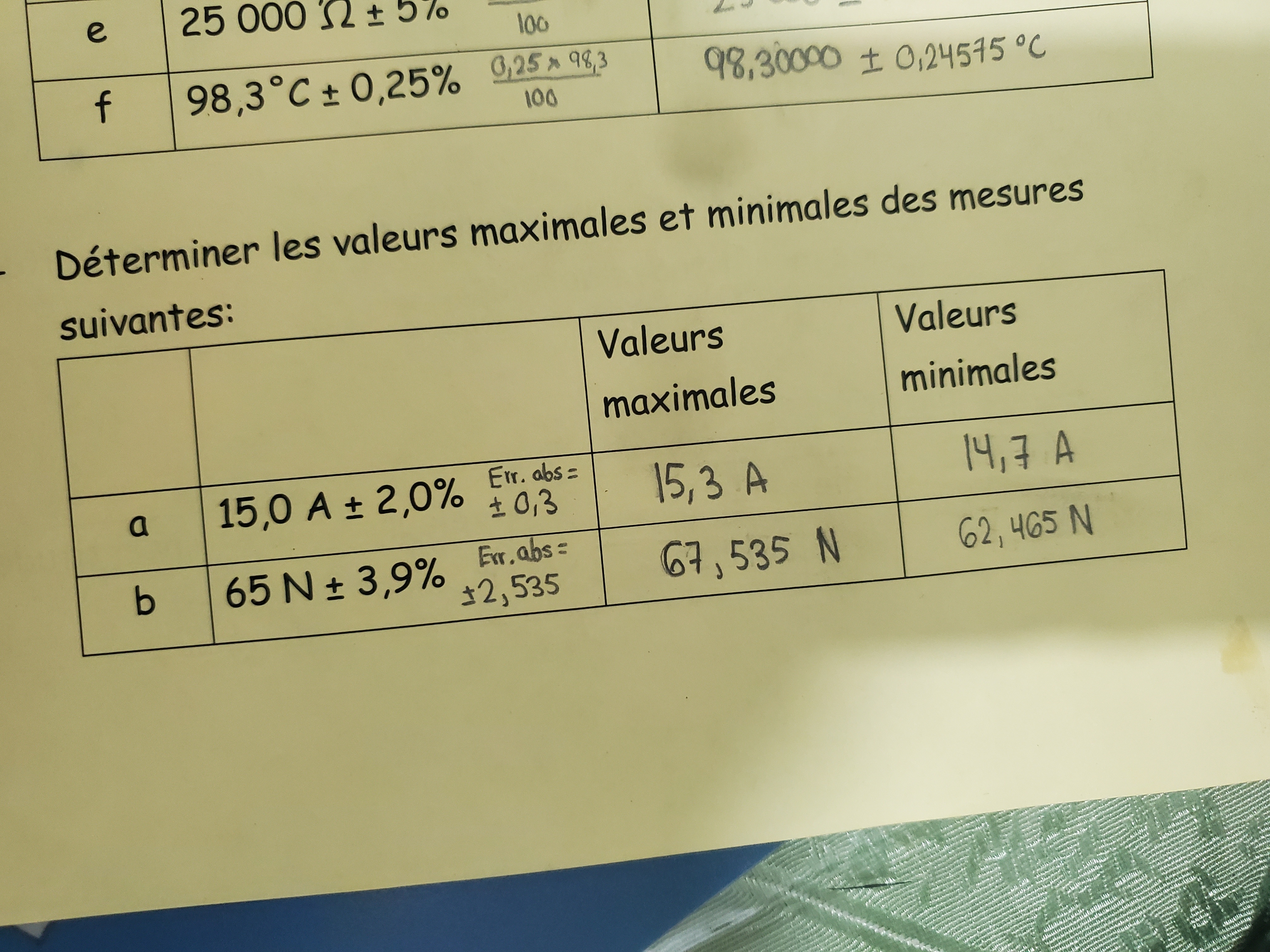
Secondaire 5 • 1aBonjour,
Je ne comprends vraiment pas comment faire ce genre de calcul d'incertitude. J'ai regardé les vidéos Alloprof mais cela ne m'a pas aidé..Merci!
-
Vérifiée par Alloprof
Postsecondaire • 1aBonjour,
est-ce qu'il serait possible d'avoir une explication sur la différence entre le lavage et le conditionnement d'un instrument en laboratoire?
merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aUne dernier question svp et c'est la plus importante aidez moi svpJe regarder des fichiers sur alloprof mais j'ai pas trop compris car moi j'ai transformé l'erreur relative en erreur absolue et après ça j'ai fais mes calculs mais je trouve que mes nombres contiennent beaucoup trop de chiffre et mon prof a dit ce que j'ai fais n'est pas bon alors pouvez vous me dire pk c'est pas bon je ne trouver mon erreur svp
-
Vérifiée par Alloprof
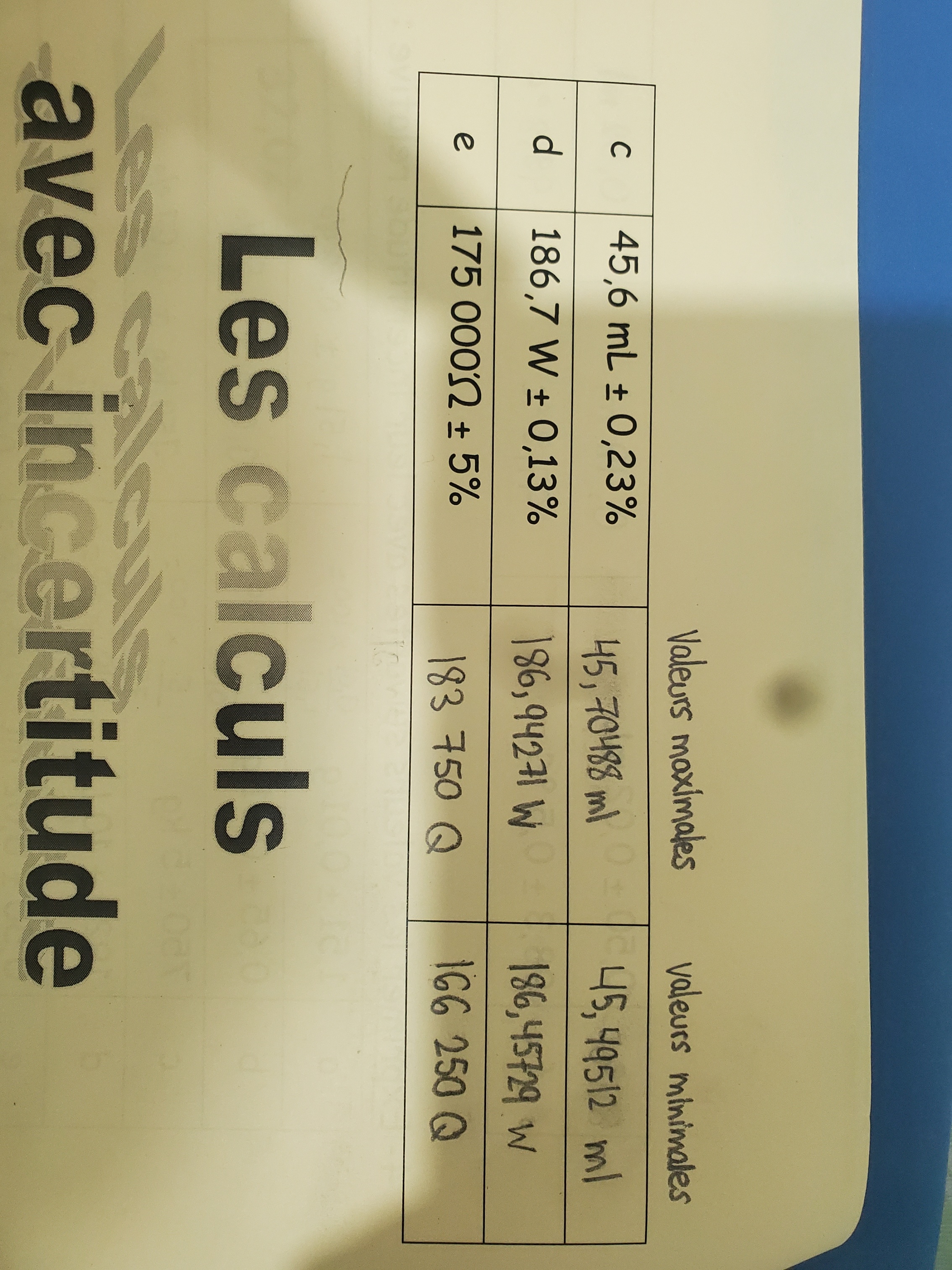
Secondaire 5 • 1aBonjour le numero 5 me cause beaucoup de problème
Je sais pas vraiment quoi faire j'ai fais quelque chose mais cela ne m'a pas l'air d'être correct genre je sais pas si je dois ajouter tous ces 0 dans les meures ou non comme j'ai ajoutée tellement de 0 dans la mesure où bien est ce que je fais qu'arrondir l'erreur absolue?
-
Vérifiée par Alloprof
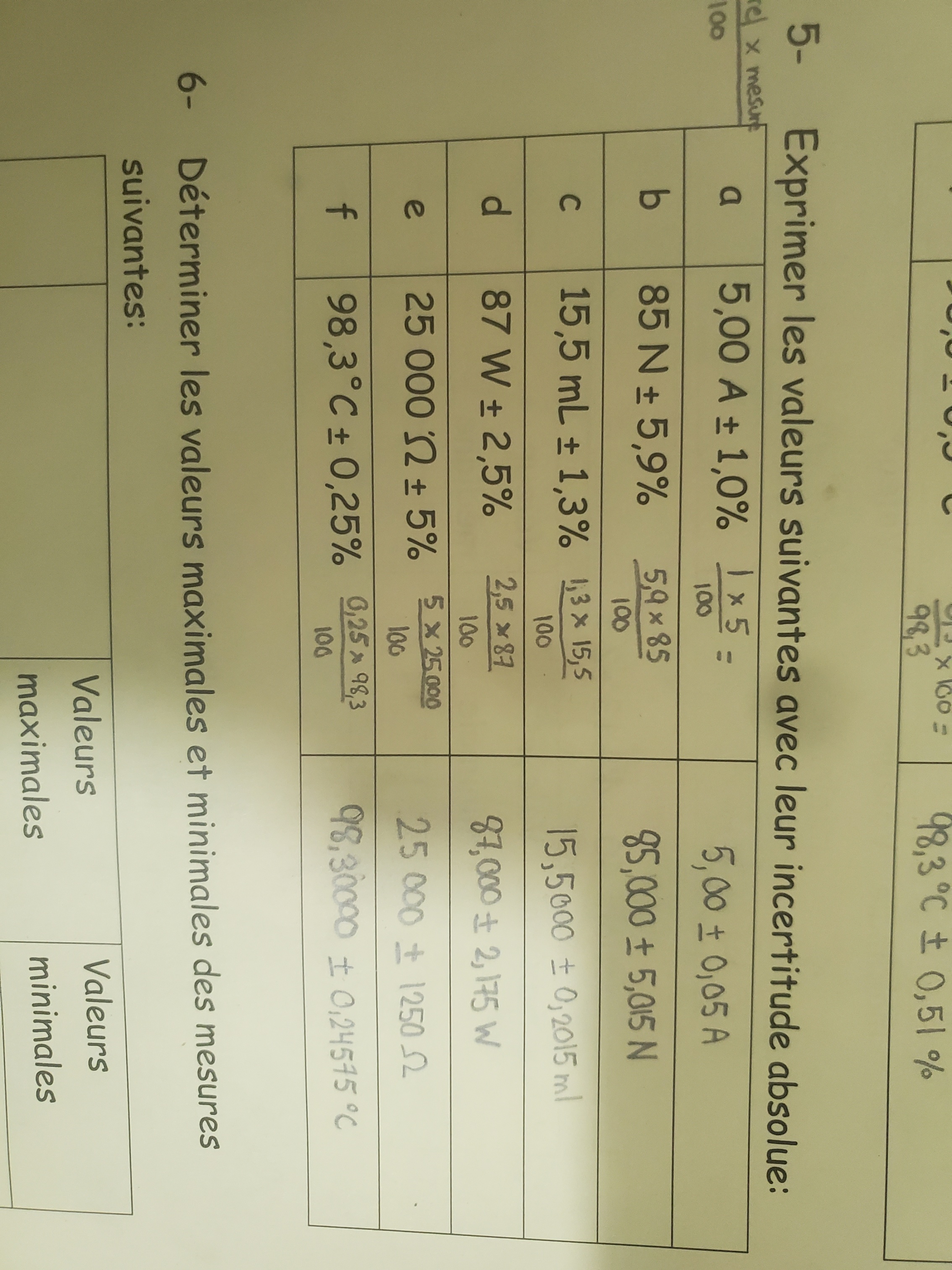
Secondaire 5 • 1aJ'ai une autre questionDans ce numéro, dans le c) et e) j'ai ajouté plusieurs 0 dans la mesure comme le 26.5 je l'ai transformé en 26.500 alors est ce que je dois faire ça?
-
Vérifiée par Alloprof
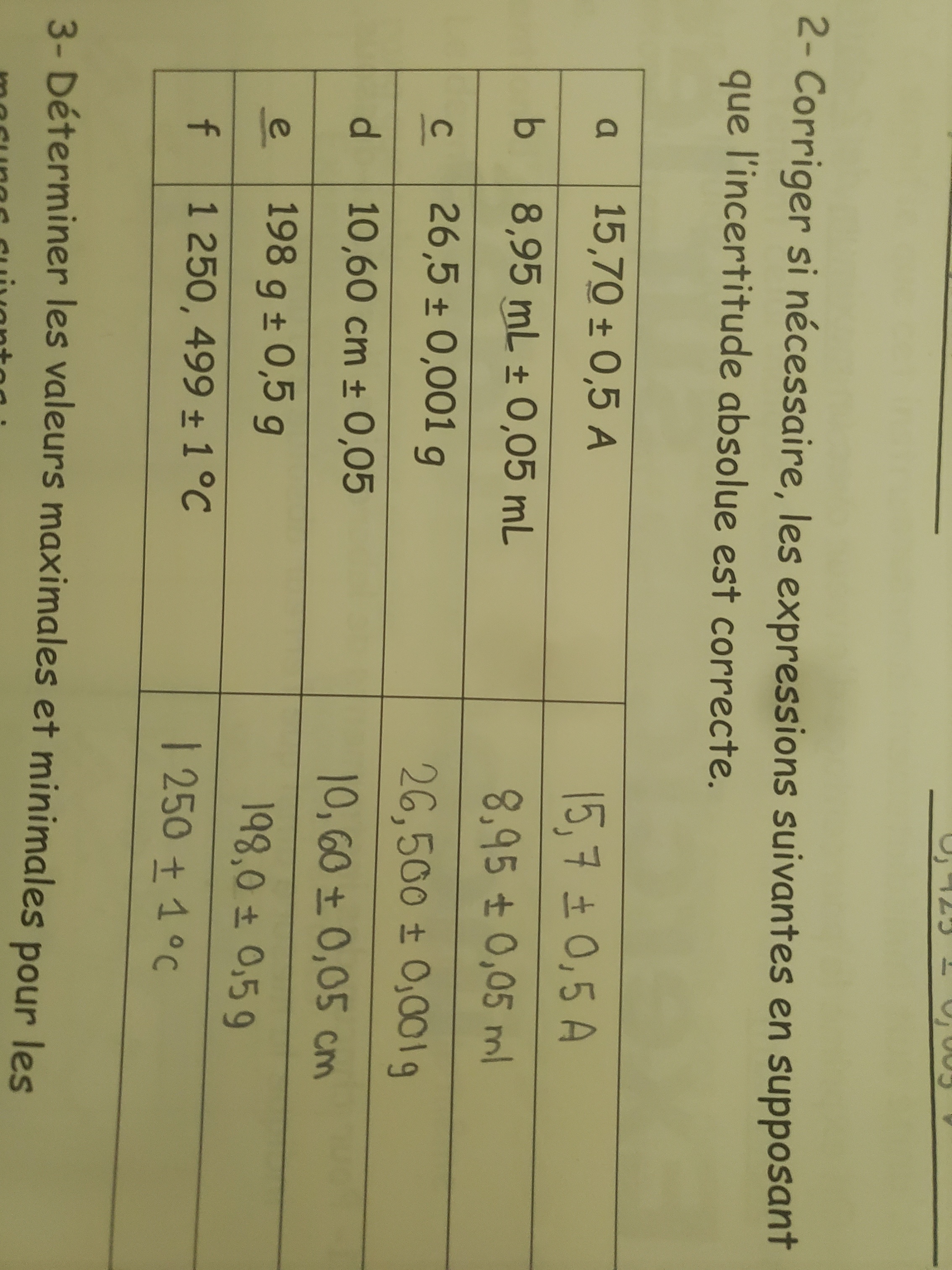
Secondaire 5 • 1aBonjour c'était mon premier cours en chimie aujourd'hui et j'ai beaucoup de questions :Pour ce numéro est ce que c'est ça l'erreur absolue comme dans le premier j'ai mis 0.05 puisque l'incertitude est sur le dernier chiffre et dans le cas du premier c'est sur le chiffre 2 alors c'est vraiment ça les erreurs absolues ?
-
Vérifiée par Alloprof
Secondaire 4 • 1aSalut, J'aimerai apprendre comment placer les électrons sur les couches électroniques...Je suis capable de les placer jusqu'à 8 sur la 3ième couche, mais après ça je sais que la méthode est différente et je ne la connais pas...(Par exemple, pour un atome qui a 19 protons.) Je suis allée voir la page du modèle atomique simplifié (sur Alloprof) et cela ne m'a pas aidée...
-
Vérifiée par Alloprof
Secondaire 5 • 1ameci pour nous édé
montre le a tout le monde
je veus 100 explication
svp
-
Vérifiée par Alloprof
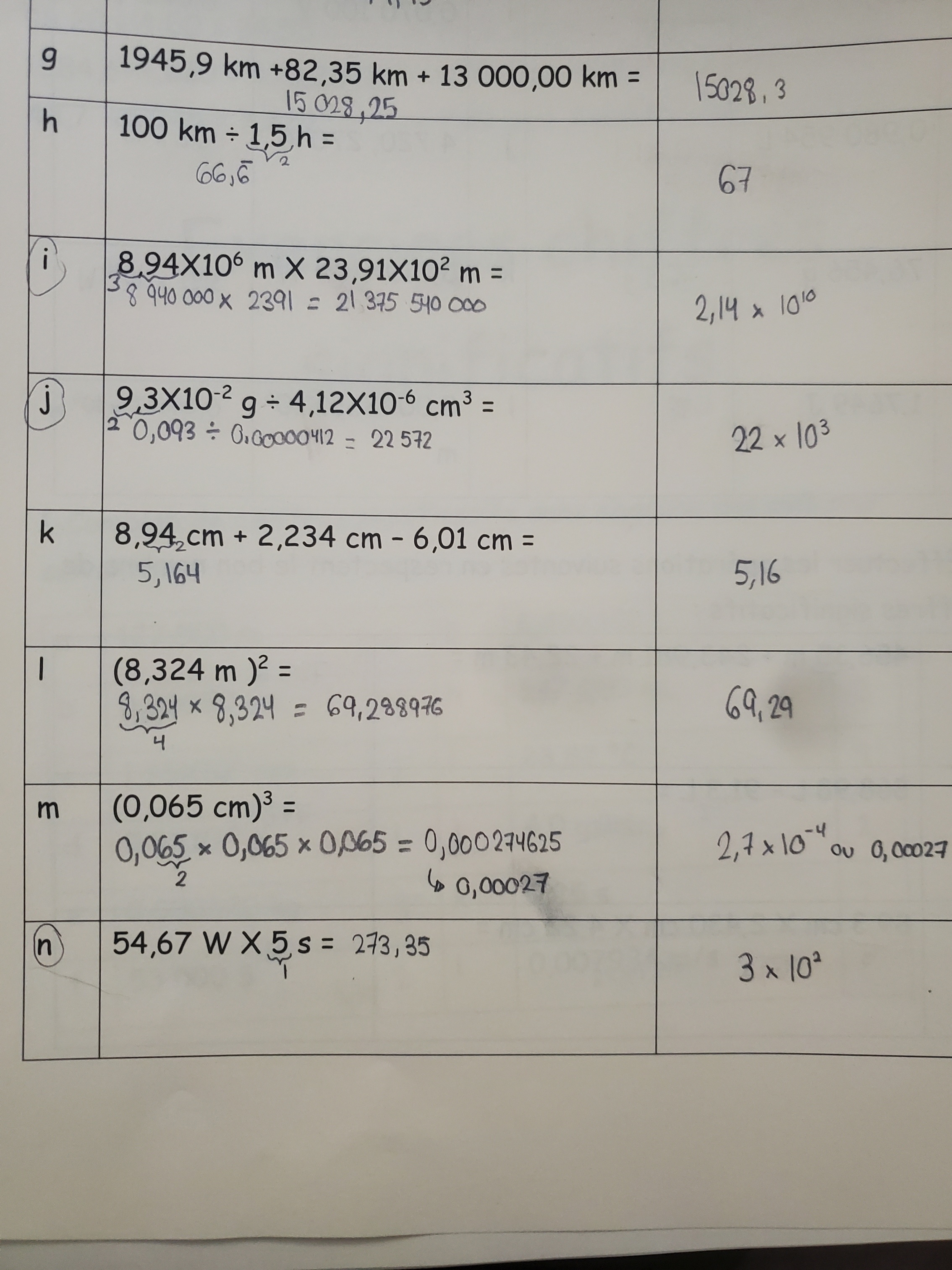
Secondaire 5 • 1aPouvez vous m'aider pour le i) et le j)
Il faut effectuer les opérations suivantes en respectant le bon nombre de chiffres significatifs
Je crois que j'ai pas bien fais le i et le j
-
Vérifiée par Alloprof
Postsecondaire • 1aBonsoir je n’arrive pas à répondre à cette question,
la superficie d’un objet est de 4ft 3 in par 14 in, quelle est son aire en cm2?
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aSalut ici je ne comprends pas pour vos chiffres significatifs comment vous avez fait, par ex dans les 1. vous obtenez 8.90 ce qui est bon car 12.3 a 3c.s mais en reponse finale vous n en mettez que 2 ? de meme pour le 2. il y a 240.0 avec 4 cs au lieu de 3 vu que 20.0 x 12.0 = possede 3 c.s et pas . Aussi, la réponse en que contient 2... ? je comprends pas trop pourquoi ? c est quelle regle des c.s ? merci bcp