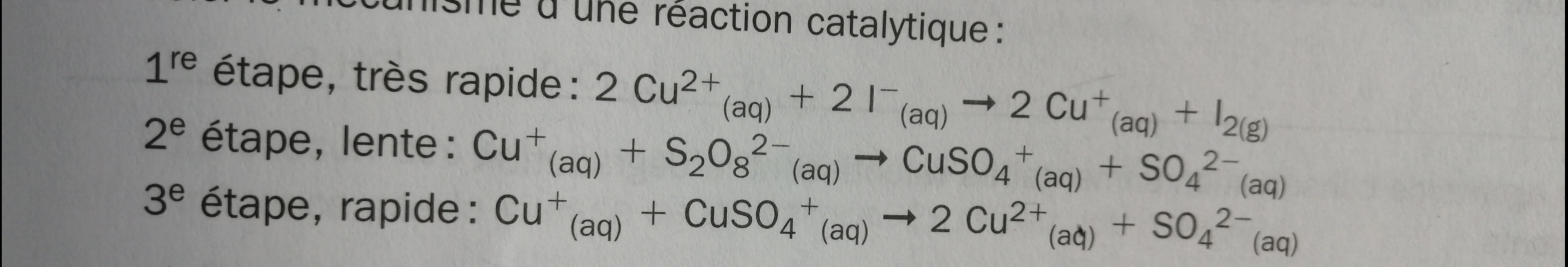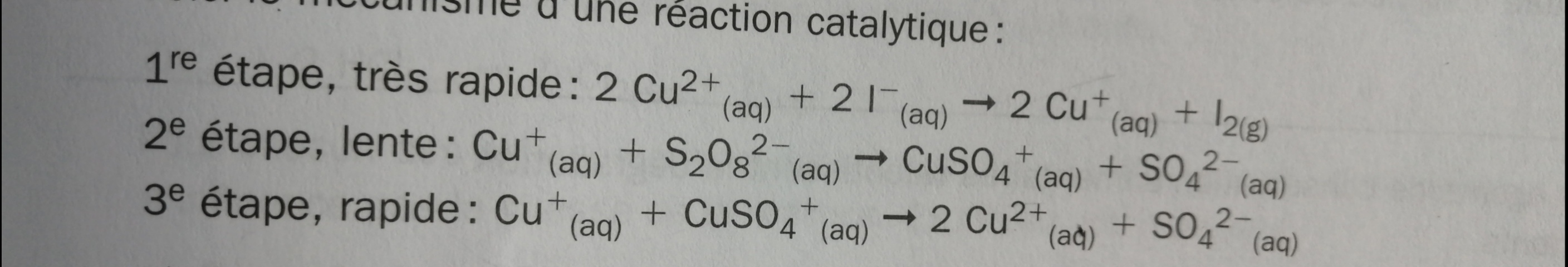Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 3aComment est-ce qu’on fait pour convertir une capacité massique thermique qui est en kelvin en celsius?
-
Vérifiée par Alloprof
Secondaire 5 • 3aComment je peut faire pour trouver la vitesse d’une réaction en ayant le nombre de mole finale et initiale et le temps. Lors de mon labo la température change… Est ce que ça va affecter mes calculs ou non ?
-
Vérifiée par Alloprof
Secondaire 5 • 3aSalut! J'ai une question pour les chiffres significatifs. Dans ma multiplication, mon nombre avec le moins de chiffres significatifs est 4. Mais ma réponse au total donne 483,6720...
Quelle serait donc ma réponse? 300 ou 342 ou je me fis à mon deuxième chiffre avec le moins de chiffres significatifs?
Merci pour l'aide
-
Vérifiée par Alloprof
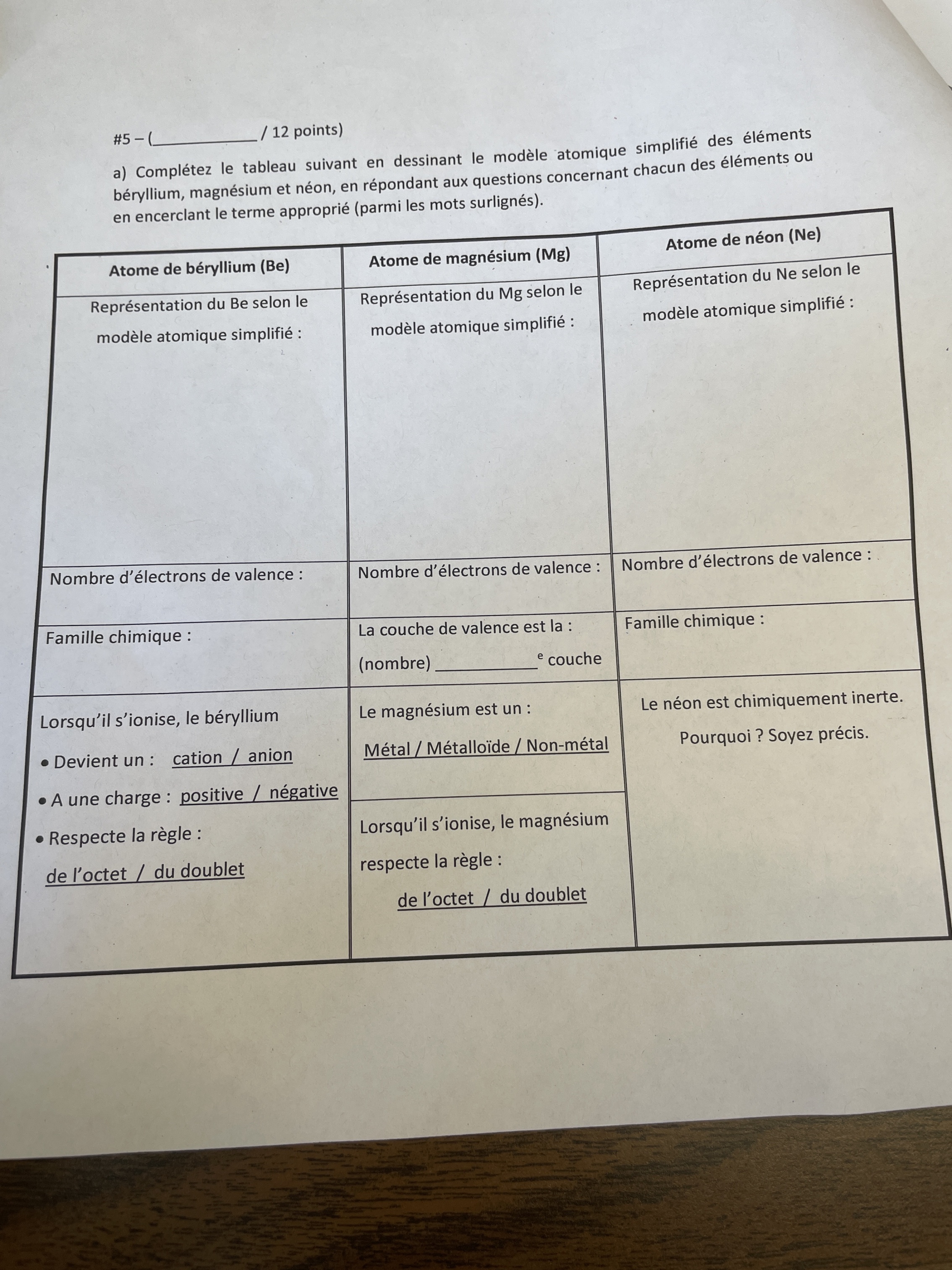
Secondaire 4 • 3aSvp aidez moi avec ce numéro. C’est urgent svp merci beaucoup
-
Vérifiée par Alloprof
Secondaire 4 • 3aSvp aidez moi avec le numéro 3
-
Vérifiée par Alloprof
Secondaire 4 • 3aDémontrer une démarche claire a fini d’identifier la charge du manganèse dans les composés suivants:
MnBr7
Mn3P4
Mn2(Cr04)3
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour je voulais savoir, les dissolutions sont des réactions physiques, mais les dissolutions ioniques? Ce sont des réactions physiques (car c'est une dissolution) ou chimique (car il y a un bris de lien chimique)?
ex. KNO3 (s) + H20 (l) --> K+ (aq) + NO3- (aq)
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour je voudrais savoir la capacité thermique massique de la paraffine C25H52 est de combien?
J’en ai besoin pour un calcul d’énergie et je ne la trouve nulle part!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je suis en secondaire 5 et je dois écrire une hypothèse sur la vitesse de réaction seulement, je n’ai pas compris le laboratoire et je ne sais pas comment m’y prendre pour écrire une bonne hypothèse, anticipations et comparer les expériences. Nous avons comme consigne de parler de la théorie (vitesse de réactifs et produits, stœchiométrie, vitesse instantanée et générale et collisions efficaces) mais en contexte de laboratoire. Pour contexte, nous avons mélangés du Mg et du H2. Le Mg étant sois en poudre ou en ruban (soit de 0,7M ou de 1M) donc au total nous avons fais 4 expériences. Pouvez-vous m’aider à me donner la direction pour ce laboratoire.
-
Vérifiée par Alloprof
Postsecondaire • 3aVous avez une solution aqueuse de Ca(NO3)2 ayant un pourcentage masse/volume de 5,2 %m/V et une masse volumique de 1,125 g/mL.
Calculez la concentration molaire volumique (mol/L) de cette solution.
-
Vérifiée par Alloprof
Postsecondaire • 3aBonsoir,
J'ai bien aimé la vidéo que vous m'avez proposé. (https://www.alloprof.qc.ca/zonedentraide/discussion/60306/question/p1) En auriez-vous d'autres?
Merci beaucoup et bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Secondaire 4 • 3aOn me dit de calculer la massa de carbonate de calcium (CaCO3) qui résulterait du mélange de 25 ml de dichlorure de calcium (CaCl2) à 0.5mol/L.
CaCl2 + Na2CO3 → CaCO3 + 2 NaCl
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonjour
On me dit de calculer la massa de carbonate de calcium (CaCO3) qui résulterait du mélange de 25 ml de dichlorure de calcium (CaCl2) à 0.5mol/L.
-
Vérifiée par Alloprof
Postsecondaire • 3aSabrina fait chauffer un solide inconnu de 25,625 g. Lorsque le solide atteint une température de 85,0 C, elle le dépose dans un thermos contenant 225,0 g d’éthanol (c = 2,46 J/g•C), à une température de 20,0 C. La température de l’éthanol s’élève alors jusqu’à 22,6 C. Si l’on considère qu’il n’y a pas eu de perte d’énergie dans l’environnement, calculez la capacité thermique massique du solide inconnu.
-
Vérifiée par Alloprof
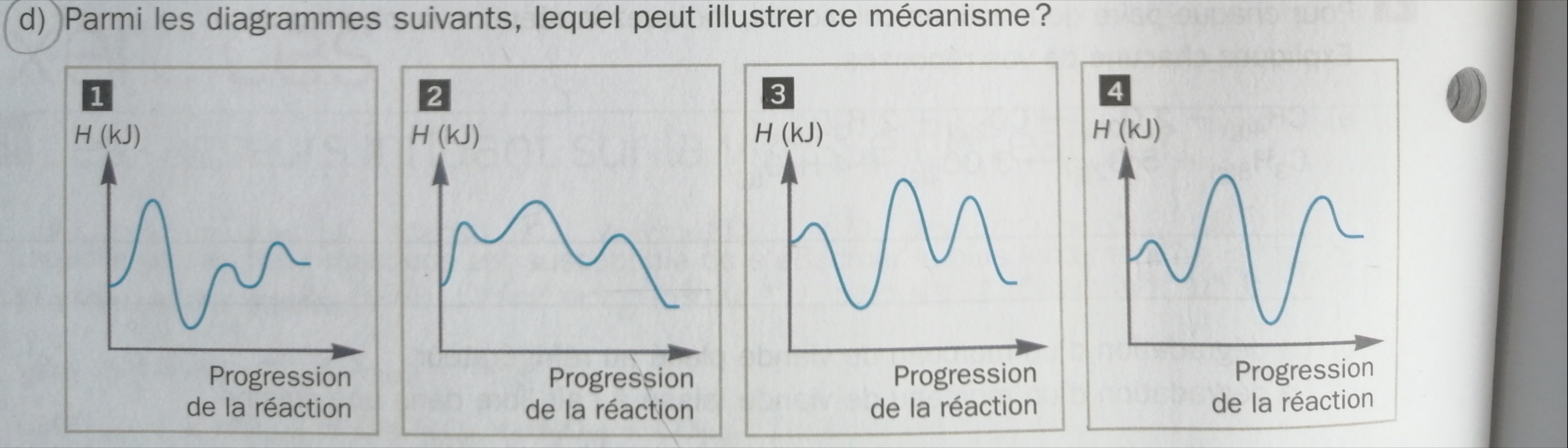
Secondaire 5 • 3aBonjour Alloprof! Pourquoi c'est le diagramme 3 qui représente le mieux la réaction et non le 2 ou le 4? Je n'ai pas compris pourquoi c'est le diagramme 3 qui correspond le mieux à la réaction catalytique sachant que pour le diagramme deux et 4, c'est la réaction du milieu qui est la plus lente aussi.
-
Vérifiée par Alloprof
Secondaire 5 • 3abonjour vous pouvez m’aidez s’il vous plait pour cette question merci d’avance.
-
Vérifiée par Alloprof
Postsecondaire • 3aBonsoir,
Petite question : le spectre de raies s'applique-t-il uniquement aux atomes et aux molécules à l'état gazeux ou à tous les atomes et à tous les molécules?
Merci beaucoup et bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Secondaire 4 • 3aPourquoi la chaux(CaO) se comporte comme une base dans la neutralisation acido-basique ?
-
Vérifiée par Alloprof
Postsecondaire • 3aBonsoir,
J'aimerais savoir pourquoi c'est la b qui comporte la longueur d'onde la plus courte dans cette question : laquelle des deux transitions suivantes permettrait, pour un atome d'hydrogène, l'émission de la radiation comportant la longueur d'onde la plus courte? a) ni = 5 --> nf = 3 et b) ni = 4 --> nf = 2.
Merci beaucoup et bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je suis présentement en train de faire ma chimie de secondaire 5 et je ne comprend pas la question suivante :
Calculez la masse de réactif nécessaire pour recueillir 40 ml de gaz aux conditions ambiantes? Faites vos calculs pour le magnésium et pour l’aluminium.Note : À température ambiante et à pression normale, une mole de gaz occupe un volume de 24,5 L.Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aun calorimètre contient 60,0 mL d'eau dont la température initiale est de 25 degre C et que 85,0% de la chaleur est récupérée par ce liquide, quelle sera la température finale de l'eau du calorimètre
-
Vérifiée par Alloprof
Postsecondaire • 3aBonsoir,
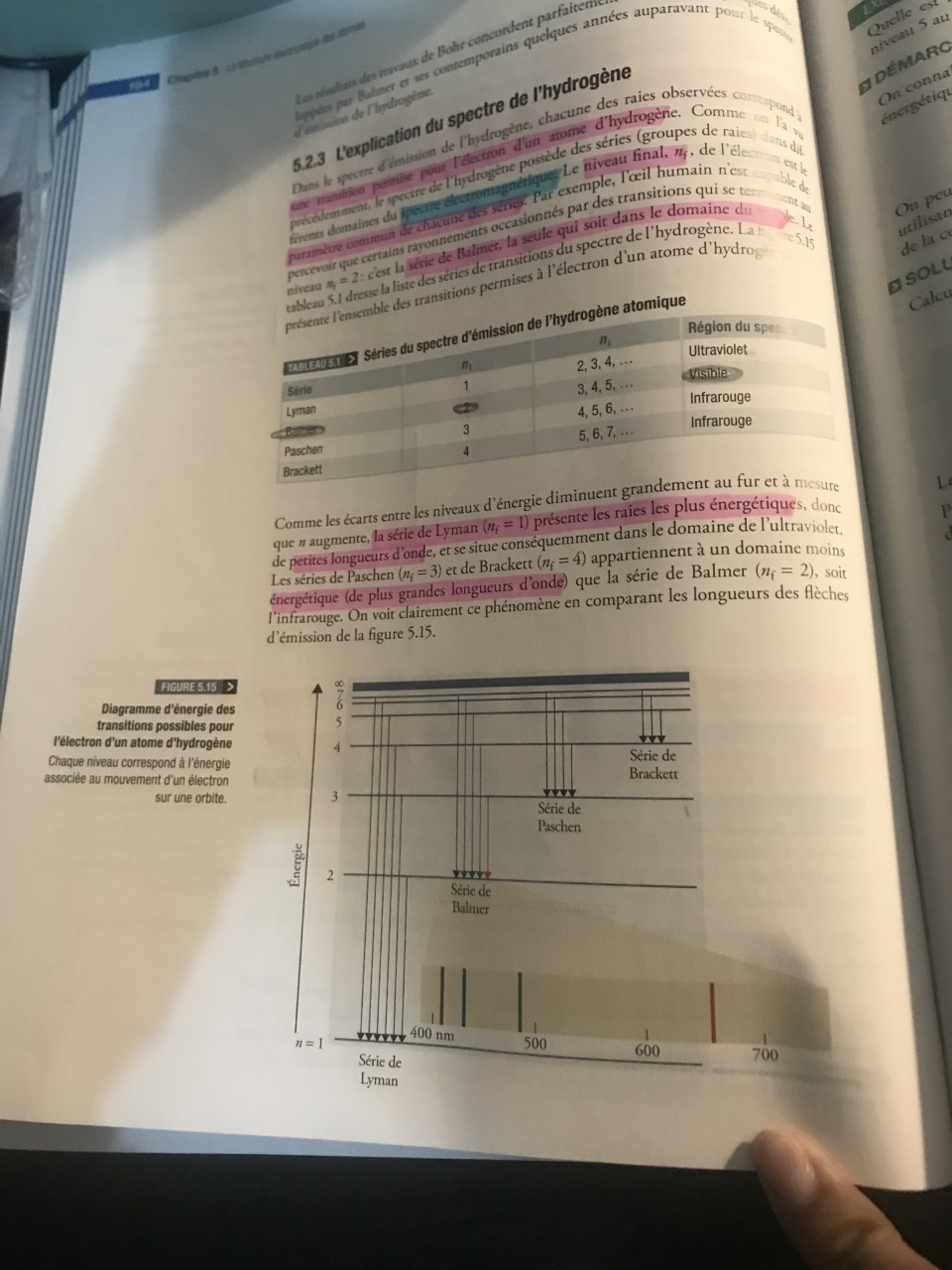
J'aimerais savoir ce qui est à comprendre du diagramme d'énergie des transitions possibles pour l'électron d'un atome d'hydrogène.Voici ce que j'ai compris.
La série de Lyman qui est la plus énergétique comporte des longueurs d'ondes plus petites que les séries de Paschen et de Brackett qui ont des longueurs d'ondes plus longues que celle de Balmer qui comporte certaines radiations visibles.
Merci beaucoup et bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
j'ai un laboratoire à faire dans lequel nous devons émettre une hypothèse sur la question suivante: Parmi trois substances solides (KNO3, KOH, NH4Cl) , déterminer celle qui est la plus efficace pour produire une compresse froide.
Je ne sais pas quoi dire ni comment l'expliquer.
merci de votre aide!
-
Vérifiée par Alloprof
Postsecondaire • 3aBonsoir,
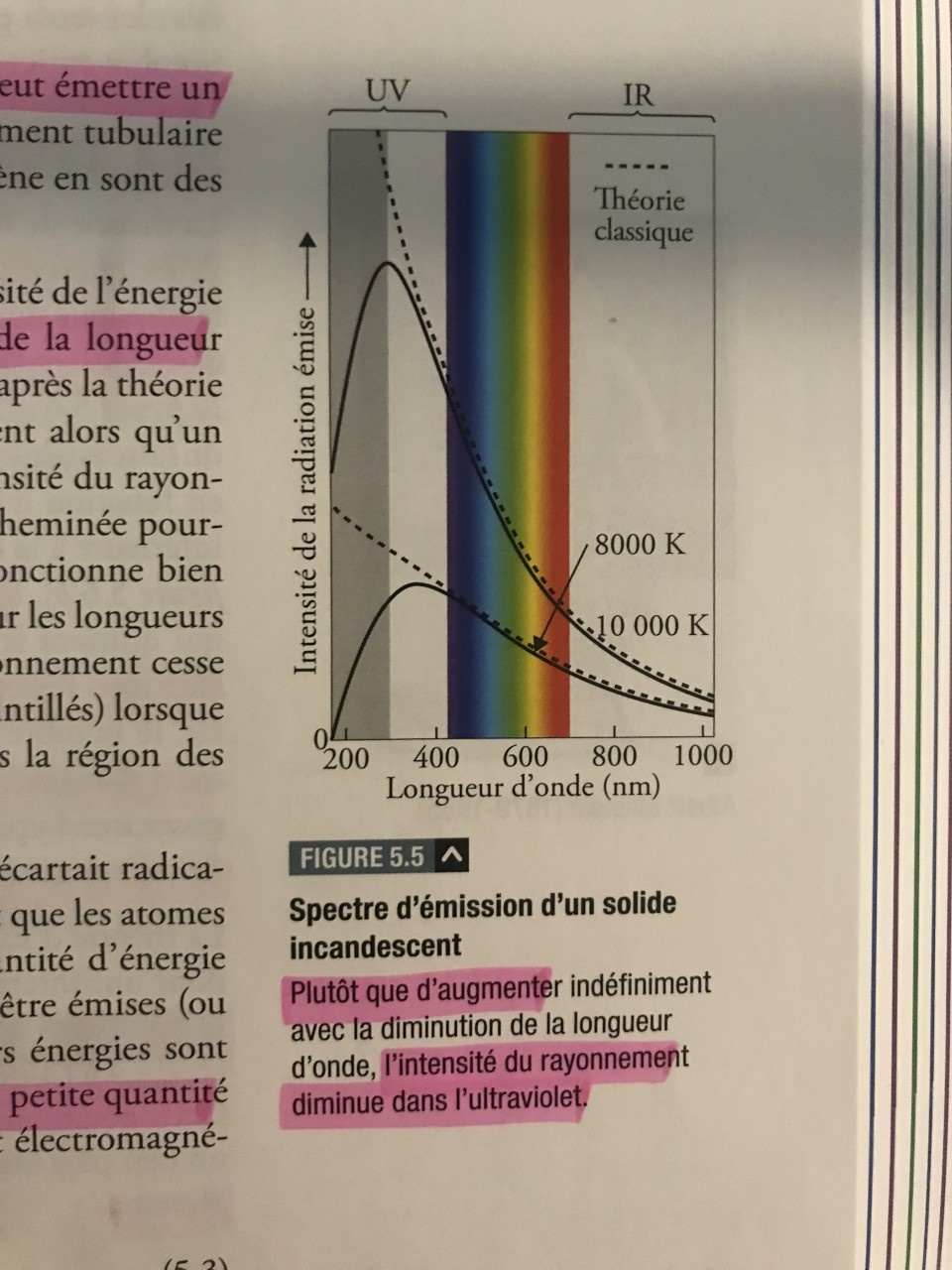
Est-ce que quelqu'un pourrait svp m'expliquer ce qu'il se passe dans ce graphique?Merci et bonne soirée! ;)
OrAutonome2754
-
Vérifiée par Alloprof
Postsecondaire • 3aBonsoir,
J'aimerais savoir comment on détermine la longueur d'onde la plus courte ainsi que la longueur d'onde la plus longue si on nous donne l'énergie cinétique des électrons éjectés.
Merci beaucoup et bonne soirée! ;)
OrAutonome2754
Contexte : Une surface métallique est irradiée avec des faisceaux de trois longueurs d'onde différentes, lambda1, lambda2 et lambda3. Les énergies cinétiques des électrons éjectés sont les suivantes : lambda1 : 7,2 x 10^-20 J ; lambda 2 : approximativement 0 J ; lambda 3 : 5,8 x 10^-19 J. Déterminez le faisceau qui a la longueur d'onde la plus courte et celui qui a la longueur d'onde la plus longue.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour!
Dans mon cahier de théorie, il est écrit que: "la vitesse de réaction pour les différents réactifs ou pour les produits est équivalente pour une même réaction". Mais il y est aussi écrit que: "la vitesse dépend de la proportion de la substance choisie (réactif ou produit) dans une réaction donnée. Plus précisément, cette proportion est définie par le coefficient qui précède chacune des substances dans l'équation chimique balancée."
J'aurais besoin d'explications, je ne comprends pas comment c'est possible.
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aAllo! Je ne suis pas sure des étapes que je dois faire pour avoir mon résultat en mol/s, dans la section calculs. Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir,
pouvez-vous m’expliquer c’est quoi la différence entre le bilan énergétique et la variation d’enthalpie SVP? Ou les deux n’ont pas de différence…
merci en avance
-
Vérifiée par Alloprof
Secondaire 5 • 3ala question me demande de trouver la vitesse moyenne du magnésium mais je ne sais pas comment aider moi svp
-
Vérifiée par Alloprof
Secondaire 5 • 3aJ’ai de la difficulté à trouver comment résoudre ce problème. Logiquement je suis tenté de trouver la masse de chaque molécule, mais ça me parait trop simple…