Matières
Niveaux
Le pH, abréviation de potentiel hydrogène, est une mesure qui permet de déterminer le degré d’acidité ou de basicité d’une solution. Le pH n’a pas d’unité de mesure.
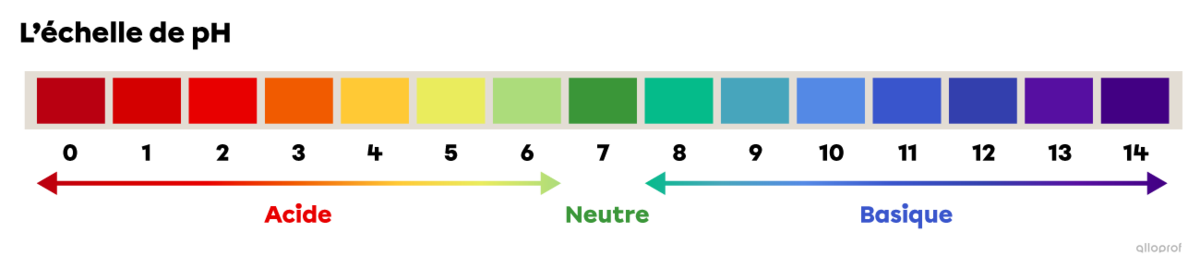
L’échelle de pH permet de comparer le caractère acide, neutre ou basique des solutions. L’échelle de pH varie généralement de 0 à 14.
Un indicateur acidobasique est une substance qui a la propriété de changer de couleur en fonction du pH.
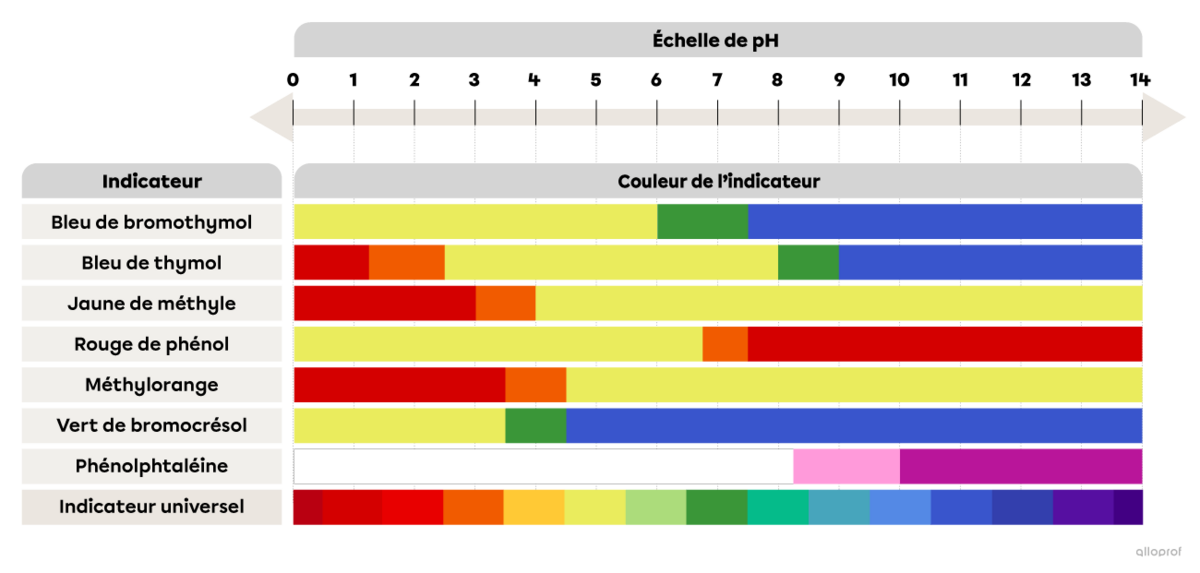
La couleur de quelques indicateurs acidobasiques en fonction du pH
La phénolphtaléine est un indicateur qui peut être utilisé pour déterminer si une solution est basique. Il suffit d’en déposer quelques gouttes dans la solution en question et on observe s’il y a un changement de couleur.
Si la phénolphtaléine reste incolore, on ne peut pas déterminer si la solution est acide (pH inférieur à 7), neutre (pH égal à 7) ou basique (dans ce cas, pH entre 7 et 8,2).
Si l’indicateur devient rose, cela signifie que le pH de la solution se situe entre 8,2 et 10 et que la solution est basique.
Si l’indicateur devient fushia, cela signifie que le pH est supérieur à 10 et que la solution est basique.
En bref, si la phénolphtaléine devient rose ou fushia lorsqu’elle est mélangée à une solution, cette solution est nécessairement basique.
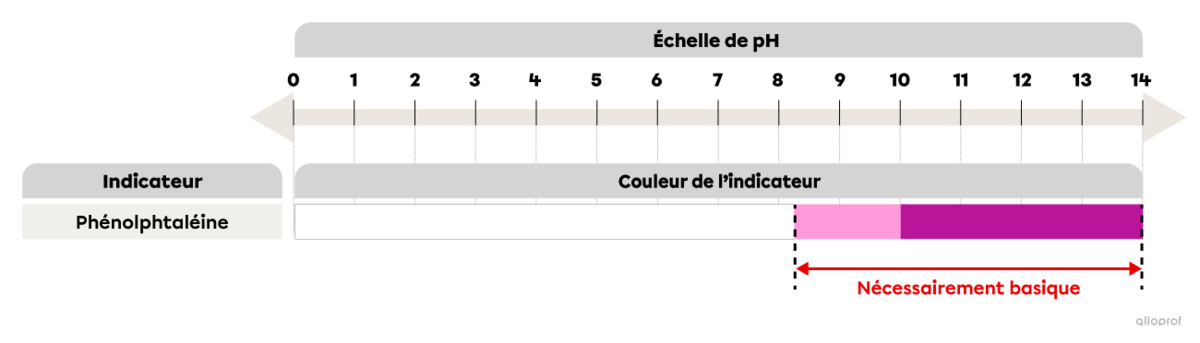
La couleur de la phénolphtaléine en fonction du pH
Dans une éprouvette remplie de jus de citron de pH 2, on ajoute quelques gouttes d’un indicateur acidobasique : le bleu de thymol. On s'assure que le bleu de thymol soit bien mélangé avec le jus de citron et on observe le changement de couleur.
En te référant à l’image La couleur de quelques indicateurs acidobasiques en fonction du pH, détermine quelle sera la couleur du bleu de thymol après avoir été mélangé avec le jus de citron.

L’ajout de bleu de thymol dans du jus de citron
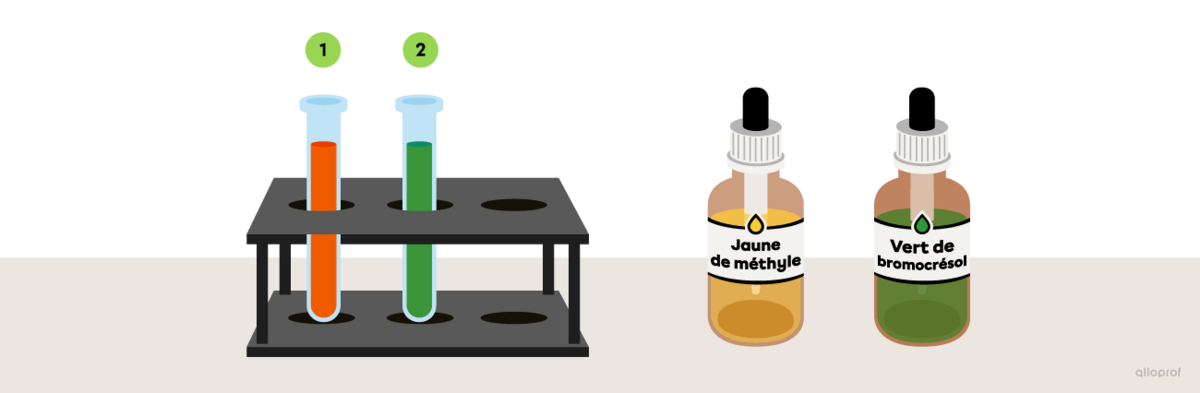
On ajoute quelques gouttes de jaune de méthyle à une substance inconnue et la solution devient orange. Dans une deuxième éprouvette, on ajoute du vert de bromocrésol et la solution inconnue devient verte.
En te référant à l’image La couleur de quelques indicateurs acidobasiques en fonction du pH, détermine dans quel intervalle se situe la valeur du pH de cette substance inconnue.
La réaction du jaune de méthyle et du vert de bromocrésol avec une substance inconnue