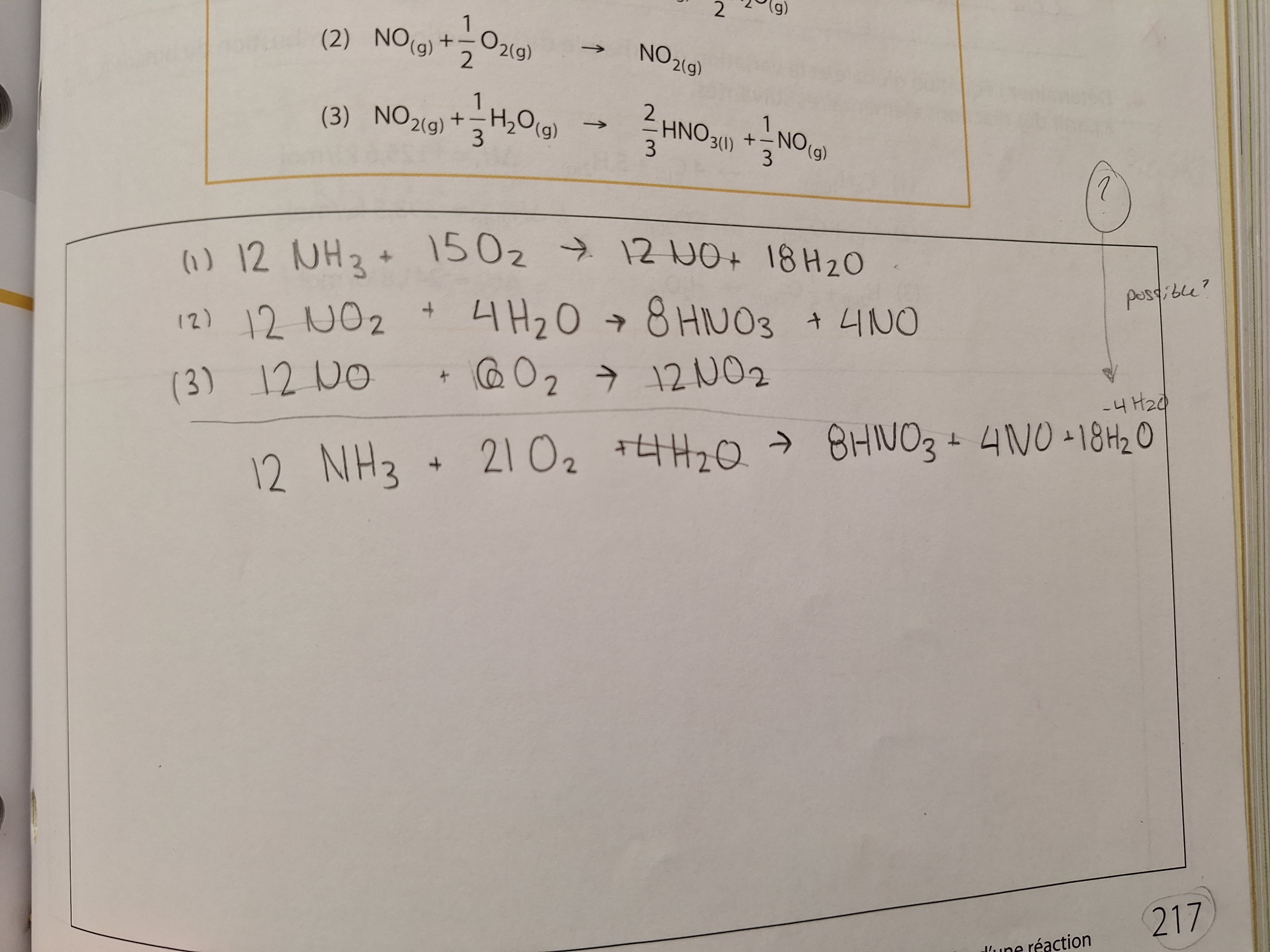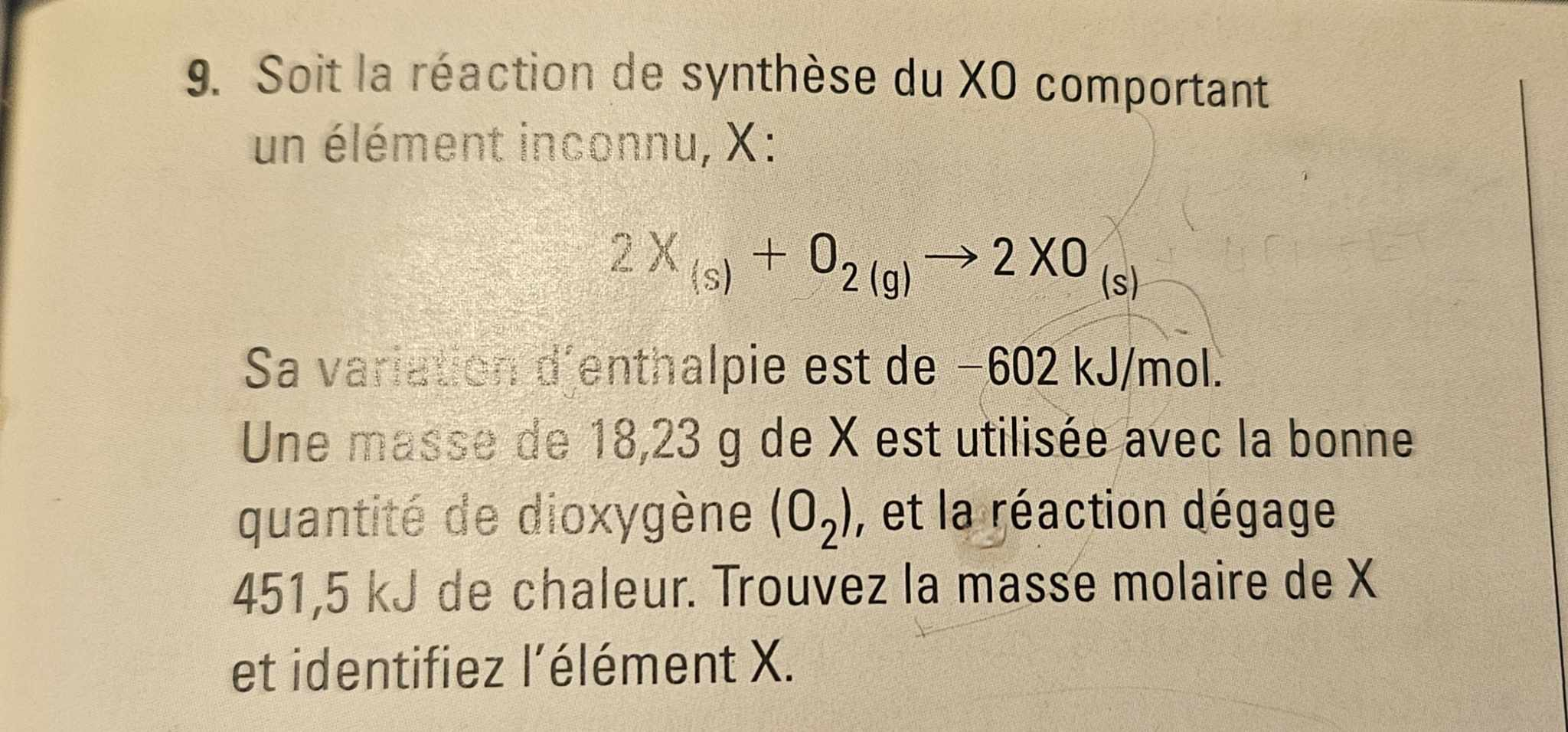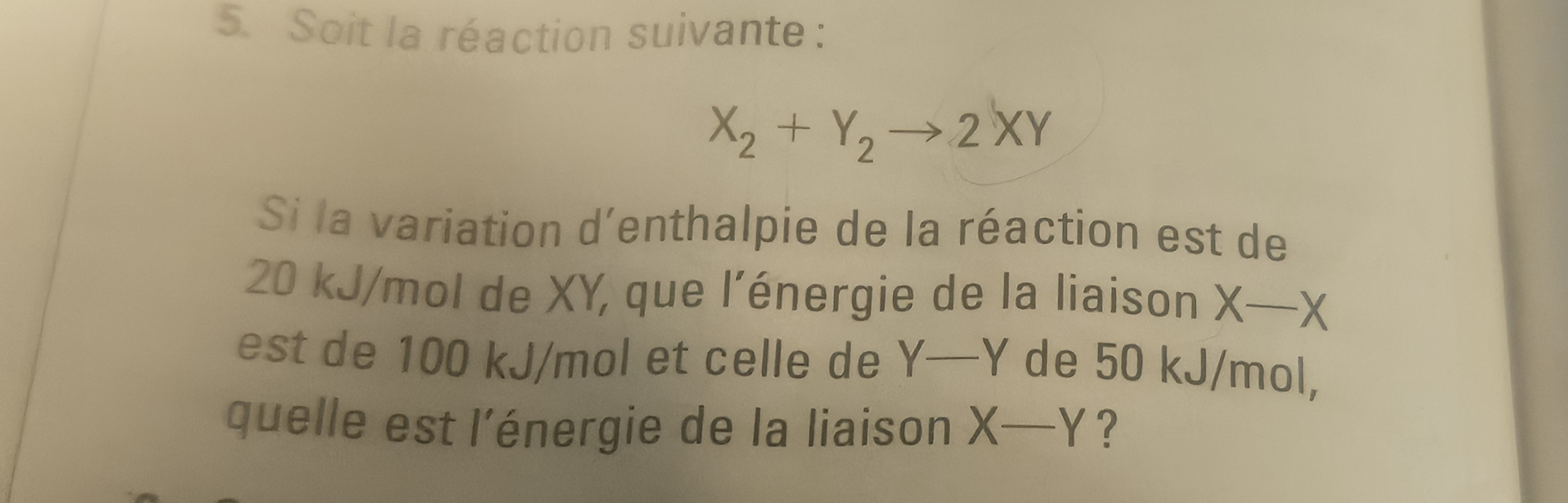Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 1aCe que je comprend c'est que lorsque une même substance précédé du même coefficient stochio sont de chaque côté de la flèche, ça s'annule. Mais est ce que si ce n'est pas le même coefficient je peut soustraire les coefficient.Dans cet exemple j'ai eu la bonne réponse mais je comprend pas alors on a le droit de soustraire même si coefficent est différent, car j'ai fait 18h2o - 4h2o. Est ce que c'est correct? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour , j'ai une question pour chimie de secondaire 5
existe t'il une relation entre la profondeur en mètre et l'unité de mesure atm?
faut-il les convertir en mmhg?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Pourriez-vous m’expliquer se numéro là.
Mercii!!
-
Vérifiée par Alloprof
Secondaire 5 • 1aPouvez-vous m`expliquer une équation thermique globale à partir d`équation intermédiaire selon la loi de Hess? svp
-
Vérifiée par Alloprof
Secondaire 5 • 1arebonjour, donc si je comprend bien, l'énergie d'activation c'est l'énergie qui va être barber par les réactifs pour qu'ils puissent ce briser et par la suite former le complexe activé et ensuite ils vont dégager de l'énergie pour former les produits?? Merci à L'avance!!
-
Vérifiée par Alloprof
Secondaire 5 • 1aRebonjour, par rapport à ma deuxième question, je ne comprenais pas trop c'est quand que l'énergie d'activation arrivais Merci à l'avance!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, j'espère que vous allez bien, nous sommes entraide voir la calorimétrie et il y a quelques chose que je n'arrive pas à comprendre, quand il y a une réaction qui arrive, est-ce que c'est genre les réactifs pour qu'ils puissent ce défaire, ils absorbent de l'énergie pour briser les liaisons donc l'énergie absorber vient de l'eau et ensuite, ils vont former un complexe activé qui est genre toutes les molécules sont là en un gros Group et ensuite pour reformer les produits, il font dégager de l'énergie et donc la calorimétrie ses de savoir avec l'eau si la réaction à absorber plus ou si elle a dégager plus?? Est-ce que mon raisonnement est bon?? Merci à l'avance!!
-
Vérifiée par Alloprof
Secondaire 5 • 1ac'est quoi la chaleur molaire d'une réaction?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir, pourquoi la résolution de ces deux questions sont contradictoires?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir! Merci beaucoup pour l'explicationhttps://www.alloprof.qc.ca/zonedentraide/discussion/116530/questionmais du coup, comme cela fonctionne pour un problème comme celui-ci? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir, merci beaucoup pour l'explication !https://www.alloprof.qc.ca/zonedentraide/discussion/116470/questionToutefois, je ne suis pas très sûre de comprendre. Je pensais que le 90,2kJ/mol était pour toute la réaction, donc 1mol de N2 absorberait 90,2kJ pour que la réaction se produise. Ainsi pourquoi ici avoir fait le 90,2 *2? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir, pourquoi on n'a pas directement utiliser 90.2 ici? Merci!(Numéro 5)
-
Vérifiée par Alloprof
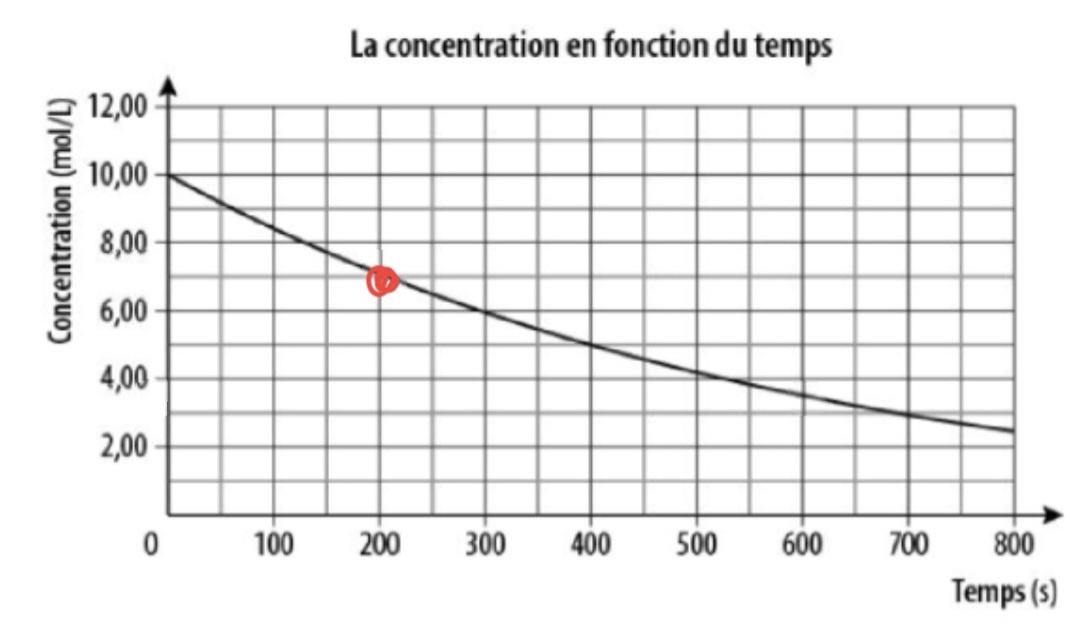
Secondaire 5 • 1aBonjour dans ce problème, je dois Calculez la vitesse instantanée à la 200 seconde, je sais que je dois tracer une tangente mais je sais pas où la placer exactement, je sais quelle doit etre parallele a la courbe et qu'elle a un point en commun avec la courbe et cest à 200 secondes mais je ne sais pas comment la tracer jai vu les fichiers sur alloprof mais je suis quand meme perdu donc est ce que cest possible que vous pussiez me montrer a quoi va ressembler la tangente sur la figure merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir! Pourquoi, vu que c'est dit par mol de XY, on a pas fait 20* 2?
Merci
-
Vérifiée par Alloprof
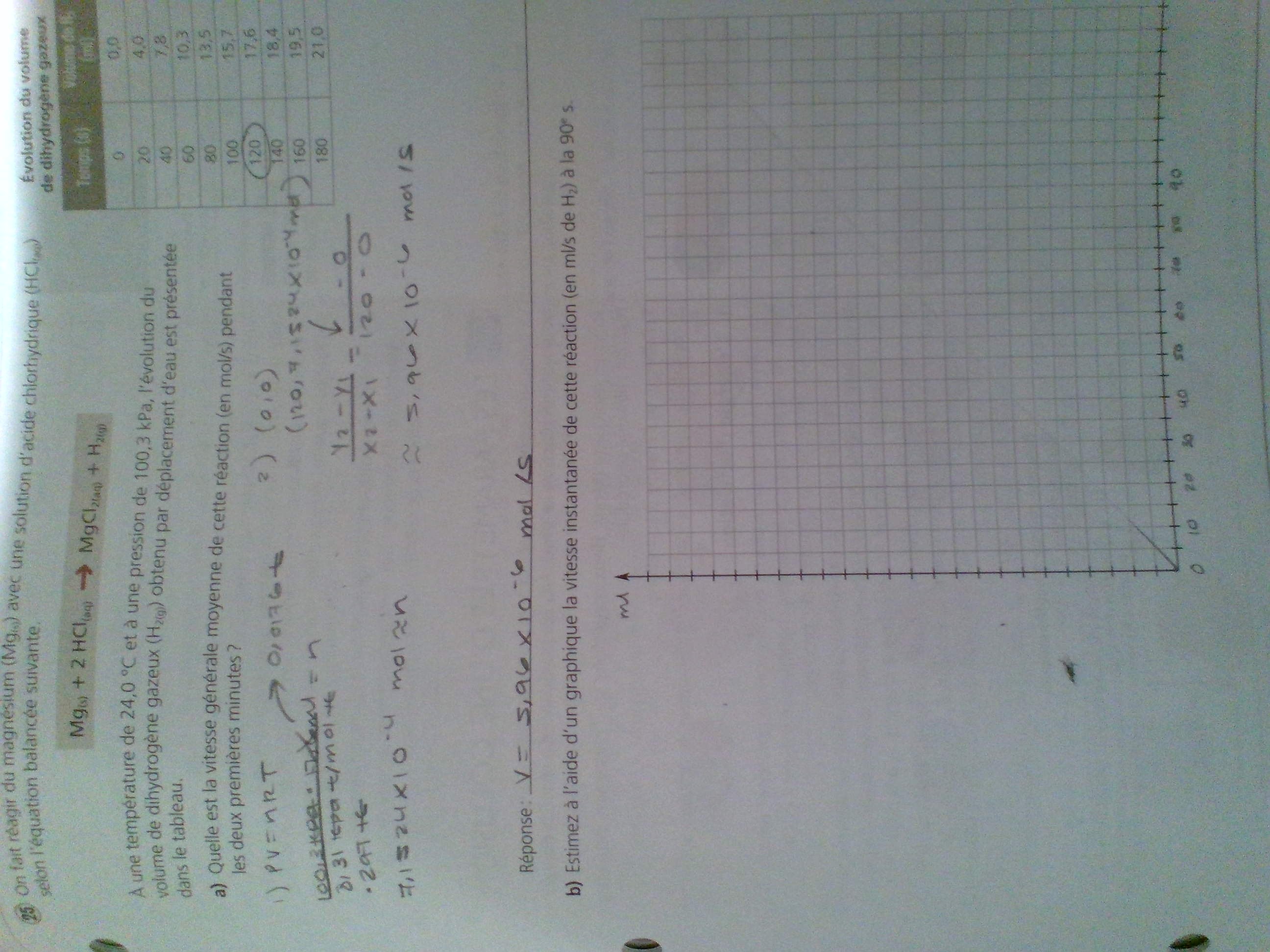
Secondaire 5 • 1aBonjour,
Je comprends pas cette question (la b)):
Je ne sais pas comment estimer la vitesse instantanée en général.:
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir merci beaucoup pour l'explication! Mais pourquoi ainsi on procède comme ça dans cette exercice https://www.alloprof.qc.ca/zonedentraide/discussion/116351/questionSi on a trouver que le bilan est -1016kj/mol, pourquoi dans le rapport on dit pas sur 3 mol si on a 3 mol d'eau dans l'équation balancée? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir. Je suis totalement perdu. Je ne comprend vraiment pas quand multiplier le ∆H. Tout les exercices sont contradictoires. S'il vous plaît, expliquer moi quand je doit multiplier...
Par exemple, pourquoi ici -64.3 n'est pas multiplier avec le 4? Cela m'a l'aide du recation de synthèse non?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aRebonsoir,
dans une equation thermochimique ou est - ce qu'on met la chaleur molaire dependemment si c'est une réaction endothermique ou exothermique?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir,
J'ai un laboratoire demain et j'aimerais savoir qu'elle est la précision d'un thermomètre. Est - ce +/- 1 degés celcius ou +/-0.5?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, la formation de buée sur le mirror d'une salle de bain, est-elle endo ou exothermique? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! En lien avec ceci: https://www.alloprof.qc.ca/zonedentraide/discussion/116126/question
La question était comme cela. Ainsi, je ne comprend pas pourquoi au premier ils ont diviser par 2 et dans le b) non. Et comment, avec les informations donner on sait quel des deux réactif on a diviser le ∆H?Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, j'aurais besoin de l'aide à savoir mon erreur!
Dans le corrigé de cette exercice, la réponse est de 66 fois plus grand mais moi je trouve seulement 6,6 fois plus grand!
-
Vérifiée par Alloprof
Secondaire 5 • 1aAllo! J'arrive pas à savoir quel type de réaction est :
Mg + 2HCl --- MgCl2 + H2
mercii
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir !
Je ne comprend pas le problème a ci-dessous.
-
Vérifiée par Alloprof
Secondaire 5 • 1aLorsqu'on a une valeur (ex: 5,78 g ) que l'on veut multiplier par un rapport ( ex: par 2 ), qu'arrive-t-il aux chiffres significatifs?
Dans mon exemple j'ai une valeur de 5,78 g d'acide oxalique dont je doit doubler, car je doit faire la réaction avec 5,78 g d'acide oxalique deux foix ( c'est un rapport non? ).
-
Vérifiée par Alloprof
Secondaire 3 • 1apour chimi les composer moleculer et ionique les ion et tous cet truc
-
Vérifiée par Alloprof
Secondaire 5 • 1aAllo!! je me demandais si quelqu'un pouvais m'aider avec les calculs de chaleur molaire et massique ?
-
Vérifiée par Alloprof
Secondaire 1 • 1aJ'ai besoin d'aide avec ça
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! En lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/116128/questionMerci beaucoup pour l'explication ! Toutefois, le fait que les valeurs théoriques sont prises à TAPN qu'elles peuvent varier si on change ces conditions parfaites, cela ne vient pas dire que cela n'est plus une variation d'enthalpie molaire? Puis, quand on parle de changement de température, voulons-nous dire que la transformation, par exemple, de la fusion de l'eau ce passe à TAPN ? (et on ne parle donc du point de fusion de 0 degrés)?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! En lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/116117/questionMerci pour l'explication! Toutefois, je ne suis pas sûre de comprendre, car je pensais que la variation d'enthalpie standard était pour la transformation d'une mole à TAPN? Comment elle peut changer selon la température si TAPN est fixé à 25°C?
Merci