Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 3mSalut, j'ai des questions sur la formule Q1 = -Q2
J'ai oublie la formule
Mercii
-
Vérifiée par Alloprof
Secondaire 5 • 3mje comprend pas comment reconnaitre quelque chose qui est endothermique ou exothermique comme par exemple la congelation de leau, la combustion du bois, la fermentation du raisin, explosion de TNT, désintégration de luranium et encore moin savoir si cest physique ou chimique
-
Vérifiée par Alloprof
Secondaire 4 • 3mBonjour! Est-ce que quelqu'un pourrait m'expliquer c'est quoi le principe d'adopter la configuration électronique d'un des gaz nobles quand un atome devient un ion?
Genre, est-ce que c'est juste quand le nombre d'électrons de l'ion est pareil au nombre d'électrons d'un des gaz nobles? Par exemple, dans mon cahier, on dit que l'aluminium adopte la configuration électronique du néon. Est-ce que c'est parce que la forme ionique de l'aluminium possède 10 électrons tout comme le néon?
Merci et passez une bonne soirée! :D
-
Vérifiée par Alloprof
Primaire 6 • 3msa ser a quoi pourquooooiiiiii
-
Vérifiée par Alloprof
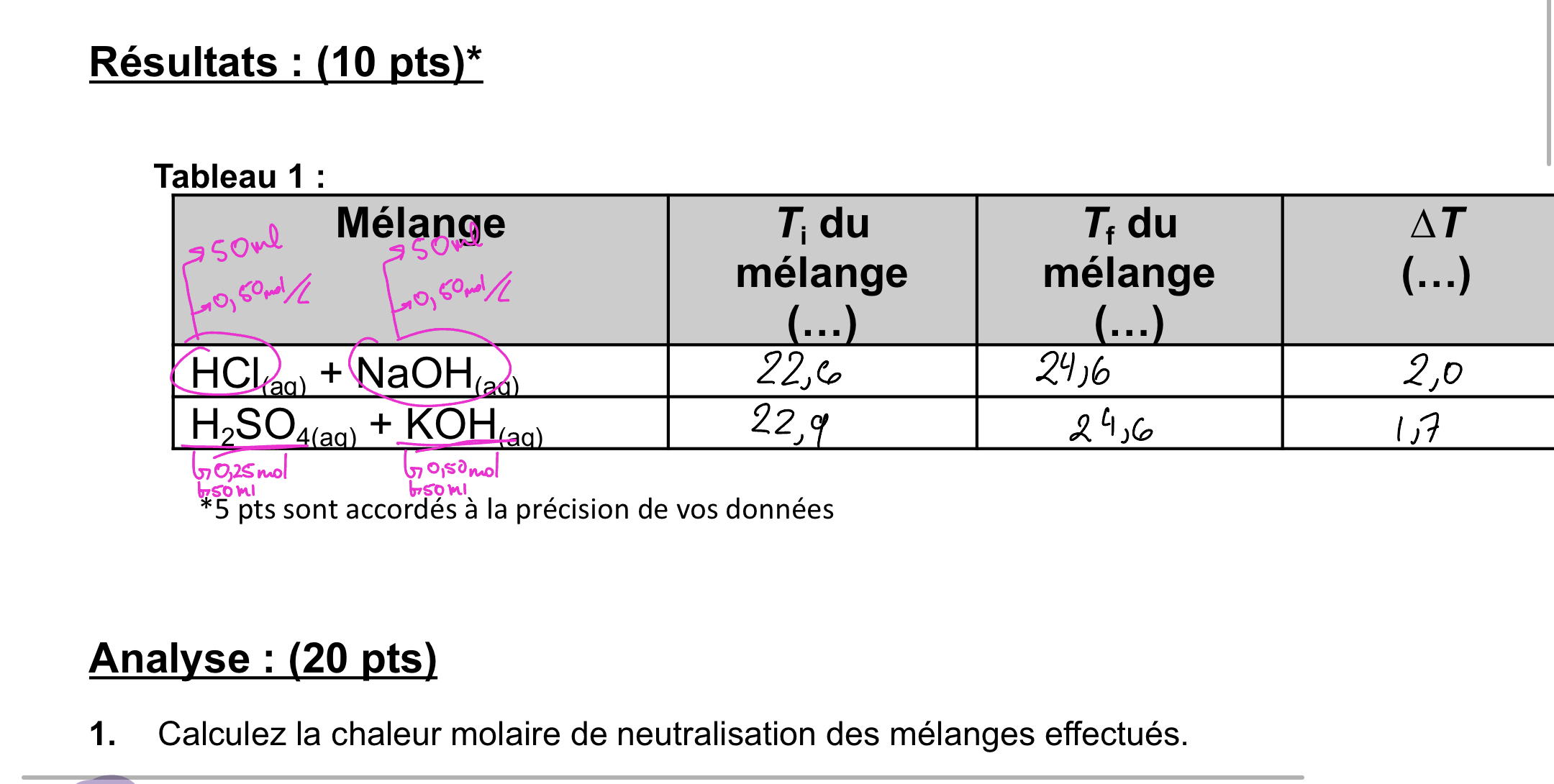
Secondaire 5 • 3mComme suis-je supposé trouver la chaleur molaire des deux réactions?
-
Vérifiée par Alloprof
Secondaire 5 • 3mQuelle est la chaleur molaire de neutralisation du NaOH solide?
-
Vérifiée par Alloprof
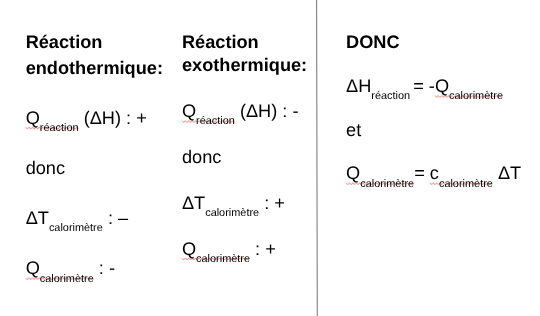
Secondaire 5 • 3mBonsoir!
On nous a présenté ces formules en calorimétrie, mais je ne suis pas certaine de comprendre ce qu'elles représentent et pourquoi elles représentent cela.
Je ne sais pas si ma question est claire, mais si oui, est-ce que quelqu'un peut m'expliquer?
Merci!
-
Vérifiée par Alloprof
Secondaire 4 • 3mSalut !
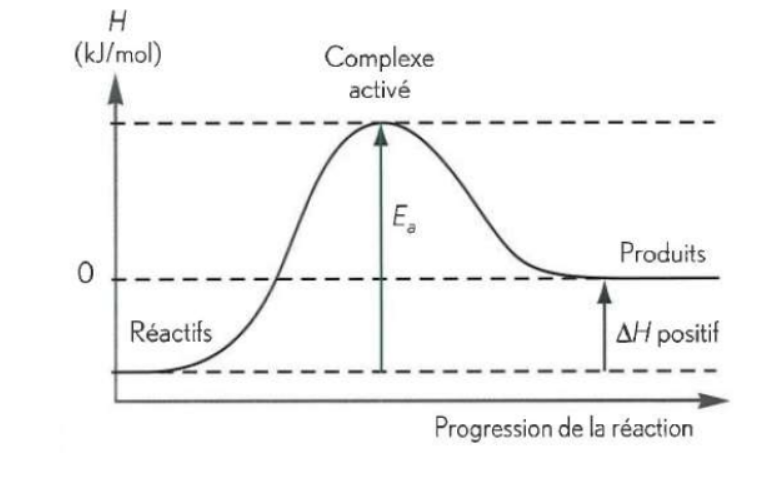
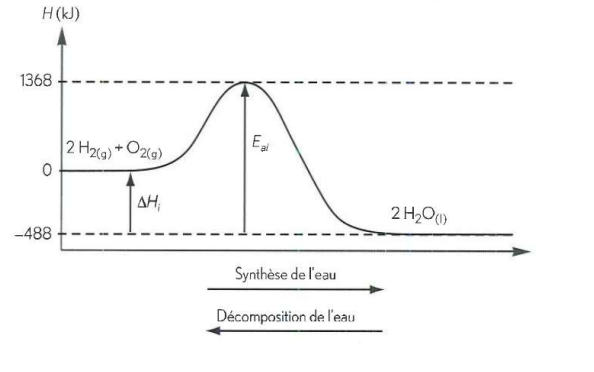
Pourquoi dans ces diagrammes, 𝐻 est soit en kJ ou en kJ/mol? Que font les moles ici. À quoi concrètement serves-t-elles dans sans exercices? Est-ce que ces unités de mesure sont interchangeables
-
Vérifiée par Alloprof
Secondaire 5 • 3mSalut je me demandais comment calculer l’énergie du Na (il faut que je trouve le delta H des réactifs et mes réactifs sont le NaOH). La liaison du O-H est connue mais je sais pas pour le reste.
-
Vérifiée par Alloprof
Secondaire 5 • 3mcomment isoler la variable temperature dans la formule p1v1/n1t1=p2v2/n2t2 avec la quantiter de gaz qui est constante
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour
à part sa stabilité chimique est ce que
le borax a un autre type de stabilité?
-
Vérifiée par Alloprof
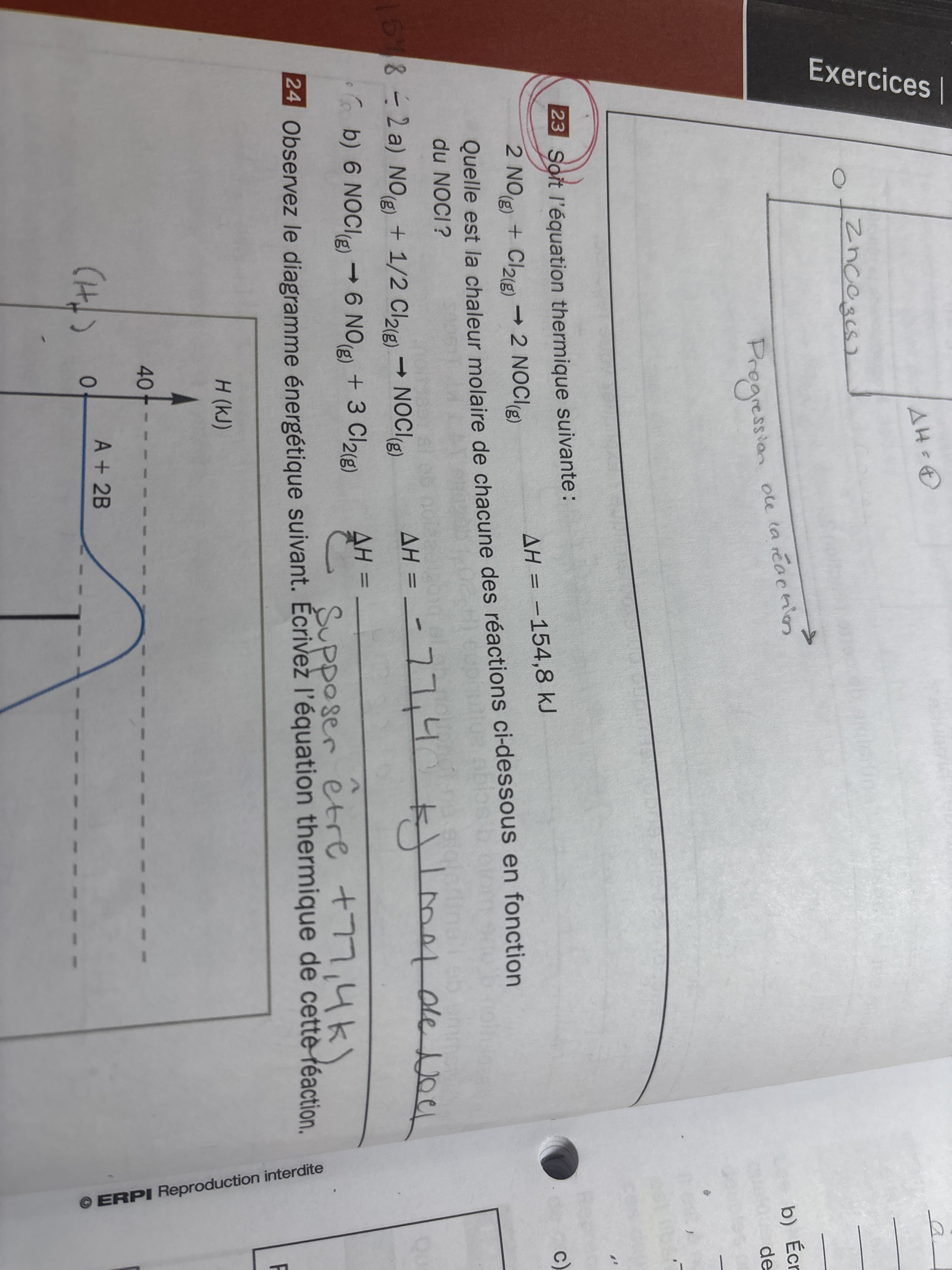
Secondaire 5 • 3mJ’arrive pas à comprendre comment résoudre le B) de la question 23. Est-ce que quelqu’un peut m’expliquer svp?
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour j'avais une petite question concernant le cours de chimie de secondaire 5: Est-ce que toutes les réactions de décomposition (dissolution) sont nécessairement endothermiques? Pouvez-vous m'éclaircir ceci avec quelques exemples ou de contre exemples afin de mieux comprendre svp?
-
Vérifiée par Alloprof
Secondaire 1 • 3mBonjours j'aimerais savoir si lors de la rédaction d un raport de lab sur la séparation des mélanges (sédimentation et décantation distillation ect) il faut préciser de quoi a l'air la substance par exemple
avant la distillation l'eau est mélanger au colorant,[ elle est verdatre et translucide]
aprèss la ditillation l eau est dans un bécher séparer de celui de colorant, [elle est maintenat translucide]
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3mbonjour je suis pas certaine de comprendre pourquoi le borax est tres stable. je sais qu'il réagit pas vraiment avec l'air et se décompose pas, mais est-ce qu'il y a autre chose lié a sa stabilité qui lui donne un avantage?
-
Vérifiée par Alloprof
Secondaire 4 • 3mBonjour! Petite question de chimie sur les réactions endo/exo!
Donc on voit les réactions endothermiques et exothermiques en STE et j'ai beaucoup de réponses différentes à leur sujet et donc j'aimerais avoir une réponse qui n'est pas ambiguë afin de bien comprendre. Mon enseignante a dit que lorsqu'une réaction est endothermique elle absorbe de la chaleur et donc la substance se réchauffe à cause de l'absorption de chaleur (température des produits plus élevée que celle des réactifs). Ensuite, elle nous a dit que les réactions exothermiques dégagent de la chaleur dans l'environnement et donc le température diminue puisque la chaleur sort (température des produits moins élevée que celle des réactifs).
Maintenant mon problème principal est que mon cahier dit l'inverse et mon intuition aussi. Si on y pense la combustion du bois est une réaction exothermique. Cependant, la réaction dégage de la chaleur dans l'environnement et la substance elle même (le bois) se réchauffe aussi, elle n'est pas plus froide qu'au début. Donc j'aimerais comprendre svp.
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3mJe crois que c'est le bilan énergétique mais je ne suis pas sur. Dans mon cahier il y a exemple
4 H 2 O = H - O - H et 3 CO2 = O = C = O
H - O - H O = C = O
H - O - H O = C = O
H - O - H
Comment je fais pour savoir s'il y a une ou deux lignes ?
-
Vérifiée par Alloprof
Secondaire 5 • 3mAllô! Je fais le chapitre 4, La chaleur molaire d'une réaction chimique dans le cahier éléments. C'est quoi la différence entre delta H et Delta H(réaction)? C'est quoi que je dois identifier dans le problème écrit pour bien y associer les variables dans mes calculs? Merci beaucoup, voici des photos pour que vous compreniez mieux ma question.
-
Vérifiée par Alloprof
Secondaire 5 • 3mComment faire pour trouver l’énergie d’activation.
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour!
Je ne suis pas capable de faire ce numéro, je n'arrive pas à comprendre quelle est la valeur de l'enthalpie des produits, des réactifs et celle de l'énergie d'activation. Est-ce que quelqu'un peut m'aider?
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour comment je résous cette équation de stœchiométrie svp
-
Vérifiée par Alloprof
Secondaire 5 • 3mdans un bilan énergetique, comment savoir de quelles type de liaison sagit t`il ?
(liaison simple,double, ou triple
-
Vérifiée par Alloprof
Secondaire 5 • 3mdans un bilan énergetique, comment savoir de quelles type de liaison sagit t`il ?
(liaison simple,double, ou triple
-
Vérifiée par Alloprof
Secondaire 5 • 3mComment calculer l'énergie d'activation si on a les liaisons et la formule thermochimique mais pas le complexe d'activité.
Je suis bloqué sur un numéro au je doit trouver l'énergie d'activation de la réaction de décompostion de l'ammoniac (NH3) en diazote (N2) et dihydrogène (H2). Ont sait que les liaisons N-H sont simples.
-
Vérifiée par Alloprof
Secondaire 5 • 3mbonjour ,j’ai commencer la stochiometrie et je ne comprend vraiment pas comment effectuer les calculs à la fin selon ce qu’on demande je ne sais pas pas où placer mes chiffres lors du calcul de la recherche d’un produit .Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3mDans la loi de Hess, si je veux trouver l'équation globale, comment je sais quelle molécules multiplier ou quelle équation inverser?
-
Vérifiée par Alloprof
Secondaire 5 • 4mquelle est la différence entre la pression relative et absolue
-
Vérifiée par Alloprof
Secondaire 5 • 4mBonjour,
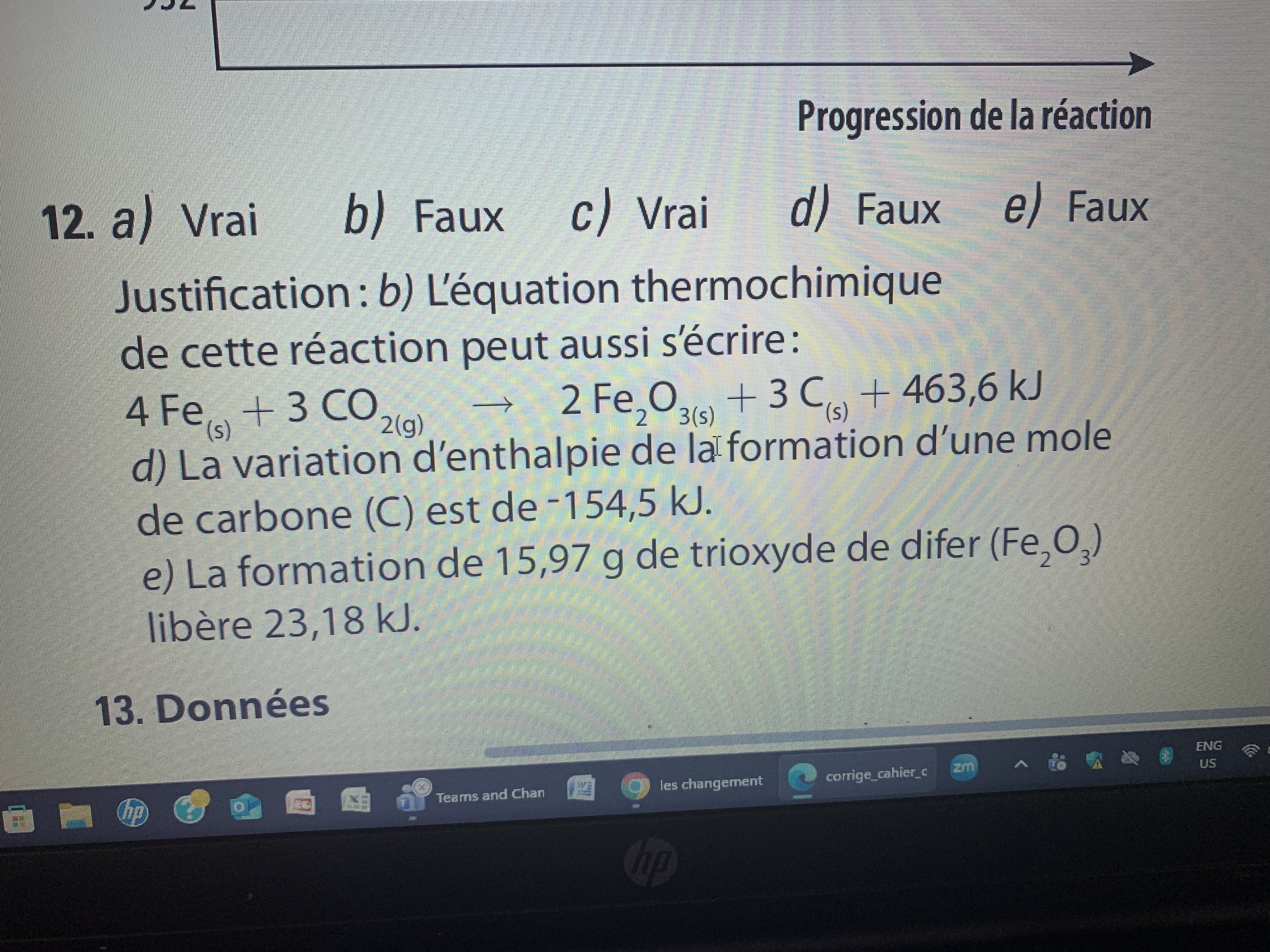
je ne comprends pas le c) et le d). Je comprends pas cmt il faut trouver la variation d’entalphie pour chacun? Ça me donne toujours la mauvais réponse . Je sais pas les calculs à faire pour trouver la variation .g mit le corriger
merci bcp
-
Vérifiée par Alloprof
Primaire 6 • 4mj'aimerais avoir des questions sur le tableau périaudique
-
Vérifiée par Alloprof
Secondaire 5 • 4mJe ne comprend pas ces questions:
Que devient la pression d'un gaz si son volume est réduit de moité tandis que la valeur de la température absolue double ??
combien y'a t'il de mol de O2 dans 20L d'air a TPN ???
Qu'arrive t'il a la pression d'un gaz lorsque la température absolue double et le volume double lui aussi ???