Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 6mAllo! Imaginons que j'ai un gaz et que j'étudie le changement de sa vitesse avec les variables de la masse molaire du gaz et de sa température. Si la masse molaire augmente, la vitesse diminuera. Si la température augmente, la vitesse augmentera. Alors, si ces deux changements arrivent, est-ce que la vitesse restera la même?
-
Vérifiée par Alloprof
Secondaire 5 • 6mBonojur,
Demain, j'ai un examen et mon prof à dit qu'il fallait savoir faire " La mesure d'une pression partielle de vapeur d'eau dans une expérience où on recueille un gaz par la méthode de déplacement d'eau". Je ne comprends pas se qu'elle veut dire par là puisqu'on apprend présentement la loi général des gaz. Bref, pourriez-vous m'expliquer ce que c'est exactement et comment faire avec un exemple svp?
-
Vérifiée par Alloprof
Secondaire 5 • 6mcomment calcul l'incertitude relative et la reconvertir en absolue
-
Vérifiée par Alloprof
Secondaire 5 • 6mBonjour! Je me demandais si il fallait toujours trouver la chaleur molaire pour trouver la chaleur massique ou si il y a un moyen de la trouver directement?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 6mAllo! On me demande de prévoir l'effet d'un changement de température ou de masse molaire sur la vitesse des gaz avec la formule suivante: Ec=1/2mv*2. J'arrive donc avec une quantité d'énergie cinétique mais je ne comprends pas quel est le rapport entre cette formule et la température puisqu'elle n'est pas dans mes variables ?
-
Vérifiée par Alloprof
Secondaire 5 • 6mAllo! Est-ce que sans les liaisons covalentes simples, doubles et triples, il y en a une plus forte ou un ordre de force entre les 3?
-
Vérifiée par Alloprof
Secondaire 5 • 6mAllo! Pourquoi est-ce que la liaison covalente est plus forte que la liaison ionique ?
-
Vérifiée par Alloprof
Secondaire 1 • 6mBonjour, j'ai vraiment besoin d'aide!!!
Demain j'ai examen de science et je suis nul!!!!!!!!!!!
Donc est ce que peut m'aider?? Avec ca?Merciiii
-
Vérifiée par Alloprof
Secondaire 5 • 6mBonjour, j'espère que vous allez bien !
Je ne comprends pas pourquoi, dans l'exercice de la fiche Le bilan énergétique d'une réaction, nous avons conclu que le produit 2 H2O a 4 liaisons simples et non seulement 2, si le coefficient est 2.
<< 2 H2O : Il y a 4 liaisons simples O - H >>
Pour le réactif 2 O2, nous avons trouvé 2 liaisons doubles O = O.
Merci pour votre temps !
-
Vérifiée par Alloprof
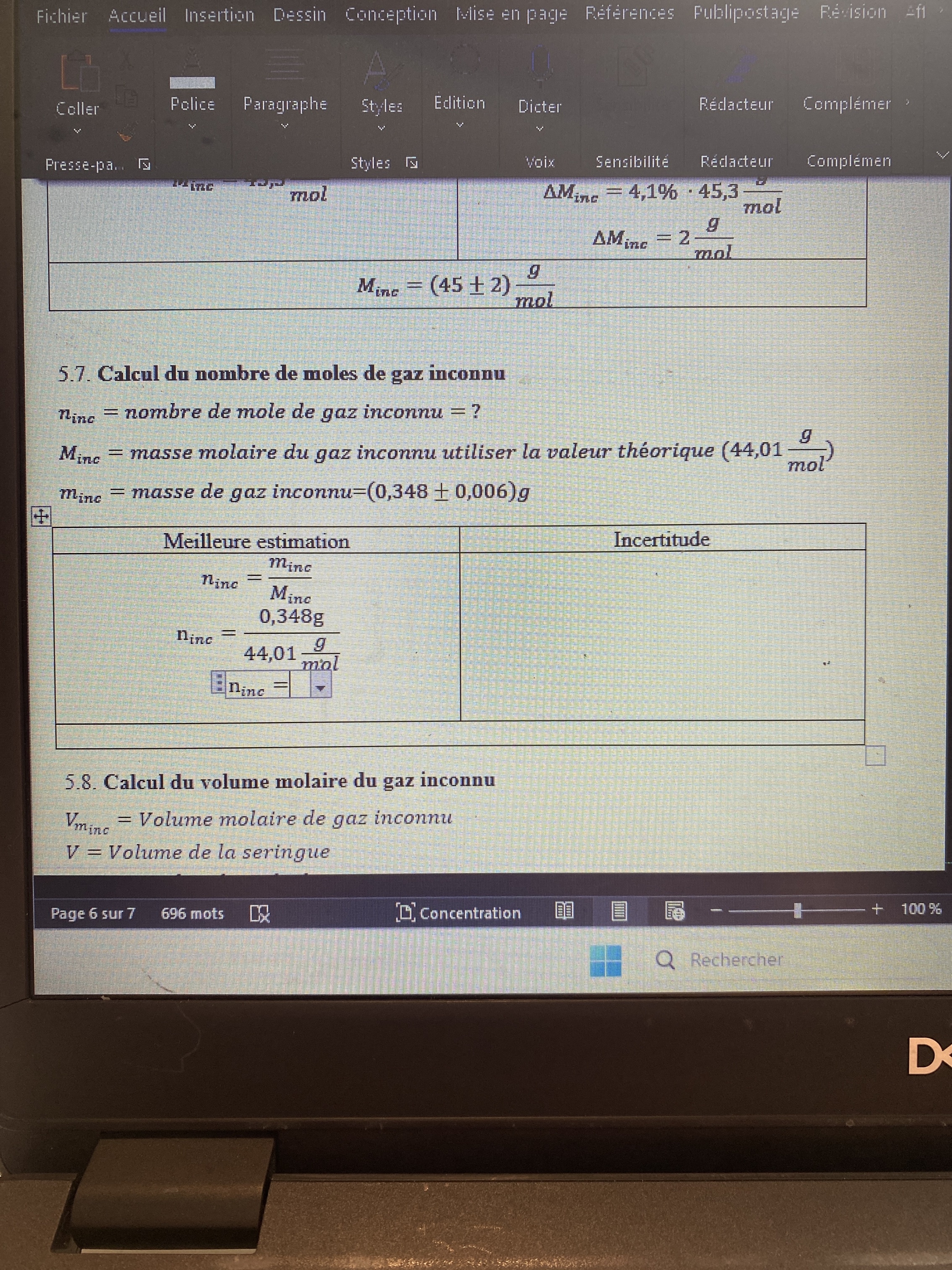
Secondaire 5 • 6mQuel Minc. Dois je utiliser le 44,01 g/mol ( note prof ) ou mon 45+-2 g /mol
-
Vérifiée par Alloprof
Secondaire 5 • 6mEst ce possible ce que j’ai fais
-
Vérifiée par Alloprof
Secondaire 5 • 6mJe ne comprends pas cette question est-ce que quelqu’un pourrait s’il-te plaît me l’expliquer
-
Vérifiée par Alloprof
Secondaire 5 • 6mLorsqu'on effectue la relation entre le volume d'un gaz et la quantité de celui-ci (V/n ou loi d'avogadro), est-ce que la nature du gaz influence cette relation? Par example, si on utilise du diazote ou du dioxyde de carbone, est-ce qu'il y aura une différence entre leur constantes?
-
Vérifiée par Alloprof
Secondaire 5 • 6mje ne comprends pas comment faire ce probleme.
Selon la loi de Hess, quelle est la chaleur molaire de formation de l’éthane (C2H6) dans ce cas-ci?
2 NH3(g) + 2 CO2(g)
C2H6(g) + 2 NO2(g)
-
Vérifiée par Alloprof
Secondaire 5 • 6mBonjour ! Dans l'exercice de la bille d'aluminium dans de l'eau, de la fiche "Les calculs de chaleur", je ne comprends pas comment nous avons supposé, dès le début, que toute l'énergie dégagée par la bille d'aluminium a été absorbée par l'eau. Avec quelles informations devrais-je en arriver à cette conclusion, lors d'un examen par exemple ? Merci :)
-
Vérifiée par Alloprof
Secondaire 5 • 6mEst-ce que quelq'un peu menvoyer quelquechose qui me montre comment faire une conclusion en chimie?
-
Vérifiée par Alloprof
Secondaire 5 • 6mBonjour, afin de réaliser un travail de vulgarisation scientifique, je dois expliquer ce qu'est une protéine substrat et une enzyme pour expliquer le phénomène de bioluminescence. Cependant, je ne trouve pas d'explication claire, alors pourriez-vous m'aider s'il vous plaît?
Merci en avance!
-
Vérifiée par Alloprof
Secondaire 5 • 6mBonsoir,
Dans le cadre de mon laboratoire, je dois inscrire la mesure de chacune de mes données ainsi que l’incertitude associée, comme le montre le tableau ci-dessous :Toutefois, je me demandais quelle pourrait être l’incertitude associée à la mesure d’un papier pH? Est-ce que l’incertitude peut s’appliquer dans le contexte d’une mesure à l’aide d’un papier pH?
Merci et bonne soirée,
LucioleLucide6774
-
Vérifiée par Alloprof
Secondaire 5 • 6mBonjour! Y a t-il une loi simple des gaz qui relie le nombre de mole à la température? Ou cela n'existe pas?
-
Vérifiée par Alloprof
Secondaire 5 • 6mComment faut il trouver les molécules standards à 25°C pour faire des réactions élémentaire dans la loi de Hess?
-
Vérifiée par Alloprof
Secondaire 5 • 6mBonjour je comprends pas ce que je dois faire pour cette question dans mon devoir de chimie (pardon pour la mauvaise qualité d'image)
-
Vérifiée par Alloprof
Primaire 5 • 6mJe ne comprend pas comment trouver les facteurs limitant en chimie secondaire 5
-
Vérifiée par Alloprof
Primaire 5 • 6mpeut tu exploser de quoi des détail
-
Vérifiée par Alloprof
Secondaire 5 • 6mJ’ai de la misère avec ce problème, je sais que la formule est v1/v2= racine carré M2/M1, mais je ne comprends pas comment le faire
-
Vérifiée par Alloprof
Secondaire 5 • 6mComment est ce que je fais la conversion mm Hg -> kPa -> atm avec la logique de 760 mmHg = 101,3 kPa = 1 atm si j’ai une valeur de 78 cm Hg et 1345 pa? Je veut convertir à atm
-
Vérifiée par Alloprof
Secondaire 3 • 6mBonjour,
Je n'ai pas bien compris les PPM, est ce que quelqu'un pourrait m'expliquer s.v.p? L'explication du document n'est pas très claire pour moi...
-
Vérifiée par Alloprof
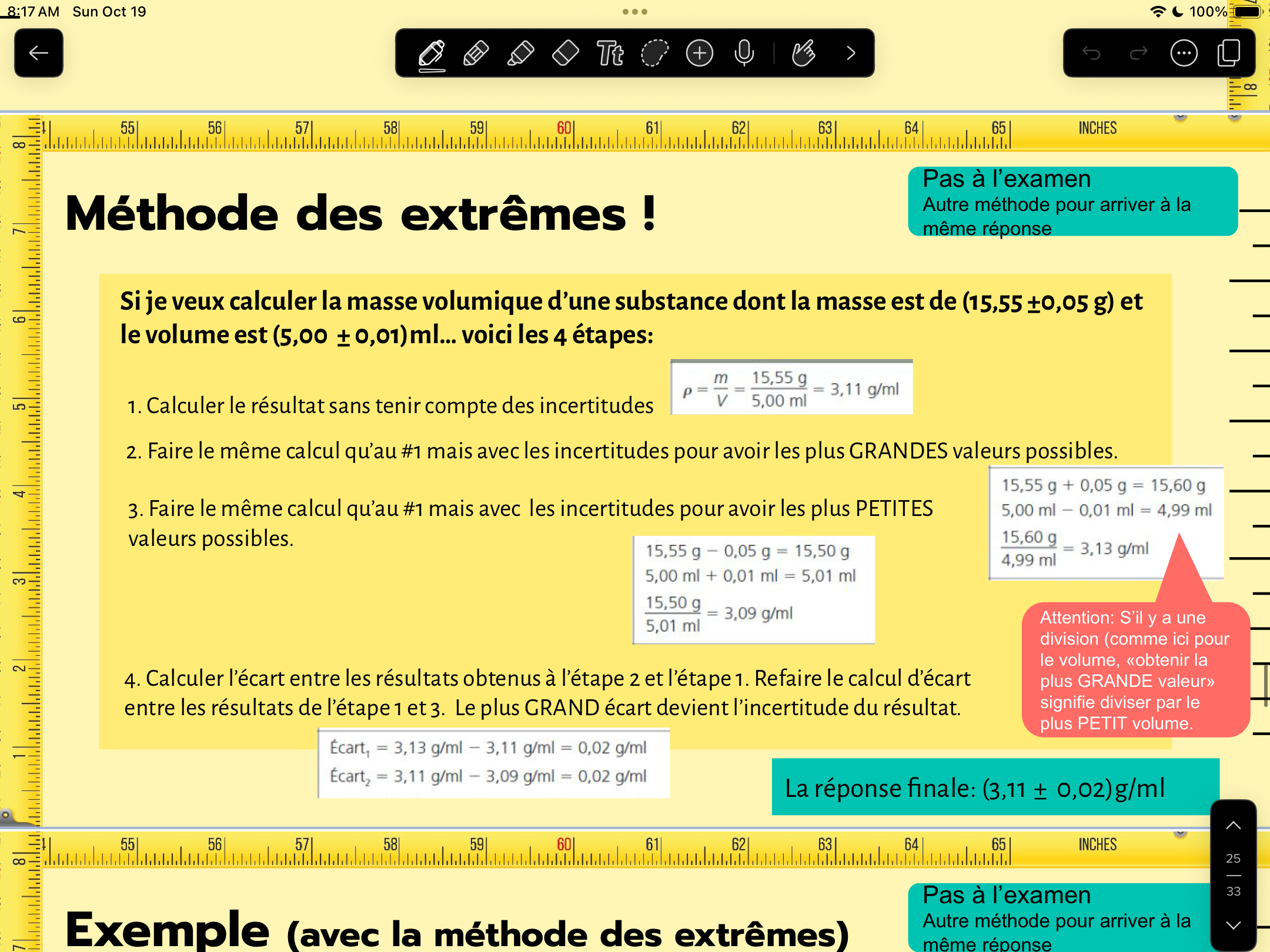
Secondaire 5 • 6mJe ne comprends pas comment faire la méthode des extrêmes pour les incertitudes dans une situation où je fais un produit croisé .Ma prof m’a montré de cette façon.
-
Vérifiée par Alloprof
Secondaire 5 • 6mquelles pourrait etre les nombreuse cause d'erreurs dans un labo de chimie?
-
Vérifiée par Alloprof
Secondaire 5 • 6mAfin de diminuer l'utilisation des énergies fossiles, certaines pompes de station-service mentionnent que l'essence peut contenir une certaine quantité d'éthanol (CH3CH2OH). Quelle est la quantité d'énergie fournie, par gramme de Quelle est la quantité d'énergie fournie, par gramme de CH3CH2OH, lors de la combustion?
2 CH3CH2OH + 6 O2 ---) 4CO2 + 6H2O
Pouvez-vous m'expliquer comment résoudre cette problème? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 6mSi j'ai une solubilité en g/L, pour la convertir en g/100ml, je dois juste faire g/L fois 0,100 pour avoir une solubilité de g/100ml?