Matières
Niveaux
Une molécule est un regroupement d’au moins deux atomes liés chimiquement entre eux.
Selon le modèle atomique de Dalton, les atomes sont représentés par des boules de couleur. Ainsi, une molécule est représentée par une combinaison d’au moins deux boules.
La molécule représentée dans l’image suivante est une combinaison de trois atomes liés chimiquement.
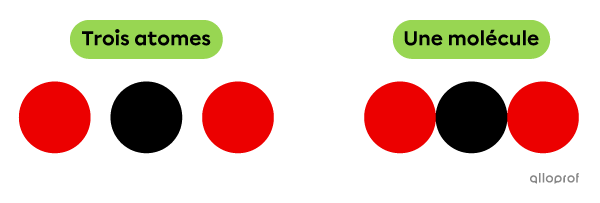
Des atomes et une molécule
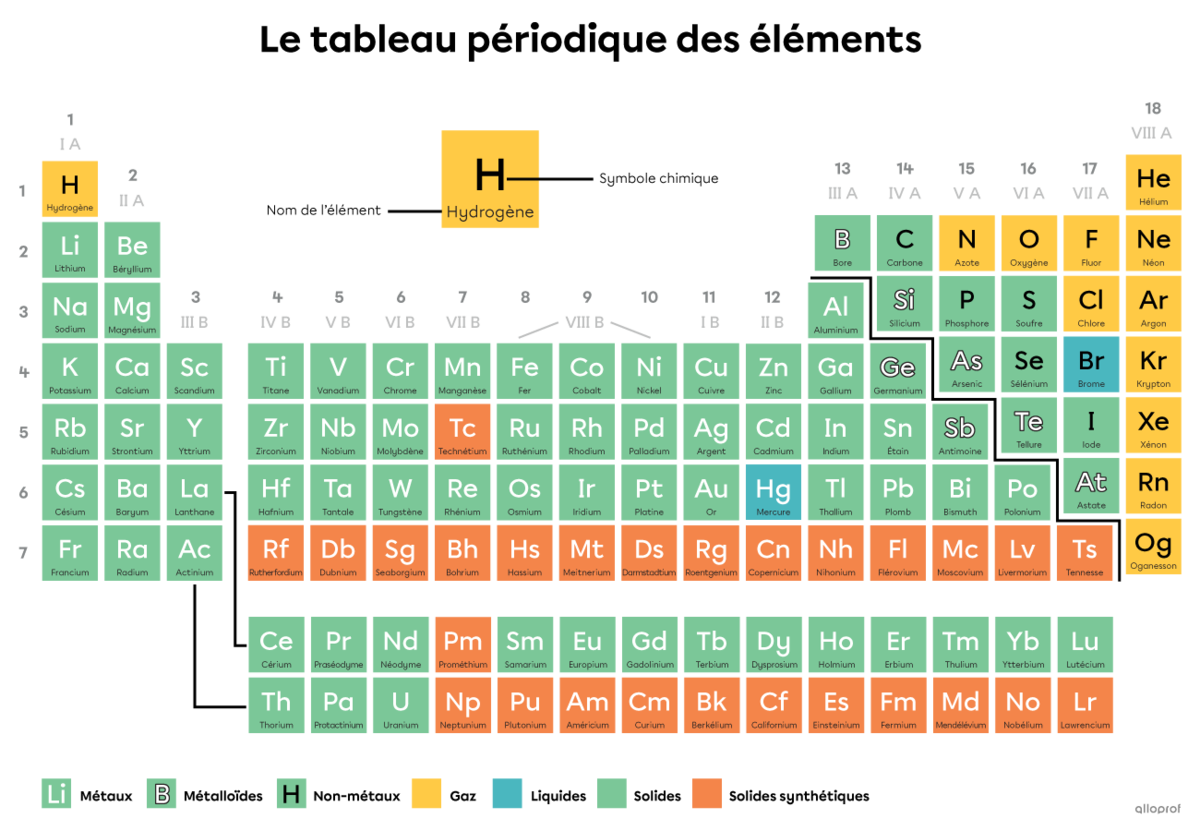
Dans le tableau périodique des éléments, on retrouve tous les éléments, c’est-à-dire toutes les sortes d’atomes. Une molécule est une combinaison d’au moins deux atomes figurant dans le tableau périodique. Ces atomes peuvent être de même sorte ou de sortes différentes.
La molécule de dioxygène |\text{(O}_2)| est faite de deux atomes d’oxygène |(\text{O}).|

La molécule de dioxygène
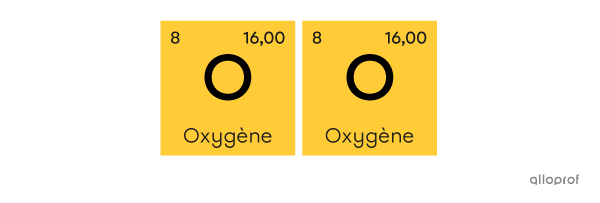
Deux atomes d’oxygène
La molécule d’acide acétique |(\text{CH}_3\text{COOH})| est faite de quatre atomes d’hydrogène |(\text{H}),| de deux atomes de carbone |(\text{C})| et de deux atomes d’oxygène |(\text{O}).|
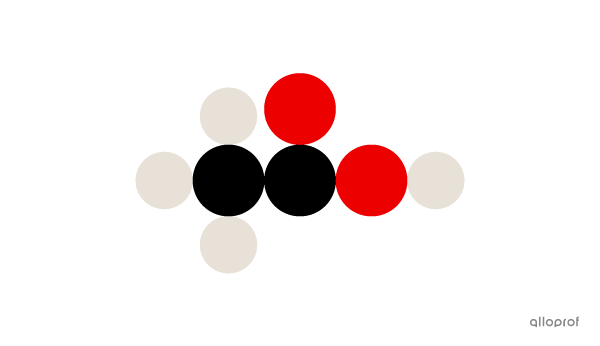
La molécule d’acide acétique
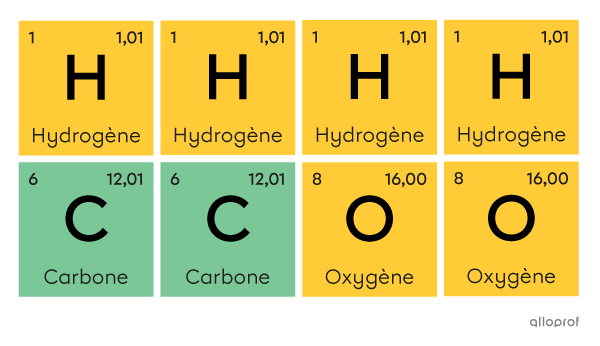
Quatre atomes d’hydrogène, deux atomes de carbone et deux atomes d’oxygène

Moments dans la vidéo :
Pour reconnaitre une molécule à partir de sa formule chimique, on peut vérifier si on y retrouve plus d’une lettre majuscule et/ou un chiffre en indice.
Toutes les sortes d’atomes (éléments) ont un symbole qui ne contient qu’une seule lettre majuscule. Ainsi, lorsque la formule chimique contient plusieurs lettres majuscules, il y a nécessairement présence de plusieurs atomes. Par exemple, |\text{HCl}| contient deux lettres majuscules. Cette substance contient donc deux sortes d’atomes : l’hydrogène |(\text{H})| et le chlore |(\text{Cl}).| C’est une molécule.
L’indice dans une formule chimique indique le nombre d’atomes d’une même sorte qu’on y retrouve. On écrit un indice dans la formule chimique seulement lorsqu’on y retrouve plus d’un atome d’une même sorte. Nécessairement, s’il y a un indice, il y a plus d’un atome. Par exemple, |\text{I}_2| contient un 2 en indice. Cette substance contient donc deux atomes d’iode |(\text{I}).| C’est une molécule.
Une molécule n’a pas les mêmes propriétés que les éléments dont elle est faite.
Lorsque des atomes liés entre eux se séparent et se lient de façon différente, ils forment de nouvelles molécules. Ces nouvelles molécules n’ont pas les mêmes propriétés que les molécules initiales, même si elles sont faites des mêmes atomes. En effet, une réaction chimique s’est produite.
Une molécule d’eau est formée à partir d’oxygène |(\text{O})| et d’hydrogène |(\text{H}).|
Le dioxygène |(\text{O}_2)|, fait d’atomes d’oxygène |(\text{O}),| est un gaz essentiel à la respiration alors que le dihydrogène |(\text{H}_2)|, fait d’atomes d’hydrogène |(\text{H}),| est un gaz inflammable.
La molécule d’eau |(\text{H}_2\text{O}),| quant à elle, n’est pas essentielle à la respiration et n’est pas inflammable. Elle a plutôt la propriété de dissoudre plusieurs substances, comme le sel, le sucre ou le gaz carbonique, par exemple.
Même si la molécule |\text{H}_2\text{O}| est formée des atomes qu’on retrouve dans la molécule |\text{O}_2| et dans la molécule |\text{H}_2,| les propriétés de ces trois molécules sont très différentes.
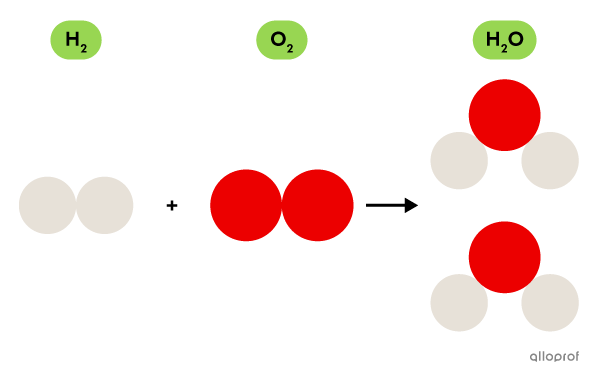
La formation de molécules d’eau
Pour valider ta compréhension à propos de l’organisation de la matière de façon interactive, consulte la MiniRécup suivante.
