Liste de discussions
-
Vérifiée par Alloprof
Secondaire 4 • 1aI am in Secondary 4 and studying for the ST exam, but I am confused about something in the carbon cycle: I know that deforestation is a disruption in the carbon cycle and reduces the flow of carbon from the atmosphere to the biosphere, but how does a larger quantity of carbon dioxide remain in the atmosphere if its being reduced?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour . Comment est ce que je sais qu’elle est l’équation équilibrée de ce problème.”Charles prépare 600 ml d’une solution de trihydroxyde d’aluminium (Al(OH)3(aq)) à une température de 19,0°C. Milan ajoute ensuite 200 ml d’une solution de sulfure de dihydrogène (H2S(aq)) également à une température de 19,0°C. La solution de trihydroxyde d’aluminium (Al(OH)3(aq)) a une concentration de 0,375 mol/L alors que la concentration de la solution de sulfure d’hydrogène (H2S(aq)) est de 0,125 mol/L. Daniel mesure alors la température finale du mélange qui est de 22°C. Écrire l’équation thermique de cette réaction de neutralisation. Le H doit être donné en fonction du sulfure de dihydrogène.
Je n’arrive pas a comprendre comment savoir qcq ce trouve du côté des produits.
-
Vérifiée par Alloprof
Secondaire 5 • 1asi on a le H d'une solution, comment fait-on pour trouver le H d'un seul élément?
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
J'ai bientôt un examen final de chimie sur toute l'année. Avez-vous un conseil pour moi? (en sachant que je perds souvent des points à cause d'erreurs d'inattentions et de calculs).
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
J'ai du mal à savoir de quel côté va le - lorsque j'utilise la formule Q=-Q. Avez-vous une astuce?
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 1aRebonjour,
Mes calculs ne marchent pas, pourquoi ?? Est a cause des formules ??
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Je ne comprends pas cette question. Ces quoi ls pression partielle ?
Merci.
-
Vérifiée par Alloprof
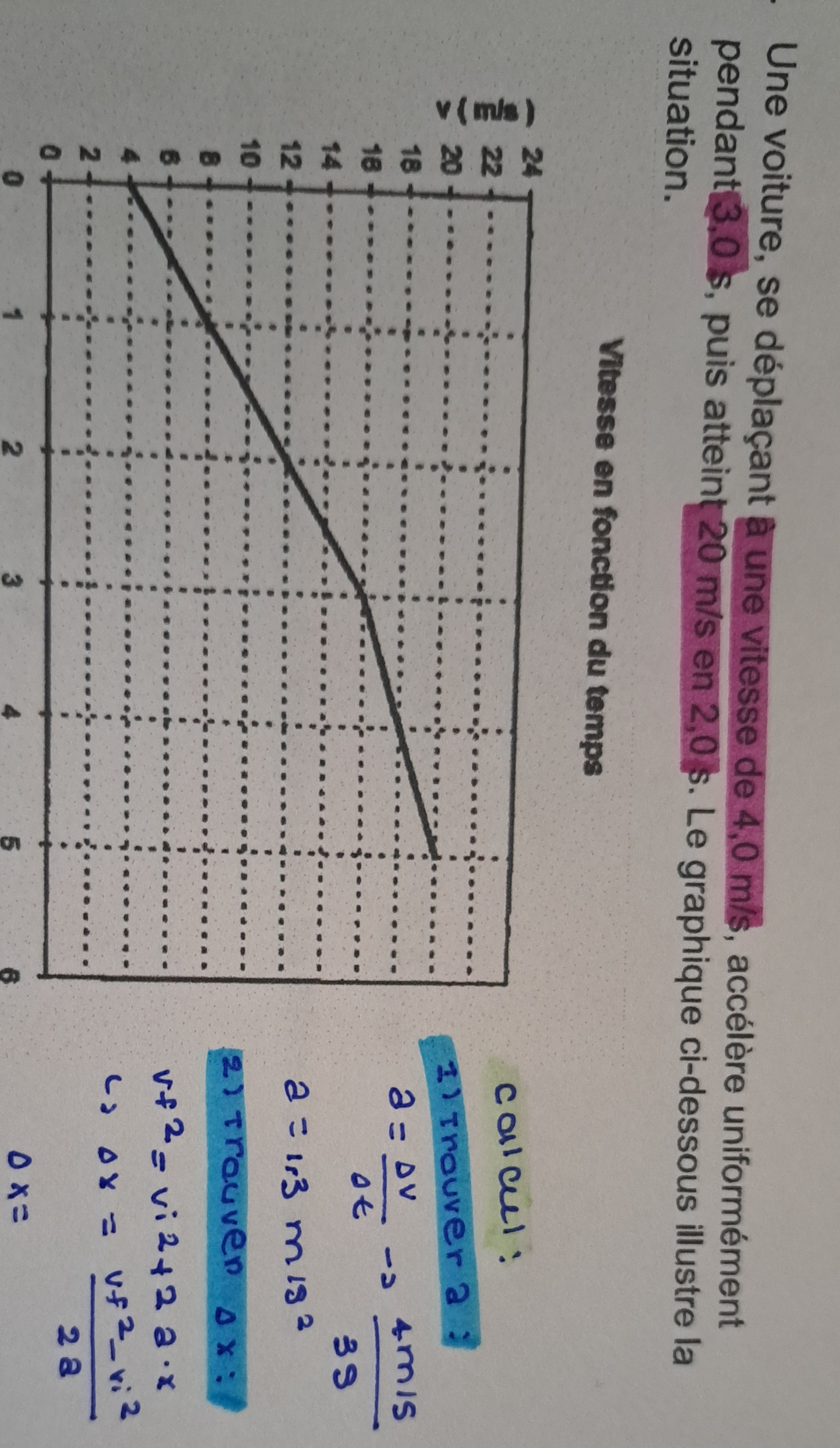
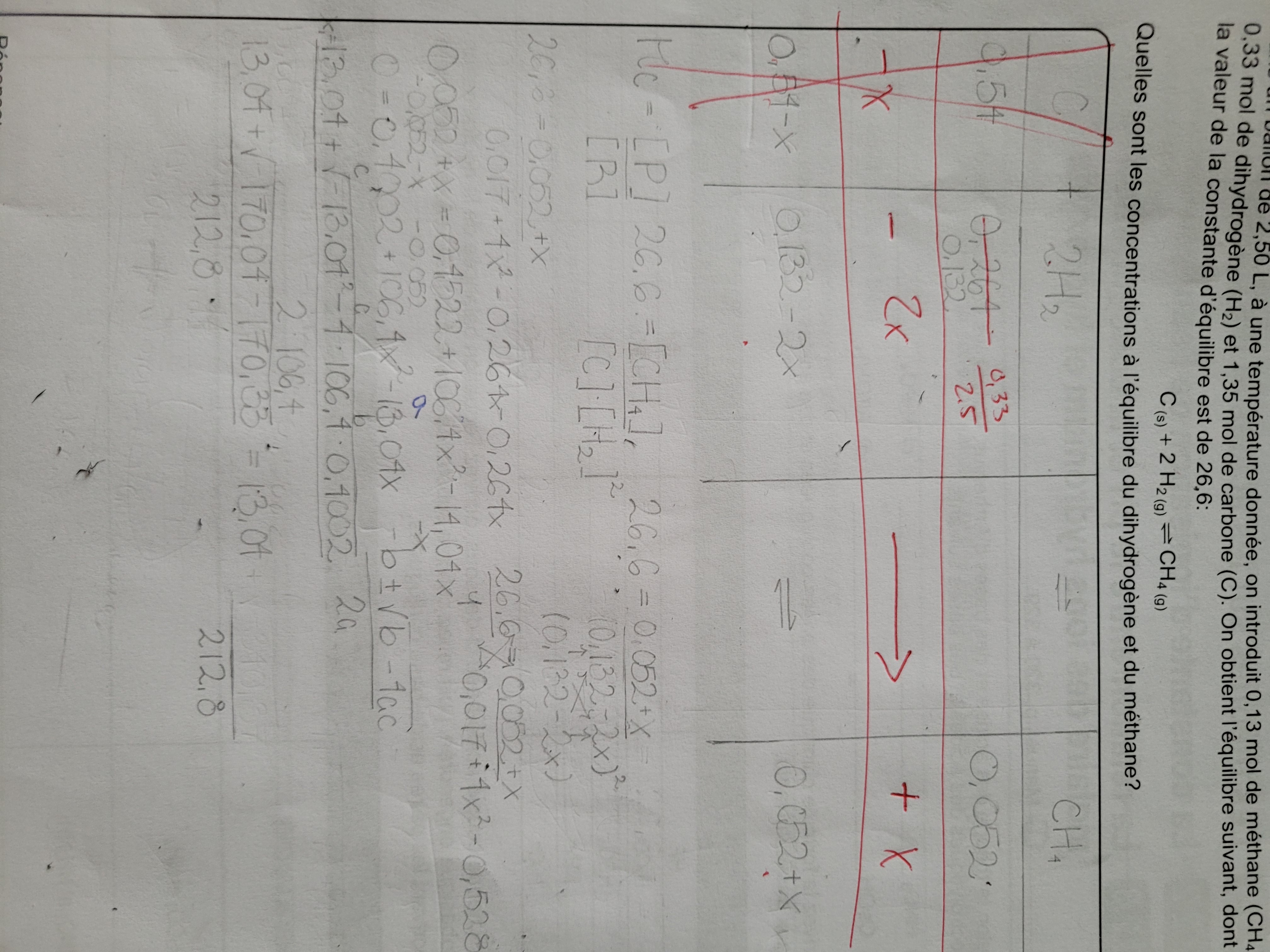
Secondaire 4 • 1aJe me demandais comment faire ma fonction quadratique avec ces variables
A: 106.4
B:-13.04
C: 0.4002
Ils me mènent vers des problèmes complexes, mais je n'ai pas appris cela et ce n'est pas supposé être appris dans mon niveau. Comment dois je faire ?Voici mon problème de chimie
Quel est l'erreur dedans ?
-
Vérifiée par Alloprof
Secondaire 3 • 1aBonjour! Je ne suis pas sûre de comprendre la définition des propriétés chimiques caractéristiques.
Dans mon cahier de sciences, on dit qu'une propriété chimique caractéristique est "le fait qu'une substance réagisse chimiquement avec une substance donnée". Ça veut dire quoi? J'ai regardé votre fiche alloprof, mais j'ai encore des doutes :(
Est-ce que c'est la réaction provoquée par la substance qui est une propriété? Par exemple, un acide va rougir le papier tournesol bleu. Dans mon cahier, on dit que c'est une de leurs propriétés et ceci est une réaction.
Merci beaucoup et bonne soirée à tous!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Quelles sont les bonnes équation partielles ? Je n'ai pas le corrigé de l'exercice.
Merci.
-
Vérifiée par Alloprof
Secondaire 3 • 1aBonjour! J'espère que vous allez bien.
J'ai deux questions en chimie :
- Est-ce que toute réaction chimique ayant du dioxygène dans les réactifs est considérée comme une oxydation? Dans mon cahier, on dit que la combustion et la respiration cellulaire sont des oxydations et chacun de ces phénomènes a de l'oxygène dans les substances initiales...
- Ça sonne peut-être stupide, mais en apprenant les formes d'énergies, je me suis donné comme truc que quand il n'y a rien qui se passe dans l'énoncé, c'est de l'énergie chimique. Est-ce que c'est un bon truc? Par exemple, il fallait mentionner la forme d'énergie pour "un bidon d'essence". Comme il ne se passe rien là-dedans (pas de chaleur, de mouvement, d'alimentation électrique, etc.), j'ai inscris "énergie chimique" et effectivement c'était la bonne réponse. Un autre exemple est "la tarte au sucre". Ça je le savais car on parlait d'aliments, mais encore une fois il n'y avait aucune action. Je m'excuse vraiment si ce n'est pas clair! SVP dites-le moi si c'est le cas et j'essayerai de réécrire ma question plus clairement. Bonne soirée à tous! :)
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Quelles sont les choses à vérifier dans les équations partielles (loi de Hess) avant les calculs. Que doit-on changer?
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Je n'ai pas vrm compris pourquoi le 0,178 est au carré et pourquoi il remplace la fonction.
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour!
comment fait on pour déterminer si une dissociation électrolytique d’un aide est faiblement endothermique ou faiblement exothermique. J’ai vu une question similaire à la mienne, ou un prof répond qu’il en est impossible sauf si tu as des appareils de mesure très précis. Y’a t-il une autre manière de déterminer cela en laboratoire?
merci beacoup!
-
Vérifiée par Alloprof
Secondaire 5 • 1aEn lien avec:https://www.alloprof.qc.ca/zonedentraide/discussion/125601/question/p1D'abord, merci beacoup à Zachary T. pour votre réponse à ma question précédente. Je comprend tout à fait qu'il ne faut pas tenir compte des solides ou liquides pour, par exemple, la constante d'équilibre de concentration d'une réaction chimique.
Cependant, ma confusion se concrétise lorsqu'il y a des susbtances uniquement solides dans les produits, et que je dois calculer la constante d'équilibre.
Je vous donne un exemple concret:Dans le cas ci-dessus, comment puis-je trouver la constante d'équilibre? La concentration du solide devient inévitable dans cette situation, alors est-ce que je la considère comme étant égale à 1 ou nulle?
C'est justement de tels cas qui me confondent.
J'espère que ma question est un peu plus claire :)
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour!
J'ai une grande confusion en chimie, concernant la constante d'équilibre (K).
En fait, considérons l'équation hypothétique suivante:A(aq) + B (g) → C (s) + D (l)1- Je sais que c'est chimiquement illogique, mais j'aimerais juste m'assurer d'une chose dans le cas du calcul du K pour la concentration:
Est-ce que, quand j'écris que K= produits/réactifs, je considère laconcentrationdessolides et liquidescomme étant1, ounulle?
Je demande cela parce que, malgré le fait qu'il ne faut pas tenir compte des concentrations des solides et liquides, j'éprouve de la difficulté quandles produits contiennent que des solides ou liquides.
2- Parallèlement, lapressiondessolides,liquidesetsolutions aqueusesest-elle considéréenulle, ouégale à 1dans les calculs de la constante d'équilibre??
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Pour revenir sur ma question précédente, j’aimerais comprendre comment différencier un acide fort d’un acide faible et aussi connaître la méthode à utiliser pour calculer les valeurs manquantes dans le cas d’un acide fort.
Merci pour votre réponse !
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
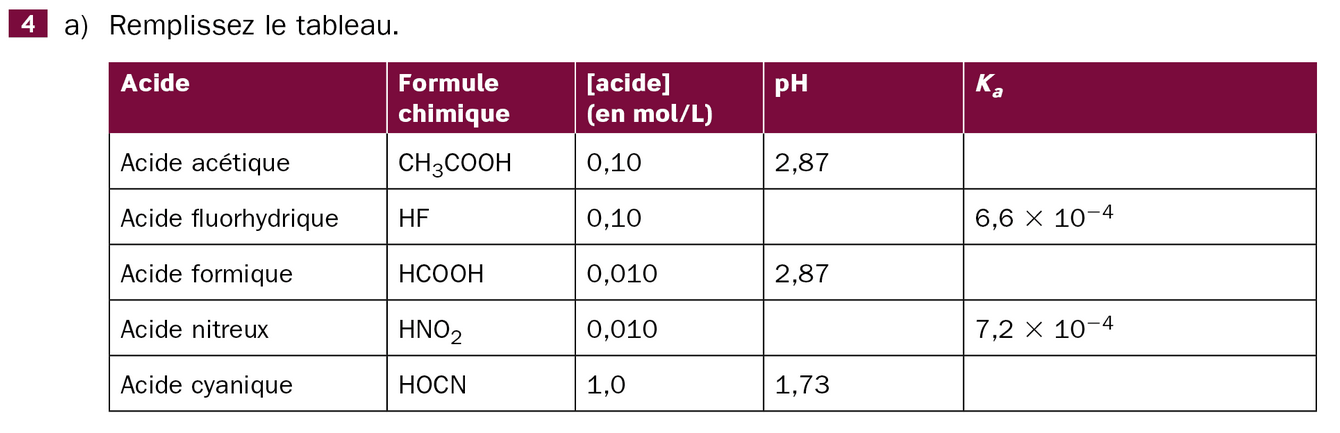
Je suis en train d'étudier les acides et les bases, et j'ai quelques difficultés à comprendre comment calculer le pH et la constante d'acidité des acides de ce tableau.
Pourriez-vous m'expliquer la méthode à suivre ?
Merci d'avance pour votre aide !
-
Vérifiée par Alloprof
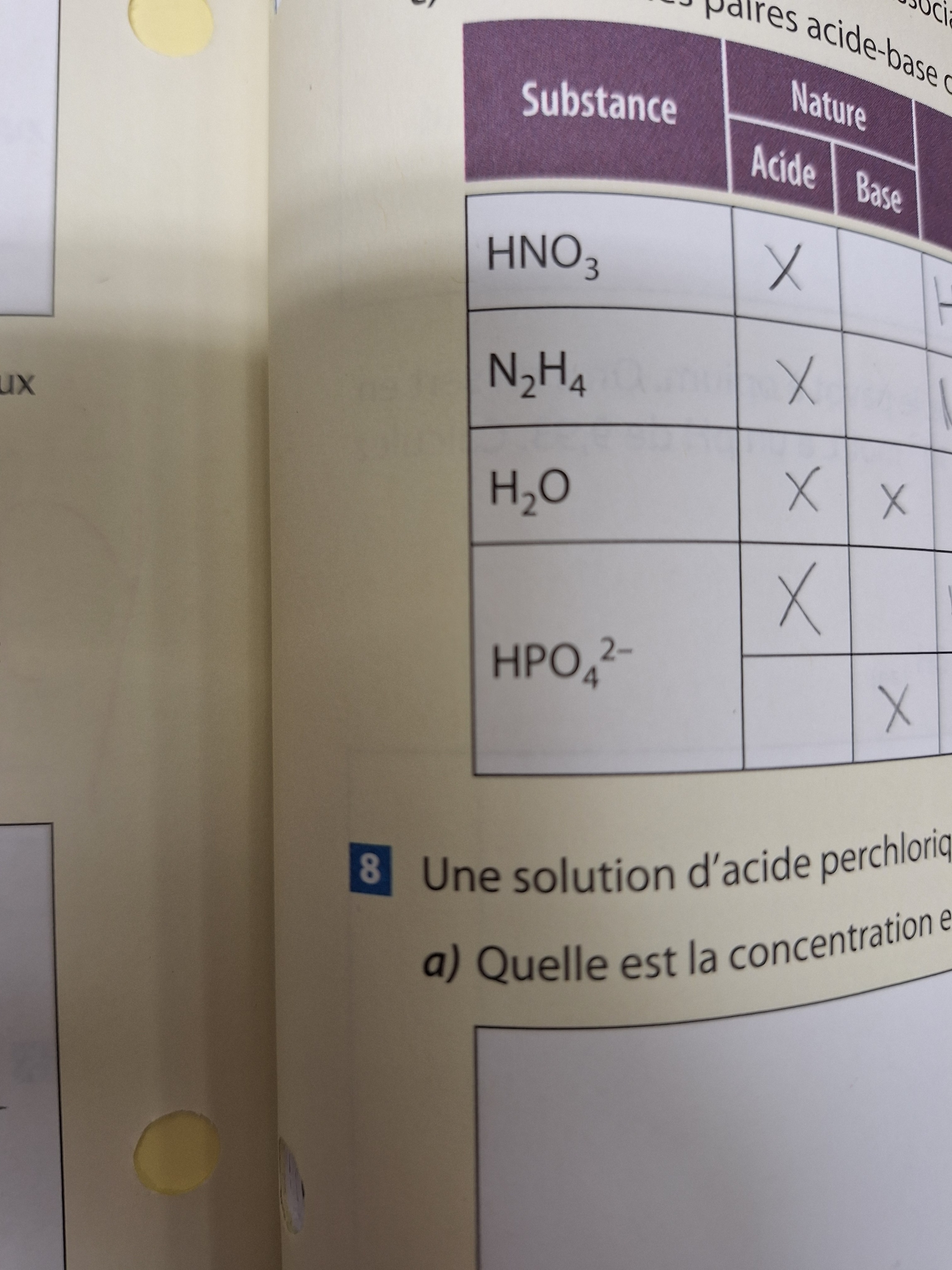
Secondaire 5 • 1aBonjour, comment est-ce possible de savoir si c'est une base ou un acide?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Je rencontre de la difficulté avec un concept. J'aimerais comprendre comment déterminer si un ion sera positif ou négatif dans une équation ou un composé.
Je comprends les règles générales pour les éléments des groupes 1, 2, 13, 15, 16 et 17, en me basant sur leur tendance à perdre ou à gagner des électrons. Cependant, je suis un peu perdu avec les ions polyatomiques et les métaux de transition.
Merci beaucoup pour votre aide !
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, je comprends qu'un système à l'équilibre implique que la vitesse de la réaction directe et indirecte soit identique. Toutefois, lorsque qu'une condition du système est modifiée, cela favorisera une des deux réaction. La vitesse de celle-ci se retrouvera augmentée. Ceci dit, le système n'est plus à l'équilibre. Si tel est le cas, pourquoi, lorsqu'il est question des concentrations dans la constante d'équilibre, sont-elles données à l'équilibre ? Je ne saisis pas très bien la matière, merci de m'éclairer un peu! ( Aussi, si il y a deux types d'équilibres, pourquoi ne sont-ils pas distingués? )
-
Vérifiée par Alloprof
Secondaire 3 • 1aBonjour! J'ai fait un exercice en chimie et j'ai eu un peu de difficulté. Pourriez-vous m'aider à comprendre?
D'abord, voici l'exercice:
"On vous demande de préparer une solution de KNO3 d'une concentration de 50% m/v. Lors de la préparation, vous constatez que le KNO3 refuse de se dissoudre complètement. Expliquez pourquoi et décrivez un moyen de surmonter cette difficulté."
Pour l'explication, j'ai dit que ça devait être parce qu'il y avait trop de KNO3 dans la solution et qu'elle était sursaturée, puisqu'une partie du soluté ne se dissolvait pas. Effectivement, j'avais la bonne réponse.
Pour le moyen de surmonter la difficulté, j'ai pensé à deux choses : Soit on rajoute du solvant, ou bien on chauffe la solution. Je me suis dis qu'en ajoutant du solvant, la concentration diminuerait et ainsi je pourrais en dissoudre davantage. Par contre, la bonne réponse était de chauffer la solution vu que la solubilité des solides augmente lorsque la température augmente.
Alors là je me demande : Pourquoi n'aurais-je pas pu juste ajouter du solvant? Parce que si le soluté ne se dissout pas au complet, en rajoutant du solvant, ça va finir par marcher.... Non?
Peut-être que je ne devrais pas mélanger la concentration et la solubilité. Mais ça me gosse de ne pas savoir pourquoi rajouter du solvant ce n'est pas bon :(
Est-ce que quelqu'un pourrait m'expliquer cela?
Merci beaucoup et bonne soirée à tous!!
:)
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! Je me demandais comment bien exprimer mon hypothèse et son explication pour mon laboratoire de chimie. Pourriez-vous m’aider à élaborer et apporter des corrections si nécessaires. Merci!!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, j’ai besoin d’aide en chimie. Dans un laboratoire, on a utilisé de l’acide acétique concentré à 0,1 mol/L et à un pH de 2,84. On l’a ensuite dilué pour avoir une concentration de 0,005 mol/L et un pH de 3,55. Je suis supposée calculer la constante d’acidité et de basicité (de l’acide à 0,1 mol/L ET de l’acide à 0,005 mol/L) , mais je ne suis pas certaine de bien le faire. Alors pouvez-vous m’expliquer comment faire? Merci beaucoup pour l’aide
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
J'ai de la difficulté avec ce problème, comment le résoudre ?
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 1aQuelqu’un peut m’expliquer pourquoi le NO3 est parti de l’équation (venant de la solution Cu(NO3)2)? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aLors de l'observation d'une réfraction de lumière, nous avons utilisés une lentille semi-circulaire, je me demandais pourquoi nous avons pris ce genre de lentille et non une autre? La lentille était remplie d'eau pour admirer un changement de milieu
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, j’aurais une petite question de chimie, en fait, j’arrive pas à comprendre quelle est la différence entre la constante d’acidité et la constante de basicité. Mes notes de cours sont beaucoup trop difficiles à comprendre et ma prof n’a pas donné d’explication en lien avec cette matière. De plus, Est-ce la constante d’ionisation de l’eau est similaire à celle de l’acidité et la basicité? Aussi, je ne vois rien sur votre site web en lien avec les solides peu solubles ou la constante de produit de solubilité. Pourrais-je avoir une explication de cette matière flou? Je voudrais remercier l’équipe d’Alloprôf pour pouvoir m’aider.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir!
Qu’est-ce que la constante d’acidité représente? Je comprends comment la trouver et la calculer, mais je ne « la » comprends pas.
Merci d’avance!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
je ne comprends pas comment écrire soi-même une réaction de décomposition en chimie, j'ai compris le principe mais je n'arrive pas a comprendre quel élément va avec le quel quand on le décompose....(pourquoi c'est ceux-ci et pas d'autres, l'agencement ).
Merci !